閲覧履歴
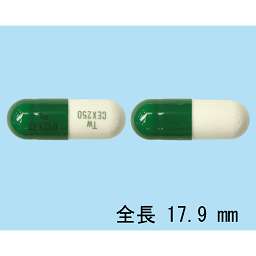
- セファレキシンカプセル250mg「トーワ」 経口用セフェム系抗生物質製剤
- 硝酸イソソルビド徐放カプセル20mg「St」 虚血性心疾患治療剤
- ロラタジンOD錠10mg「AA」 持続性選択H1受容体拮抗・アレルギー性疾患治療剤
- ドキサゾシン錠0.5mg「JG」 血圧降下剤
- イオパミロン注300シリンジ 非イオン性尿路・血管造影剤
- モンテルカスト錠10mg「タカタ」 ロイコトリエン受容体拮抗薬、気管支喘息・アレルギー性鼻炎治療薬
- エパルレスタット錠50mg「日医工」 アルドース還元酵素阻害剤
- アストミンシロップ0.25% 鎮咳剤〈非麻薬〉
- ユニフィルLA錠100mg 気管支拡張剤
- アロキシ静注0.75mg 5-HT3受容体拮抗型制吐剤
- リスペリドン錠2mg「クニヒロ」 抗精神病剤




 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379

