作成又は改訂年月
※※
2014年6月改訂
(第10版、販売名の変更)
※
2009年6月改訂
(第9版)
日本標準商品分類番号
薬効分類名
承認等
販売名
※※ビダラビン軟膏3%「トーワ」
販売名コード
承認・許可番号
※※22500AMX01849
VIDARABINE OINTMENT 3% “TOWA”
薬価基準収載年月
販売開始年月
使用期限等
貯 法:
室温保存、気密容器
使用期限:
外箱、チューブに記載
組成
1g中の
有効成分
ビダラビン…30mg
添加物
白色ワセリン、流動パラフィン
白色の軟膏剤
性状
一般的名称
禁忌
効能・効果
用法・用量
用法・用量に関連する使用上の注意
本剤の使用は、発病初期に近い程効果が期待できるので、原則として発症から5日以内に使用開始すること。
本剤を7日間使用し、改善の兆しがみられないか、あるいは悪化する場合には他の治療に切り替えること。
使用上の注意
重要な基本的注意
本剤は局所治療を目的とした薬剤であるため、発熱、汎発疹等の全身症状がみられる場合又は使用中にあらわれた場合には重症化することがあるので、他の全身的治療を考慮すること。
相互作用
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|
| ペントスタチン | ビダラビン(注射剤)との併用により腎不全、肝不全、神経毒性等の重篤な副作用が発現したとの報告がある。 | ペントスタチンが、ビダラビンの代謝に関与するADA(アデノシンデアミナーゼ)酵素の阻害作用を有するため、ビダラビンの血中濃度が高まることによると考えられる。 |
|---|
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
以下のような副作用があらわれた場合には、症状に応じて適切な処置を行うこと。
妊婦、産婦、授乳婦等への投与
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。[妊娠中の投与に関する安全性は確立していない。なお、静脈投与による動物実験(ラット、ウサギ)で催奇形作用が報告されている。]
小児等への投与
低出生体重児、新生児、乳児に対する安全性は確立していない。(使用経験が少ない)
適用上の注意
使用部位:眼科用として、角膜、結膜には使用しないこと。
その他:本剤の基剤として使用されている油脂性成分は、コンドーム等の避妊用ラテックスゴム製品の品質を劣化・破損する可能性があるため、これらとの接触を避けさせること。
薬効薬理
※※薬力学的試験
抗ウイルス作用
単純ヘルペスウイルスI型腹側部接種マウス(1群10匹)及びアシクロビル耐性ヘルペスウイルスII型腹側部接種マウス(1群10匹)におけるビダラビン軟膏3%「トーワ」及び標準製剤(軟膏剤、(70×2)mg/body/day×14日)の病変スコア、病変発症動物数及び生存日数を指標に比較検討した。
本剤及び標準製剤は、いずれの場合も発症抑制作用を示し生存日数を延長させ、両剤は生物学的に同等と判断された1)。
有効成分に関する理化学的知見
構造式:
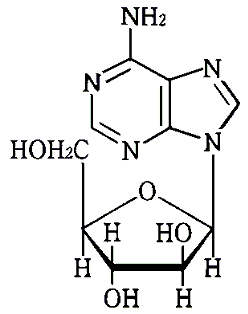
一般名:ビダラビン(Vidarabine)
化学名:9-β-D-arabinofuranosyladenine
分子式:C10H13N5O4
分子量:267.24
性 状:白色の結晶性の粉末で、におい及び味はない。ジメチルスルホキシドに溶けやすく、酢酸(100)に溶けにくく、水又はエタノール(95)に極めて溶けにくく、ジエチルエーテルにほとんど溶けない。吸湿性である。
融 点:約250℃(分解)
取扱い上の注意
※※安定性試験
最終包装製品を用いた加速試験(40℃、相対湿度75%、6ヵ月)の結果、ビダラビン軟膏3%「トーワ」は通常の市場流通下において3年間安定であることが推測された2)。
包装
※※ビダラビン軟膏3%「トーワ」:2g×10、5g×10
主要文献
1
東和薬品株式会社 社内資料:薬力学的試験
2
東和薬品株式会社 社内資料:安定性試験
※文献請求先・製品情報お問い合わせ先
主要文献(社内資料を含む)は下記にご請求下さい。
東和薬品株式会社 学術部DIセンター(24時間受付対応)
〒571-8580 大阪府門真市新橋町2番11号

0120-108-932 TEL 06-6900-9108 FAX 06-6908-5797
http://www.towayakuhin.co.jp/forstaff
製造販売業者等の氏名又は名称及び住所
製造販売元
東和薬品株式会社
大阪府門真市新橋町2番11号

 0120-108-932 TEL 06-6900-9108 FAX 06-6908-5797
0120-108-932 TEL 06-6900-9108 FAX 06-6908-5797