〈国際共同臨床試験(HERA試験)における成績〉
HER2過剰発現の手術可能乳癌患者で、手術、全身的な術前又は術後補助化学療法及び放射線療法(適応となる場合)を完了した患者を対象注6)とし、先行バイオ医薬品§を初回8mg/kg(体重)、2回目以降6mg/kgを3週間間隔で1年間投与した群又は2年間投与した群と、先行バイオ医薬品§を投与しない対照群とで有効性を比較した。なお、先行バイオ医薬品§投与群においては、定期的なLVEF評価に基づき、先行バイオ医薬品§の投与継続あるいは中止が判断された。
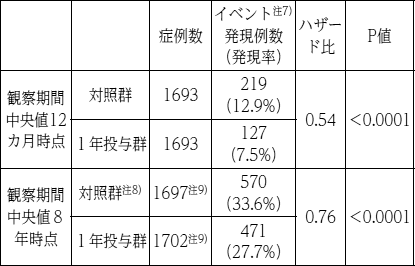
中間解析結果:観察期間中央値12カ月時点で中間解析が実施され、先行バイオ医薬品§1年投与群は対照群に比べて、無病生存に関するイベント注7)発現率が有意に改善された。なお、本試験における国内からの登録被験者の同時点の解析におけるイベント発現率は、1年投与群7.3%(3/41)、対照群13.0%(6/46)であった。
最終解析結果6):観察期間中央値8年時点で最終解析が実施された。先行バイオ医薬品§1年投与群は対照群に比べて、無病生存に関するイベント発現率が有意に改善された。先行バイオ医薬品§2年投与群と1年投与群の比較は、ランダム化の12カ月後に無病かつ生存している被験者に対して実施された。先行バイオ医薬品§2年投与群の無病生存に関するイベント発現率は23.6%(367/1,553)で、1年投与群(23.6%[367/1,552])に比べて有意な改善は認められなかった(HR:0.99、P=0.86)。
また、安全性については、3,355例(1年投与群1,682例、2年投与群1,673例)が解析対象とされ、グレード3又は4の有害事象及び無症候性又は軽度症候性の左室駆出率(LVEF)低下は、1年投与群に比べて2年投与群で発現率が高い傾向が認められた[グレード3又は4の有害事象:1年投与群16.3%(275/1,682例)、2年投与群20.4%(342/1,673例)、無症候性又は軽度症候性の左室駆出率低下:1年投与群4.1%(69/1,682例)、2年投与群7.2%(120/1,673例)]。
(ハーセプチン注射用60・150の添付文書による)
注6)HERA試験では、非転移性で根治的手術が可能であった原発性乳癌患者を対象とした。なお、腋窩リンパ節転移陰性で腫瘍径1cm以下の患者、化学療法が適応されない患者は対象外であった。
1年投与群及び対照群の無病生存に関するイベント発現率の比較
注7)乳癌の再発(部位を問わない)、対側乳癌、乳癌以外の二次癌(皮膚の基底細胞癌及び扁平上皮癌、子宮頸部上皮内癌を除く)の発症、死亡(死因は問わない)
注8)対照群には、中間解析結果発表の後、先行バイオ医薬品§の投与を開始した症例が52.1%(884/1,697)含まれた。
注9)観察期間中央値12カ月時点における解析のためのカットオフ日より後で試験にランダム化された被験者が少数含まれるため、症例数に相違がある。
〈国際共同臨床試験(ToGA試験)における成績〉
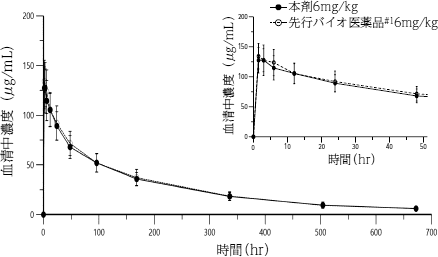
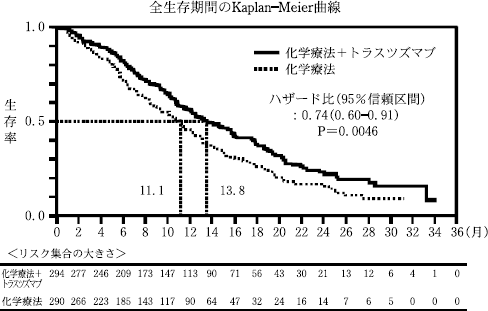
HER2過剰発現(IHC法3+又はFISH法陽性)の進行・再発の胃又は胃食道接合部腺癌患者(化学療法未治療)584例を対象に、化学療法(カペシタビン+シスプラチン又はフルオロウラシル+シスプラチン)と化学療法+先行バイオ医薬品§を比較する第III相臨床試験を実施した。先行バイオ医薬品§は初回8mg/kg(体重)、2回目以降6mg/kgを3週間間隔で、化学療法中止後も病勢進行が認められるまで同一の用法・用量で投与を継続した。化学療法は、カペシタビン1000mg/m2の1日2回14日間経口投与又はフルオロウラシル800mg/m2の5日間持続静脈内投与注10)とシスプラチン80mg/m2の静脈内投与を3週間間隔で行った。目標イベント数の75%時点の中間解析において、化学療法+先行バイオ医薬品§は化学療法単独に比べて、主要評価項目である全生存期間において有意な延長が認められた。なお、化学療法の内訳は584例中、カペシタビン+シスプラチンが511例、フルオロウラシル+シスプラチンが73例であった。国内では、全例(101例)においてカペシタビン+シスプラチンが使用された。
(ハーセプチン注射用60・150の添付文書による)
注10)フルオロウラシルの他の抗悪性腫瘍剤との併用における国内承認用法・用量:フルオロウラシルとして、通常成人1日5〜10mg/kgを他の抗悪性腫瘍剤と併用し、単独で使用する場合の方法に準じ、又は間歇的に週1〜2回用いる。
単独で使用する場合:フルオロウラシルとして、通常成人1日5〜15mg/kgを最初の5日間連日1日1回静脈内に注射又は点滴静注する。以後5〜7.5mg/kgを隔日に1日1回静脈内に注射又は点滴静注する。なお、年齢、症状により適宜増減する。