1
Langowsk JL, et al.:Nature. 2006; 442: 461-456
2
Maeda A, et al.:Cancer Res. 2006; 66: 2962-2969
3
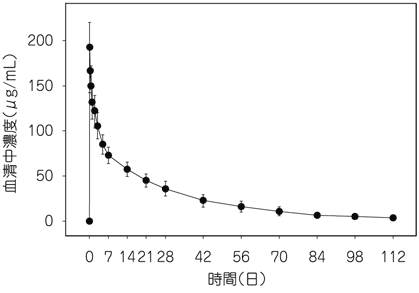
社内資料:健康成人におけるウステキヌマブ製剤の薬物動態比較試験(2017年3月30日承認、CTD2.7.1.2)
4
社内資料:クローン病に対する国際共同臨床試験の薬物濃度データの併合結果(2017年3月30日承認、CTD2.7.2.2)
5
社内資料:国際共同第Ⅲ相臨床試験成績(UCO3001 寛解導入試験)(2020年3月25日承認、CTD2.7.6.1)
6
Tabrizi MA, et al.:Drug Discov Today. 2006; 11: 81-88
7
社内資料:国際共同第Ⅲ相臨床試験成績(CRD3001)(2017年3月30日承認、CTD2.7.6.2)
8
社内資料:国際共同第Ⅲ相臨床試験成績(CRD3002)(2017年3月30日承認、CTD2.7.6.3)
9
Luo J, et al.:J Mol Biol. 2010; 402: 797-812
10
社内資料:ウステキヌマブのヒトIL-12及びIL-23中和作用機序(2017年3月30日承認、CTD2.6.2.1)
11
社内資料:ウステキヌマブのヒトIL-12及びIL-23中和作用の機能的効果(2017年3月30日承認、CTD2.6.2.1)