1
羽鳥泰彦 ほか:医薬品研究.1988;19(2):324-340.
2
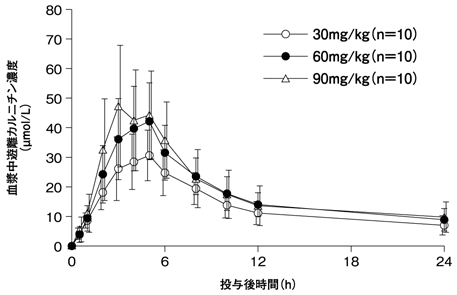
桐生千花:社内資料(単回経口投与試験).2011.(2012年12月25日承認、CTD2.7.6.1)
3
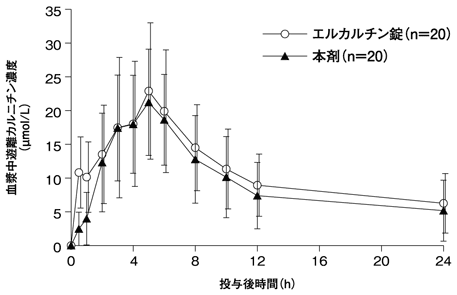
桐生千花:社内資料(レボカルニチン塩化物錠との薬物動態比較試験).2012.(2012年12月25日承認、CTD2.7.6.2)
4
崔 吉道:ビタミン.2010;84(12):604-609.
5
Levitan, M. D. et al.:Can J Neurol Sci.1987;14(1):50-54.
6
Pierre, G. et al.:J Inherit Metab Dis.2007;30(5):815.
7
Chalmers, R. A. et al.:Pediatr Res.1984;18(12):1325-1328.
8
Mayatepek, E. et al.:Pediatr Neurol.1991;7(2):137-140.
9
Giovenali, P. et al.:Kidney Int.1994;46(6):1616-1619.
10
Gidal, B. E. et al.:Pediatr Neurol.1997;16(4):301-305.
11
藤澤茂樹 ほか:日薬理誌.1989;93(5):305-313.