1
Saegusa, T. et al.:基礎と臨床 1992;26(3):969-981
2
Zheng, S. et al.:Br. J. Clin. Pharmacol. 2013;76(6):988-996
3
Coscia, L.A. et al.:Best Pract. Res. Clin. Obstet. Gynaecol. 2014;28(8):1174-1187
4
Jain, A. et al.:Transplantation. 1997;64(4):559-565
5
Fung, J.J. et al.:Transplant. Proc. 1990;22(1)Suppl.1:6-12
6
Curran, C.F. et al.:Transplantation. 1996;62(9):1376-1377
7
Mrvos, R. et al.:J. Toxicol. Clin. Toxicol. 1997;35(4):395-399
8
石橋道男 他:移植 1994;29(3):294-313
9
McDiarmid, S.V. et al.:Transplantation. 1993;55(6):1328-1332
10
Jain, A. et al.:Transplant. Proc. 1994;26(3):1609-1610
11
潰瘍性大腸炎患者・薬物動態(プログラフカプセル:2009年7月7日承認、申請資料概要 2.7.2.3)
12
高原史郎 他:今日の移植 1999;12(5):537-543
13
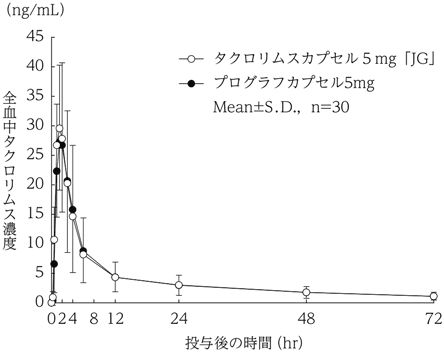
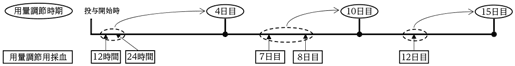
社内資料:生物学的同等性試験
14
Dressler, D. et al.:Clin. Pharmacol. Ther. 1996;59(2):151
15
潰瘍性大腸炎患者・薬物動態(プログラフカプセル:2009年7月7日承認、申請資料概要 2.7.2.3)
16
分布(プログラフカプセル:2001年1月12日承認、申請資料概要 ヘ.総括)
17
Iwasaki, K. et al.:薬物動態 1998;13(3):259-265
18
白神歳文 他:薬物動態 1999;14(4):277-285
19
Christians, U. et al.:Transplant. Proc. 1991;23(6):2741-2744
20
Venkataramanan, R. et al.:Transplant. Proc. 1991;23(6):2736-2740
21
薬物相互作用(プログラフカプセル:2001年1月12日承認、申請資料概要 ヘ.2)
22
Shiraga, T. et al.:Biochem. Pharmacol. 1994;47(4):727-735
23
深尾立 他:移植 1994;29(6):614-631
24
落合武徳 他:移植 1994;29(6):650-681
25
打田和治 他:移植 1994;29(6):632-649
26
高橋公太 他:移植 1994;29(6):682-697
27
大島伸一 他:移植 2001;36(1):20-38
28
上本伸二 他:臨床麻酔 1993;17(8):1087-1089
29
Inomata, Y. et al.:Transplantation. 1996;61(2):247-252
30
上本伸二 他:今日の移植 1999;12(4):445-451
31
上本伸二 他:今日の移植 2000;13(2):185-194
32
Reichart, B. et al.:J. Heart Lung Transplant. 1998;17(8):775-781
33
Taylor, D.O. et al.:J. Heart Lung Transplant. 1999;18(4):336-345
34
Mentzer, R.M.Jr. et al.:Transplantation. 1998;65(1):109-113
35
Pham, S.M. et al.:J. Thorac. Cardiovasc. Surg. 1996;111(4):764-772
36
Keenan, R.J. et al.:Ann. Thorac. Surg. 1995;60(3):580-585
37
Reichenspurner, H. et al.:Transplantation. 1999;68(1):67-71
38
Gruessner, R.W.G.:Clin. Transplant. 1997;11(4):299-312
39
Corry, R.J. et al.:Transplant. Proc. 1998;30(2):521
40
Atkison, P. et al.:Pediatr. Transplant. 1997;1(2):111-118
41
古川博之 他:今日の移植 1997;10(4):527-536
42
Kareem, M.A. et al.:Ann. Surg. 2009;250(4):567-581
43
平岡諦 他:今日の移植 1997;10(4):593-604
44
金丸昭久 他:今日の移植 1998;11(3):367-380
45
平岡諦 他:今日の移植 1998;11(5):649-676
46
平岡諦 他:今日の移植 2000;13(3):277-288
47
正岡徹 他:今日の移植 1993;6(3):313-320
48
潰瘍性大腸炎患者・第Ⅲ相比較試験(プログラフカプセル:2009年7月7日承認、申請資料概要 2.7.6.1)
49
潰瘍性大腸炎患者・第Ⅲ相非盲検試験(プログラフカプセル:2009年7月7日承認、申請資料概要 2.7.2.3、2.7.6.2)
50
鯉渕康全 他:今日の移植 2009;22(2):255-260
51
心移植に関する使用成績調査及び特定使用成績調査の概要(プログラフ注射液/カプセル/顆粒:2012年6月29日、再審査報告書)
52
肺移植に関する特定使用成績調査の概要(プログラフ注射液/カプセル/顆粒:2012年6月29日、再審査報告書)
53
膵移植に関する特定使用成績調査の概要(プログラフ注射液/カプセル/顆粒:2012年6月29日、再審査報告書)
54
藤澤弘佳 他:今日の移植 2009;22(2):245-253
55
奥原正國 他:日本農芸化学会誌 1996;70(1):1-8
56
Kino, T. et al.:J. Antibiot. 1987;40(9):1256-1265
57
Sakuma, S. et al.:Br. J. Pharmacol. 2000;130(7):1655-1663
58
Sakuma, S. et al.:Int. Immunopharmacol. 2001;1(4):749-757
59
Monden, M. et al.:Transplant. Proc. 1990;22(1)Suppl.1:66-71
60
Todo, S. et al.:Transplant. Proc. 1987;19(5)Suppl.6:64-67
61
稲垣和郎:広島大学医学雑誌 1988;36(1):81-89
62
岡村直孝:移植 1991;26(5):436-444
63
Mazzaferro, V. et al.:Transplant. Proc. 1990;22(1)Suppl.1:93-95
64
Loreal, O. et al.:Transplant. Proc. 1991;23(6):2825-2828
65
効力を裏付ける薬理試験(プログラフカプセル/注射液:2001年6月20日承認、申請資料概要 ホ.1)
66
Markus, P.M. et al.:Surgery. 1991;110(2):357-364
67
Todo, S. et al.:Surgery. 1989;106(2):444-451
68
Ochiai, T. et al.:Transplant. Proc. 1987;19(5)Suppl.6:53-56
69
Ochiai, T. et al.:Transplantation. 1987;44(6):734-738
70
和田洋巳 他:今日の移植 1992;5(4):387-391
71
剣持敬 他:日本外科学会雑誌 1992;93(6):626-631
72
IL10欠損マウス・薬理作用(プログラフカプセル:2009年7月7日承認、申請資料概要 2.6.2.2)