1
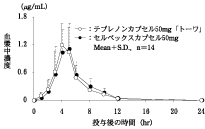
社内資料:生物学的同等性試験(カプセル50mg)
2
社内資料:生物学的同等性試験(細粒10%)
3
長谷川二郎ら:消化器科,1987;7(6):740-752
4
Murakami M.et al.:Arzneim.Forsch.,1981;31-1(5):799-804
5
Murakami M.et al.:Jpn.J.Pharmacol.,1982;32(5):921-924
6
村上 学ら:消化器科,1987;7(6):613-616
7
渡辺敦光ら:消化器科,1987;7(6):623-630
8
小林 隆ら:Ulcer Research,1994;21(1):66-69
9
佐藤泰男ら:Prog.Med.,1992;12(3):583-586
10
Terano A.et al.:Digestion,1986;33(4):206-210
11
中村正彦ら:Prog.Med.,1990;10(3):561-568
12
滝内比呂也ら:臨牀と研究,1993;70(11):3666-3670
13
内田秀一ら:医学のあゆみ,1987;143(7):605-606
14
西崎 朗ら:日本消化器病学会雑誌,1990;87(10):2352-2357
15
Oketani K.et al.:Jpn.J.Pharmacol.,1983;33(3):593-601
16
青野 充ら:日本消化器病学会雑誌,1984;81(S.):2389
17
Pappas T.N.et al.:Gastroenterology,1986;90(5):1578
18
Hirakawa T.et al.:Gastroenterology,1996;111(2):345-357
19
松田泰行ら:基礎と臨床,1989;23(17):6823-6827
20
中村紀夫ら:臨牀と研究,1984;61(5):1533-1541
21
Terano A.et al.:Digestion,1986;35(3):182-188
22
Arakawa T.et al.:Digestion,1988;39(2):111-117
23
村上 学ら:日本薬理学雑誌,1982;79(6):591-597
24
Kohli Y.et al.:京都府立医科大学雑誌,1991;100(6):637-644
25
竹村俊樹ら:臨床薬理,1989;20(1):97-98



 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379

