1
中道昇 他:薬理と治療. 1995;23(Suppl. 2):s241-s255
2
40mg 1日1回投与で効果不十分な高血圧症患者を対象とした臨床薬理試験(アダラートCR錠:2013年6月14日承認、審査報告書)
3
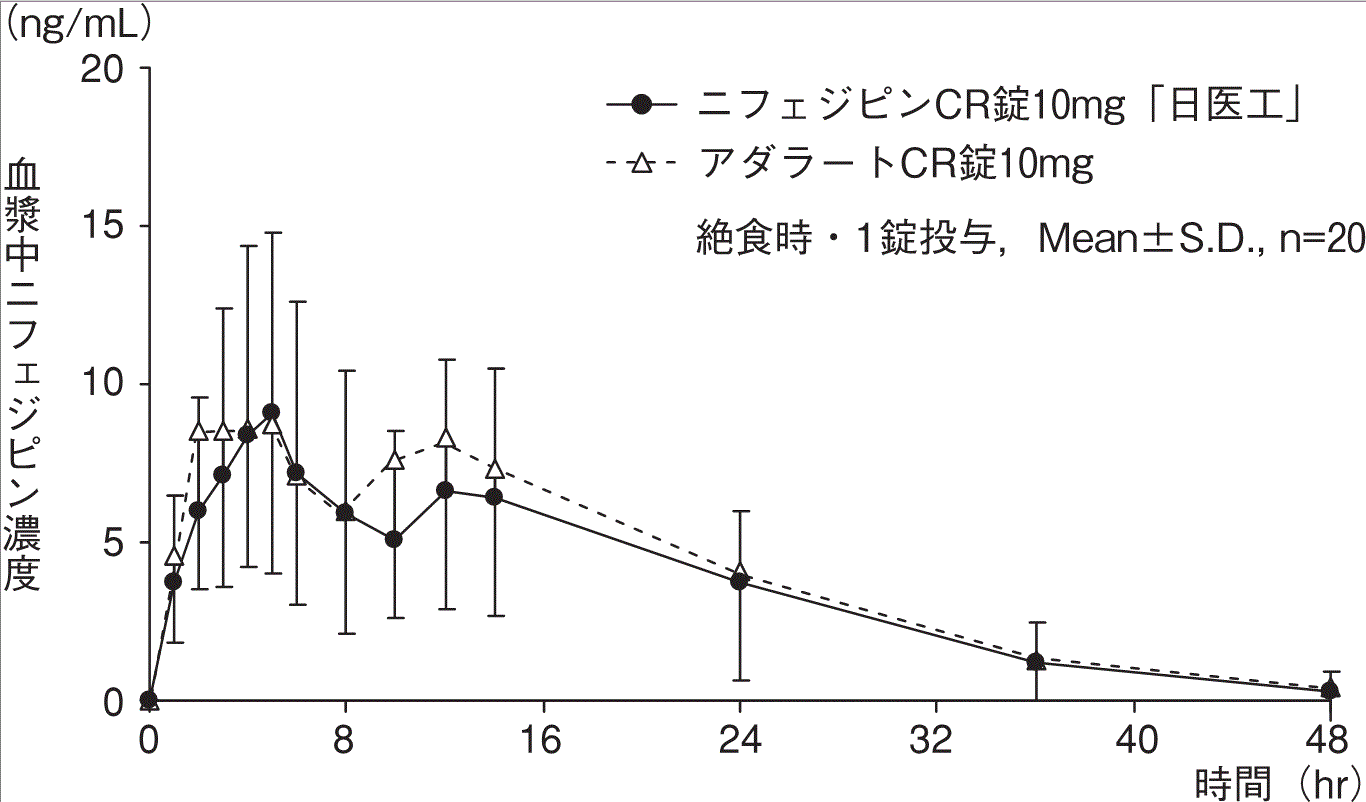
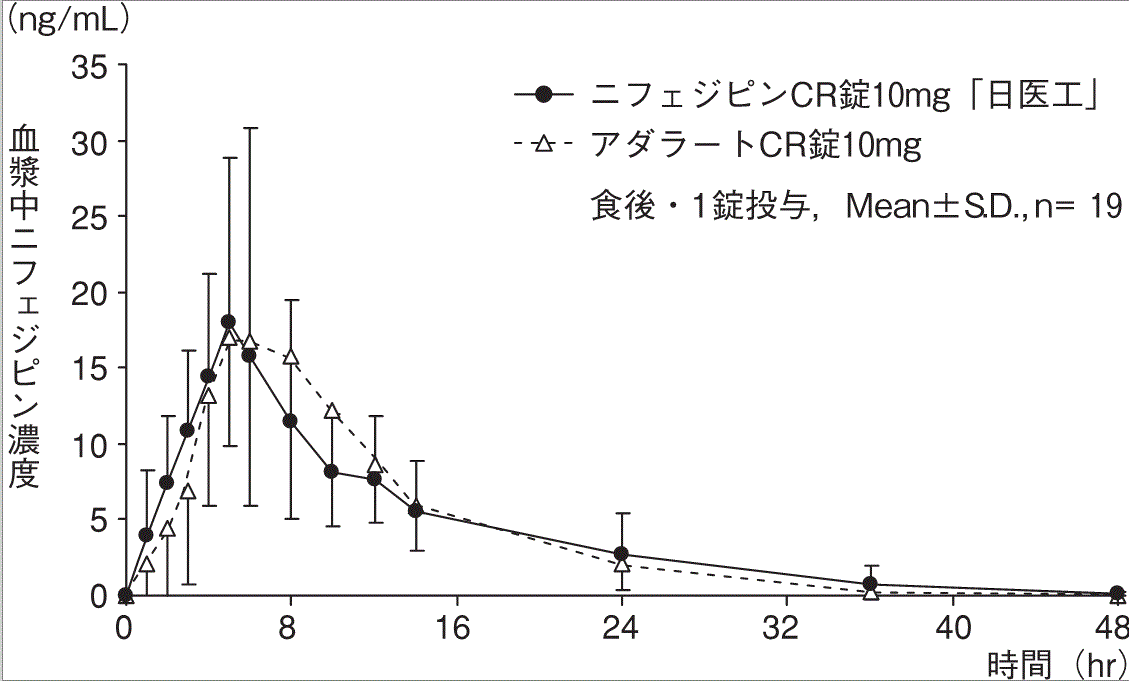
社内資料:生物学的同等性試験(錠10mg)
4
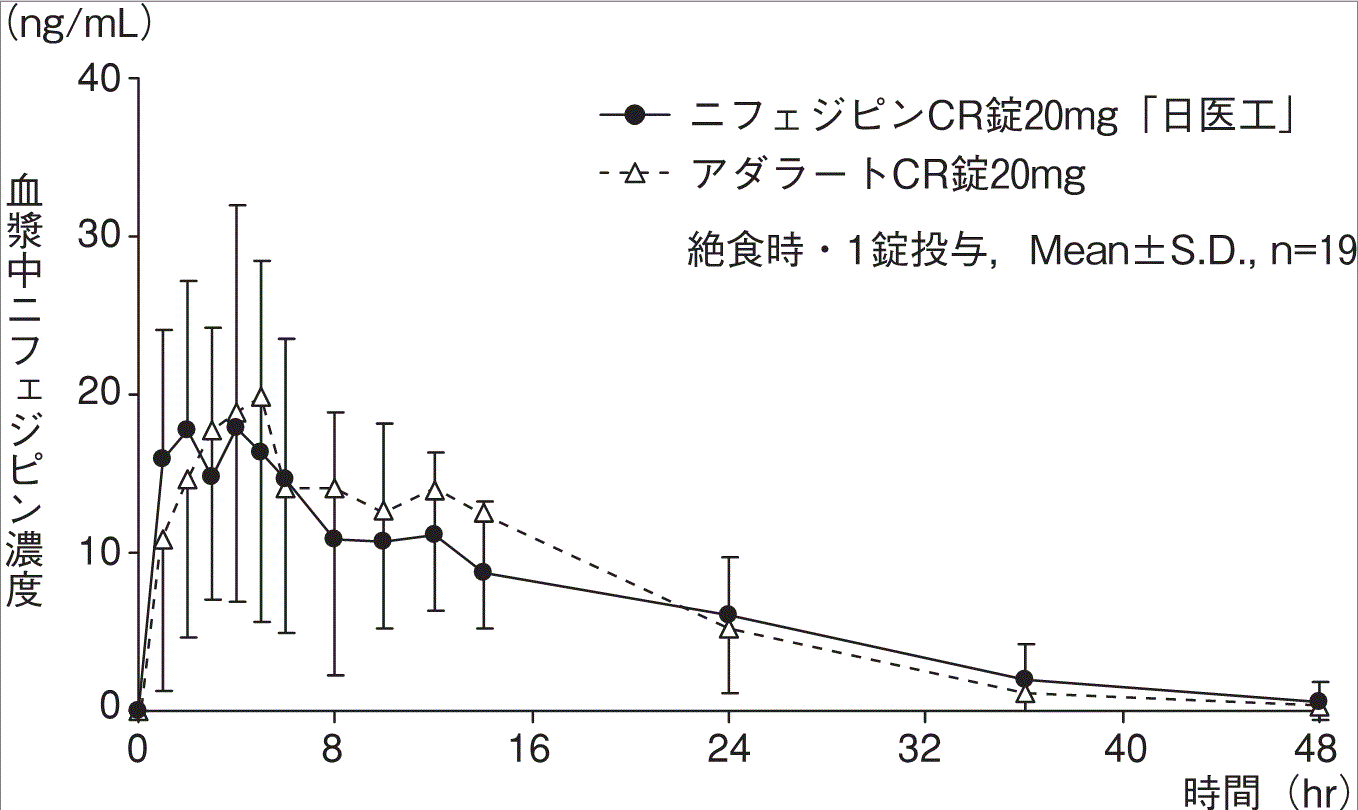
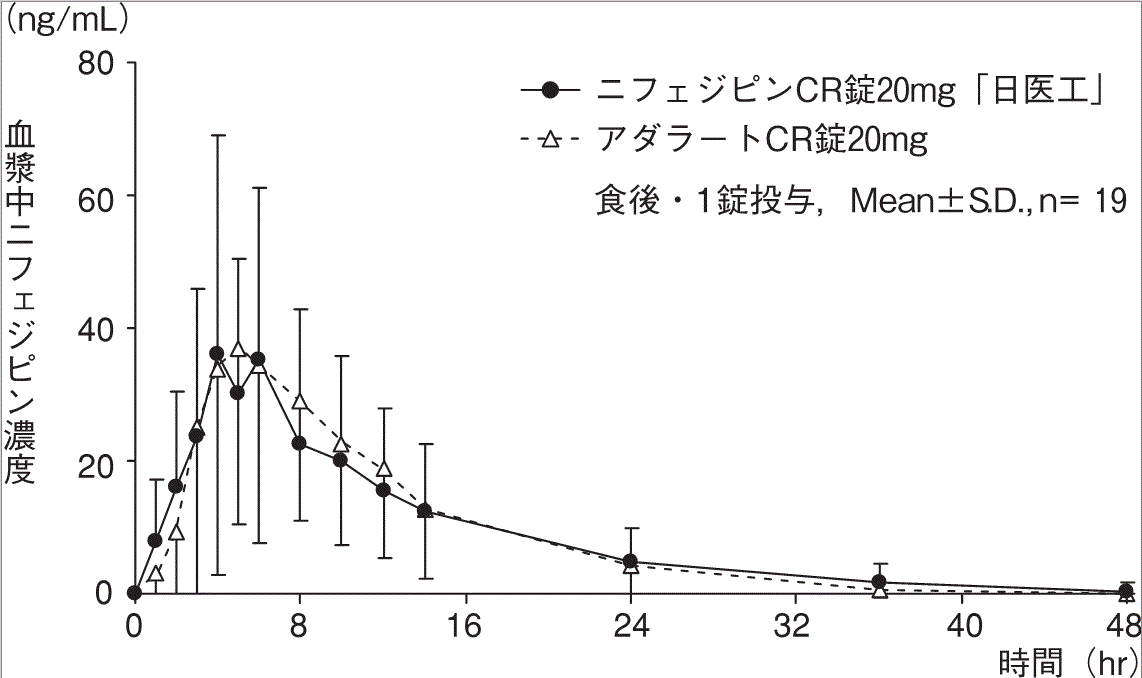
社内資料:生物学的同等性試験(錠20mg)
5
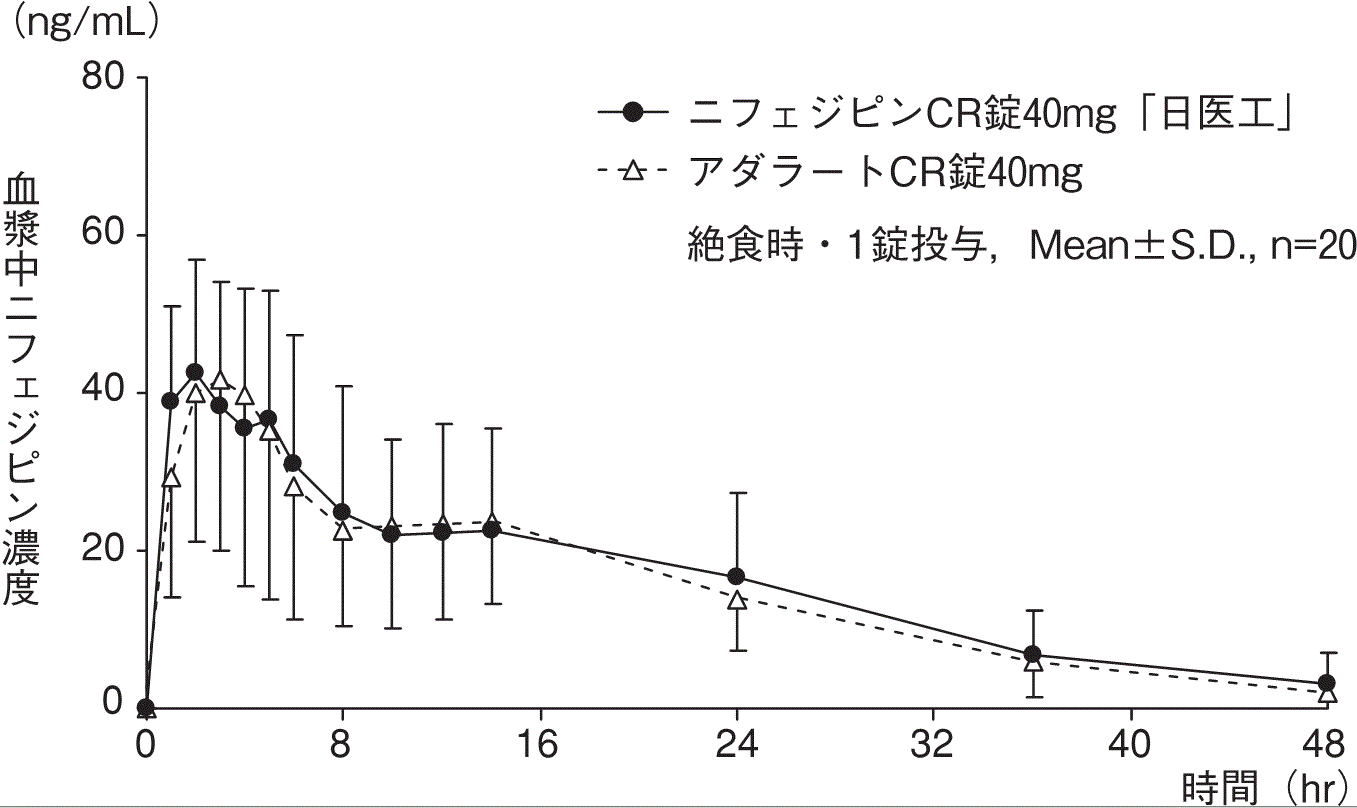
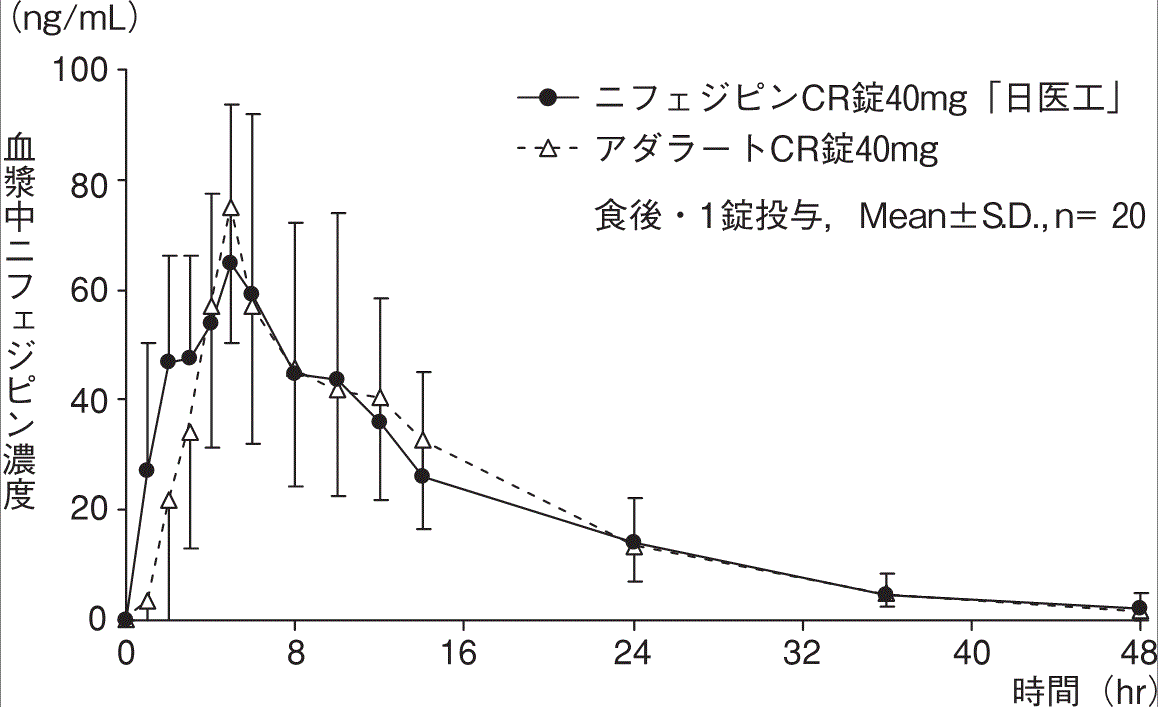
社内資料:生物学的同等性試験(錠40mg)
6
Duhm B., et al. :Arzneim.-Forsch./Drug Res. 1972;22:42-53
7
島本和明 他:薬理と治療. 1995;23(Suppl. 2):s407-s422
8
藤島正敏 他: 臨床と研究. 1995;72:174-190
9
Liu Y., et al.:Int. J. Clin. Pharmacol. Ther. 2017;55:246-255
10
40mg1日1回投与で効果不十分な高血圧症患者を対象とした二重盲検比較試験(アダラートCR錠: 2013年6月14日承認、審査報告書)
11
Shimamoto K., et al.:Hypertens. Res. 2014;37:69-75
12
長期併用投与試験(アダラートCR錠:2013年6月14日承認、審査報告書)
13
Shimamoto K., et al.:Hypertens. Res. 2015;38:695-700
14
加藤和三 他:薬理と治療. 1997;23(Suppl.2):s449-s463
15
加藤和三 他:薬理と治療. 1997;23(Suppl.2):s465-s477
16
加藤和三 他:薬理と治療. 1997;25:1943-1973
17
加藤和三 他:薬理と治療. 1997;25:1975-2005
18
Fleckenstein A., et al . : Arzneim.-Forsch./Drug Res. 1972; 22: 22-32
19
Hayase S., et al.:Jpn. Circulation J. 1971;35:903-914
20
石井當男 他: 薬理と治療. 1997;25:1829-1838
21
橋本虎六 他:心臓. 1971;3:1294-1304
22
Kanazawa T., et al.:Arzneim.-Forsch./Drug Res. 1974;24:1267-1274
23
Taira N., et al.:In Proceedings 5th International Adalat® Symposium. 1983;17-25
24
Nayler W. G.,et al.:Am. J. Cardiol. 1980;46:242-248
25
石井當男 他: 薬理と治療. 1997;25:1817-1828
26
Vater W.: 2nd International Adalat® Symposium. Springer. 1975;77-81
27
Pumphrey C. W., et al.:Am. J. Cardiol. 1983;51:591-595
28
Taira N., et al.:2nd International Adalat® Symposium. Springer. 1975;40-48







 077
077