1
Sakai, M. et al.: Mol. Hum. Reprod. 2001; 7(6): 595-602
2
Takahashi, Y. et al.: Am. J. Physiol. Regul. Integr. Comp. Physiol. 2000; 278(6): R1496-R1505
3
Knoppert, D.C. et al.: Pharmacotherapy. 2003; 23(1): 97-100
4
Hale, T.W. et al.: J. Hum. Lact. 2004; 20(4): 397-403
5
藤田雅己 他: Prog. Med. 2006; 26(Suppl. 3): 2960-2969
6
松岡 治 他: Prog. Med. 2006; 26(Suppl. 3): 2970-2976
7
松岡 治 他: Prog. Med. 2006; 26(Suppl. 3): 2977-2987
8
関節リウマチ及び変形性膝関節症患者・薬物動態(セレコックス錠:2007年1月26日承認、申請資料概要2.7.2.3.8)
9
キョーリンリメディオ株式会社社内資料:
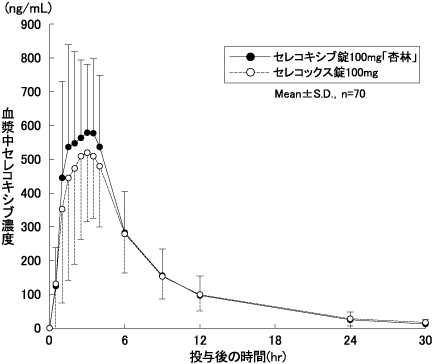
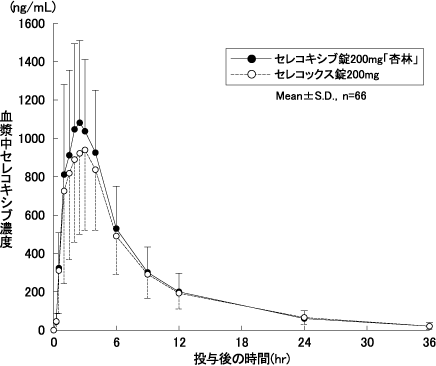
セレコキシブ錠100mg「杏林」・200mg「杏林」の生物学的同等性試験に関する資料
セレコキシブ錠100mg「杏林」・200mg「杏林」の生物学的同等性試験に関する資料
10
Paulson, S.K. et al.: Biopharm. Drug Dispos. 1999; 20(6): 293-299
11
In vitro血漿蛋白結合率(セレコックス錠:2007年1月26日承認、申請資料概要2.7.2.3.8)
12
Tang, C. et al.: J. Pharmacol. Exp. Ther. 2000; 293(2): 453-459
13
海外健康成人・代謝及び薬物相互作用(セレコックス錠:2007年1月26日承認、申請資料概要2.7.2.2.3.1.1)
14
Nasu, K. et al.: Pharmacogenetics. 1997; 7(5): 405-409
15
健康成人・代謝(セレコックス錠:2007年1月26日承認、申請資料概要2.7.2.3.2.6)
16
Kirchheiner, J. et al.: Pharmacogenetics. 2003; 13(8): 473-480
17
Lundblad, M.S. et al.: Clin. Pharmacol. Ther. 2006; 79(3): 287-288
18
Paulson, S.K. et al.: Drug Metab. Dispos. 2000; 28(3): 308-314
19
海外腎障害患者・薬物動態(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.17)
20
海外腎障害患者・薬物動態(セレコックス錠:2007年1月26日承認、審査報告書)
21
肝障害患者・薬物動態(セレコックス錠:2007年1月26日承認、申請資料概要2.7.2.2.2.2)
22
肝障害患者・薬物動態(セレコックス錠:2007年1月26日承認、審査報告書)
23
海外健康成人・薬物動態(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.15)
24
海外健康成人・薬物相互作用(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.20)
25
海外健康成人・薬物相互作用(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.27)
26
Karim, A. et al.: J. Clin. Pharmacol. 2000; 40(6): 655-663
27
海外健康成人・薬物相互作用(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.30)
28
海外健康成人・薬物相互作用(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.31)
29
海外健康成人・薬物相互作用(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.28)
30
海外健康成人・薬物相互作用(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.25)
31
安倍 達 他: Prog. Med. 2006; 26(Suppl. 3): 2788-2819
32
安倍 達 他: Prog. Med. 2006; 26(Suppl. 3): 2820-2845
33
青木虎吉 他: Prog. Med. 2006; 26(Suppl. 3): 2869-2910
34
菅原幸子: Prog. Med. 2006; 26(Suppl. 3): 2911-2931
35
菊地臣一 他: Prog. Med. 2009; 29(Suppl. 2): 2853-2872
36
高岸憲二 他: Prog. Med. 2009; 29(Suppl. 2): 2893-2917
37
高岸憲二 他: Prog. Med. 2009; 29(Suppl. 2): 2918-2940
38
荻野利彦 他: Prog. Med. 2009; 29(Suppl. 2): 2941-2963
39
手術後疼痛試験(セレコックス錠:2011年12月22日承認、審査報告書)
40
太田博嘉 他: Prog. Med. 2010; 30(12): 3117-3130
41
代田達夫 他: 歯科薬物療法 2001; 20(3): 154-172
42
抜歯後疼痛追加投与試験(セレコックス錠:2011年12月22日承認、審査報告書)
43
RAに対する第Ⅲ相試験(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.34)
44
OAに対する第Ⅲ相試験(セレコックス錠:2007年1月26日承認、申請資料概要2.7.6.36)
45
心血管系に関する有害事象(セレコックス錠:2007年1月26日承認、申請資料概要2.7.4.2.1.5.5)
46
心血管系有害事象について(セレコックス錠:2009年6月17日承認、審査報告書)
47
外傷後疼痛試験(セレコックス錠:2011年12月22日承認、審査報告書)
48
製造販売後臨床試験(セレコックス錠:2020年3月18日、再審査報告書)
49
Bertagnolli, M.M. et al.: N. Engl. J. Med. 2006; 355(9): 873-884
50
Arber, N. et al.: N. Engl. J. Med. 2006; 355(9): 885-895
51
Solomon, S.D. et al.: Circulation. 2006; 114(10): 1028-1035
52
Penning, T.D. et al.:J. Med. Chem. 1997;40(9):1347-1365
53
Yoshino, T. et al.: Arzneimittel-Forschung/Drug Res. 2005; 55(7): 394-402
54
作用機序(セレコックス錠:2007年1月26日承認、申請資料概要2.6.2.6.1)
55
Noguchi, M. et al.: Eur. J. Pharmacol. 2005; 513(3): 229-235
56
抗炎症作用(セレコックス錠:2007年1月26日承認、申請資料概要2.6.2.2.2.2)
57
鎮痛作用(セレコックス錠:2007年1月26日承認、申請資料概要2.6.2.2.3.2)
58
消化管粘膜に対する作用(セレコックス錠:2007年1月26日承認、申請資料概要2.6.2.2.5)
59
厚生省薬務局: 医薬品副作用情報No.98, 1989
60
Yoshino, T. et al.: Eur. J. Pharmacol. 2005; 507(1-3): 69-76