1
Hewett C et al:Arzneimittelforschung. 1986: 36:592-596
2
社内資料: 河野恒文ほか:生物学的利用率比較試験
3
吉田 剛ほか:薬理と治療 1985:13:3333
4
Bechtel W.D. et al.:Br J Clin Pharmacol. 1983:16 (Suppl. 2):261s
5
Senda C et al:Xenobiotica. 1997: 27(9):913
6
Bechtel W D:Br J Clin Pharmacol. 1983: 16(Suppl. 2):279S
7
筒井末春ほか:医学のあゆみ. 1984: 131:412
8
村田忠良ほか:臨床精神医学. 1985: 14:121
9
工藤義雄ほか:医学のあゆみ. 1985: 134:494
10
稲永和豊ほか:薬理と治療. 1984: 12:5111
11
山村秀夫ほか:臨牀と研究. 1985: 62:1924
12
吉武潤一ほか:Therapeutic Research. 1984: 1:829
13
Ishiko J.et al:Neuropharmacology. 1983: 22:221
14
Kuhn F J et al:Br J Clin Pharmacol. 1983: 16(Suppl. 2):253S
15
Kimishima K et al:Jpn J Pharmacol. 1984: 36:461-475
16
Ueki S et al:Jpn J Pharmacol. 1984 : 35:287-299
17
花岡一雄ほか:臨床薬理. 1983: 14:365-377
18
大川敏彦ほか:臨床精神医学. 1984: 13:749
19
Nicholson A N et al:Br J Clin Pharmacol.1980: 10:75
20
金 英道ほか:臨床精神医学. 1991: 20:55




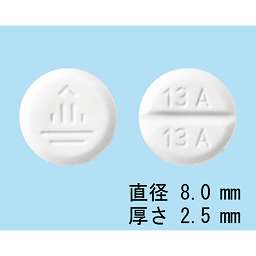

 13A
13A