作成又は改訂年月
日本標準商品分類番号
薬効分類名
承認等
販売名
クロルマジノン酢酸エステル錠25mg「日医工」
販売名コード
承認・許可番号
承認番号 22500AMX00443000
欧文商標名 Chlormadinone Acetate
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
室温保存
使用期限
外箱等に表示の使用期限内に使用すること
規制区分
処方箋医薬品
(注意−医師等の処方箋により使用すること)
組成
クロルマジノン酢酸エステル錠25mg「日医工」
製剤の性状
表面 裏面 側面 質量 直径 厚さ 本体 包装 200 8.0 3.0
一般的名称
禁忌
重篤な肝障害・肝疾患のある患者[代謝能が低下しており肝臓への負担が増加するため,症状が増悪することがある。]
効能又は効果
・前立腺肥大症
・前立腺癌
ただし,転移のある前立腺癌症例に対しては,他療法による治療の困難な場合に使用する。
用法及び用量
・前立腺肥大症
クロルマジノン酢酸エステルとして,1回25mg(1錠)を1日2回食後に経口投与する。
・前立腺癌
クロルマジノン酢酸エステルとして,1回50mg(2錠)を1日2回食後に経口投与する。
使用上の注意
慎重投与
心疾患,腎疾患又はその既往歴のある患者[ナトリウムや体液の貯留により,これらの症状が増悪することがある。]
糖尿病患者[耐糖能の低下があらわれることがある。]
重要な基本的注意
劇症肝炎等の重篤な肝機能障害による死亡例が報告されているので,投与開始後3ヵ月までは少なくとも1ヵ月に1回 ,それ以降も定期的に肝機能検査を行うこと。
前立腺肥大症に使用する場合は次の点に留意すること。
本剤による前立腺肥大症に対する治療は,根治療法ではないことに留意し,本剤投与により期待する効果が得られない場合には,手術療法等他の適切な処置を考慮すること。
投与期間は16週間を基準とし,期待する効果が得られない場合には,以後漫然と投与を継続しないこと。
ポテンツ低下等があらわれた場合,治療上の有益性を考慮の上,必要に応じ休薬又は他の療法への変更を行うこと。
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用
うっ血性心不全 (頻度不明)
うっ血性心不全があらわれることがあるので,このような場合には投与を中止するなど適切な処置を行うこと。
血栓症 (頻度不明)
血栓症(脳,心,肺,四肢等)があらわれることがあるので,異常が認められた場合には投与を中止し適切な処置を行うこと。
劇症肝炎,肝機能障害,黄疸 (頻度不明)
本剤投与1〜2ヵ月後に劇症肝炎,肝機能障害,黄疸があらわれ,死亡に至った症例が報告されているので,投与開始後3ヵ月間は少なくとも1ヵ月に1回,それ以降も定期的に肝機能検査を行い,悪心・嘔吐,食欲不振,全身倦怠感等の異常が認められた場合には直ちに投与を中止し適切な処置を行うこと。
糖尿病,糖尿病の悪化,高血糖 (頻度不明)
糖尿病,糖尿病の悪化あるいは高血糖があらわれることがあり,昏睡,ケトアシドーシスを伴う重篤な症例も報告されているので,血糖値や尿糖に注意するなど観察を十分に行い,異常が認められた場合には投与を中止するなど適切な処置を行うこと。
その他の副作用
頻度不明 生殖器 インポテンス,性欲低下等 過敏症 注1) 発疹,そう痒等 肝臓 注2) 肝機能異常等 腎臓 注3) BUN上昇,クレアチニン上昇等 電解質代謝 注4) 浮腫,体重増加等 循環器 注3) 動悸,心悸亢進,胸内苦悶,息切れ等 血液 貧血 消化器 胃部不快感,悪心,便秘,下痢,食欲不振,口渇,嘔吐,腹痛等 精神神経系 頭痛,眠気等 泌尿器 頻尿,尿道不快感,下腹部痛等 脂質代謝 中性脂肪上昇 内分泌 女性型乳房,血中FSH,LH,テストステロン値の低下,プロラクチン値の上昇 皮膚 脱毛 その他 倦怠感,微熱,発汗,肥満
注1:発現した場合には投与を中止すること。
注2:肝機能検査値に注意するなど観察を十分に行い,異常が認められた場合には投与を中止するなど適切な処置を行うこと。
注3:発現した場合には投与を中止するなど適切な処置を行うこと。
注4:観察を十分に行い,発現した場合には投与を中止するなど適切な処置を行うこと。
高齢者への投与
高齢者への投与の際には用量並びに投与間隔に留意するなど慎重に投与すること。[一般に高齢者では生理機能が低下していることが多いため,血中濃度が持続するおそれがある。]
適用上の注意
薬剤交付時 :
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。(PTPシートの誤飲により,硬い鋭角部が食道粘膜へ刺入し,更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告されている。)
その他の注意
ラット,ウサギ及びイヌにおいて精子形成異常が認められるという報告がある。
*海外の疫学調査において,クロルマジノン酢酸エステルの6カ月間の累積投与量が360mg超の女性では,360mg以下の女性と比較して髄膜腫の発生リスクが高く(ハザード比4.4(95%信頼区間:3.4-5.8)),累積投与量の増加に伴い発生リスクが高くなるとの報告がある。1)
薬物動態
生物学的同等性試験
クロルマジノン酢酸エステル錠25mg「日医工」及び標準製剤を,クロスオーバー法によりそれぞれ1錠(クロルマジノン酢酸エステルとして25mg)健康成人男子に絶食単回経口投与して血漿中クロルマジノン酢酸エステル濃度を測定し,得られた薬物動態パラメータ(AUC,Cmax)について統計解析を行った結果,両剤の生物学的同等性が確認された。
2) 血漿中濃度並びにAUC,Cmax等のパラメータは,被験者の選択,体液の採取回数・時間等の試験条件によって異なる可能性がある。
溶出挙動
クロルマジノン酢酸エステル錠25mg「日医工」は,日本薬局方外医薬品規格第3部に定められたクロルマジノン酢酸エステル錠の溶出規格に適合していることが確認されている。3)
有効成分に関する理化学的知見
一般名
クロルマジノン酢酸エステル(Chlormadinone Acetate)
化学名
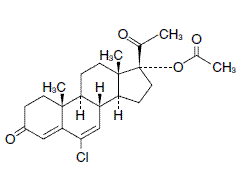
6-Chloro-3,20-dioxopregna-4,6-dien-17-yl acetate
構造式
分子式
C23 H29 ClO4
分子量
404.93
性状
白色〜淡黄色の結晶又は結晶性の粉末で,においはない。
融点
211〜215℃
取扱い上の注意
安定性試験
本品につき加速試験(40℃,相対湿度75%,6ヵ月)を行った結果,クロルマジノン酢酸エステル錠25mg「日医工」は通常の市場流通下において3年間安定であることが推測された。4)
包装
クロルマジノン酢酸エステル錠25mg「日医工」
主要文献及び文献請求先
主要文献
1
Pierre Nguyen, et al. : Utilisation prolongee de l’acetate de chlormadinone et risque de meningiome intracranien : une etude de cohorte a partir des donnees du SNDS(Avril 2021 Rapport final)
2
日医工株式会社 社内資料:生物学的同等性試験
3
日医工株式会社 社内資料:溶出試験
4
日医工株式会社 社内資料:安定性試験
文献請求先
主要文献欄に記載の文献・社内資料は下記にご請求下さい。
〒930‐8583 富山市総曲輪1丁目6番21
フリーダイアル(0120)517-215
Fax(076)442-8948
製造販売業者等の氏名又は名称及び住所
製造販売元
日医工株式会社
富山市総曲輪1丁目6番21



 967
967 967
967