1
社内資料:生物学的同等性試験(錠20mg)
2
社内資料:生物学的同等性試験(錠40mg)
3
Regårdh,C.G.,et al.:J.Pharmacokinet.Biopharm.,1974;2(4):347-364
4
Bertz,R.J.,et al.:Clin.Pharmacokinet.,1997;32(3):210-258
高血圧・狭心症・不整脈治療剤
1錠 7.5円
有効成分 | 1錠中 |
|---|---|
有効成分 | 日局 メトプロロール酒石酸塩 20mg |
添加剤 | 乳糖水和物、結晶セルロース、ヒドロキシプロピルセルロース、カルメロースカルシウム、軽質無水ケイ酸、ステアリン酸マグネシウム、ヒプロメロース、マクロゴール6000、タルク、酸化チタン |
有効成分 | 1錠中 |
|---|---|
有効成分 | 日局 メトプロロール酒石酸塩 40mg |
添加剤 | 乳糖水和物、結晶セルロース、ヒドロキシプロピルセルロース、カルメロースカルシウム、軽質無水ケイ酸、ステアリン酸マグネシウム、ヒプロメロース、マクロゴール6000、タルク、酸化チタン |
| 剤形 | フィルムコーティング錠 |
|---|---|
| 色調 | 白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 6.1mm 大きさ(厚さ) 3.0mm |
| 質量 | 93mg |
| 識別コード | Tw/SP20(表/裏) Tw.SP20 |
| 剤形 | フィルムコーティング錠 |
|---|---|
| 色調 | 白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 8.1mm 大きさ(厚さ) 3.5mm |
| 質量 | 186mg |
| 識別コード | Tw/SP40(表/裏) Tw.SP40 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
交感神経系に対し抑制的に作用する他の薬剤 レセルピン β遮断剤(チモロール等の点眼剤を含む)等 | 過剰の交感神経抑制を来し、徐脈、血圧低下等があらわれるおそれがあるので、用量に注意すること。 | 共に交感神経抑制作用を有するため。 |
血糖降下剤 インスリン グリベンクラミド等 | 血糖降下作用を増強することがある。また、低血糖症状(頻脈等)をマスクすることがあるので、血糖値に注意すること。 | 本剤のβ遮断作用により、低血糖からの回復が遅れることがあり、また、低血糖に伴う交感神経系の症状をマスクする。 |
カルシウム拮抗剤 ベラパミル ジルチアゼム等 | 相互に作用が増強され、過度の降圧又は心機能抑制があらわれることがあるので、用量に注意すること。 | 共に陰性変時・変力作用、降圧作用を有するため。 |
クロニジン | クロニジンの投与中止後のリバウンド現象(血圧上昇)を増強するおそれがある。クロニジンの投与を中止する場合には、本剤を数日前に中止し、経過を観察してから行うこと。 | クロニジンの投与中止により血中ノルアドレナリンが増加した場合、本剤のβ遮断作用によりα刺激作用(血管収縮作用)が優位となるため。 |
ClassⅠ抗不整脈剤 ジソピラミド プロカインアミド アジマリン等 ClassⅢ抗不整脈剤 アミオダロン等 | 過度の心機能抑制があらわれることがあるので、用量に注意すること。 | 共に心機能抑制作用を有するため。 |
抗不整脈剤 キニジン プロパフェノン アミオダロン等 | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | これらの薬剤の肝代謝酵素阻害作用により本剤の代謝が抑制されると考えられる。 |
ミラベグロン | 本剤のAUCが3.29倍上昇したとの報告があり、本剤の作用が増強するおそれがある。 | ミラベグロンのCYP2D6阻害作用により、本剤の血中濃度が上昇する可能性がある。 |
麻酔剤 セボフルラン等 | 過剰の交感神経の抑制を起こす可能性があるので心機能等に注意すること。 | 共に交感神経抑制作用を有するため。 |
ジギタリス製剤 | 房室伝導時間が延長し、徐脈、房室ブロック等があらわれるおそれがあるので、心機能に注意すること。 | 共に刺激伝導速度の抑制作用を有するため。 |
非ステロイド性抗炎症剤 インドメタシン等 | 本剤の降圧作用が減弱することがあるので、用量に注意すること。 | 非ステロイド性抗炎症剤は、血管拡張作用を有する腎プロスタグランジンの合成・遊離を阻害し血圧を上昇させることがある。 |
降圧作用を有する他の薬剤 ニトログリセリン タダラフィル等 | 過度の降圧を来すおそれがあるので、用量に注意すること。 | 共に降圧作用を有するため。 |
シメチジン | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | これらの薬剤の肝代謝酵素阻害作用により本剤の代謝が抑制されると考えられる。 |
選択的セロトニン再取込み阻害剤 パロキセチン等 | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | これらの薬剤の肝代謝酵素阻害作用により本剤の代謝が抑制されると考えられる。 |
抗ヒスタミン剤 ジフェンヒドラミン等 | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | これらの薬剤の肝代謝酵素阻害作用により本剤の代謝が抑制されると考えられる。 |
ヒドララジン | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | ヒドララジンは肝血流量を増加させ、本剤の初回通過効果を減少させると考えられる。 |
リファンピシン | 本剤の血中濃度が低下し、作用が減弱することがあるので、用量に注意すること。 | リファンピシンの肝代謝酵素誘導作用により本剤の代謝が促進されると考えられる。 |
リドカイン | リドカインの血中濃度を上昇させることがあるので、用量に注意すること。 | 本剤による肝血流量の減少及び肝代謝酵素活性阻害によりリドカインの代謝を遅延させると考えられる。 |
フィンゴリモド | フィンゴリモドの投与開始時に本剤を併用すると重度の徐脈や心ブロックが認められることがある。 | 共に徐脈や心ブロックを引き起こすおそれがある。 |
0.1~5%未満 | 0.1%未満 | 頻度不明 | |
|---|---|---|---|
眼 | 視覚障害(霧視等) | 涙液分泌減少、結膜炎 | |
過敏症 | 発疹(乾癬型等) | そう痒 | 光線過敏症 |
血液 | 血小板減少 | ||
循環器 | 動悸 | 末梢循環障害(四肢の冷え・しびれ等) | 心室性期外収縮、起立性低血圧注)、低血圧 |
呼吸器 | 息切れ | 鼻閉、鼻炎、気管支痙攣 | |
精神神経系 | めまい・ふらつき、頭痛、不眠、眠気、抑うつ | 悪夢、不安 | 幻覚、感覚異常、注意力障害、神経過敏、健忘、錯乱 |
消化器 | 腹痛、食欲不振、便秘、下痢、胸やけ、口渇 | 悪心・嘔吐、腹部膨満感 | |
肝臓 | AST上昇、ALT上昇 | ||
その他 | 胸部圧迫感、浮腫、疲労感、耳鳴 | 性欲減退 | 倦怠感、トリグリセライドの上昇、発汗、CK(CPK)の上昇、筋痙直、勃起障害、味覚異常、脱毛、難聴、関節痛、体重増加、乾癬悪化 |
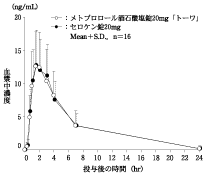
判定パラメータ | 参考パラメータ | |||
AUC0-24 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
メトプロロール酒石酸塩錠 20mg「トーワ」 | 86.5±43.2 | 13.5±5.8 | 1.7±0.6 | 3.0±1.2 |
セロケン錠20mg | 85.7±35.4 | 14.5±4.9 | 1.8±0.7 | 3.2±1.4 |
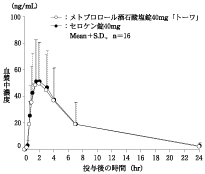
判定パラメータ | 参考パラメータ | |||
AUC0-24 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
メトプロロール酒石酸塩錠 40mg「トーワ」 | 408.9±295.4 | 54.9±32.5 | 1.9±0.8 | 5.0±0.5 |
セロケン錠40mg | 421.1±307.3 | 56.3±30.4 | 1.7±0.6 | 5.0±0.6 |
 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379