添付文書番号
1329702R3217_1_02
企業コード
480115
作成又は改訂年月
日本標準商品分類番号
871329
薬効分類名
粘膜付着型鼻過敏症治療剤
承認等
販売名
ベクロメタゾン点鼻液50μg「DSP」
販売名コード
販売名英字表記
BECLOMETASONE Nasal Solution 50μg “DSP”
承認番号等
販売開始年月
貯法、有効期間
規制区分
一般的名称
ベクロメタゾンプロピオン酸エステル点鼻液
禁忌(次の患者には投与しないこと)
有効な抗菌剤の存在しない感染症・全身の真菌症の患者[症状を増悪するおそれがある。]
本剤の成分に対して過敏症の既往歴のある患者
組成・性状
組成
ベクロメタゾン点鼻液50μg「DSP」
有効成分 | 1瓶中の内容物重量約8.5g
1g中ベクロメタゾンプロピオン酸エステル 1mg |
|---|
添加剤 | カルボキシビニルポリマー、L-アルギニン、ベンザルコニウム塩化物、エデト酸ナトリウム水和物、ポリソルベート80、濃グリセリン |
|---|
| 1回の噴霧主薬量 | 0.05mg |
|---|
| 1容器の噴霧回数 | 約80回 |
|---|
製剤の性状
ベクロメタゾン点鼻液50μg「DSP」
| 剤形 | 定量噴霧式の気密なポリエチレン瓶に充てんした懸濁剤
内容物は白色懸濁性の粘稠な液で、ほとんど無臭である。 |
|---|
効能又は効果
用法及び用量
擤鼻後十分の呼吸を行わせ、吸気の際に本剤を1側鼻孔より1回噴霧し、この際他側の鼻孔は指で閉鎖する。
次いで他側鼻孔に同様の操作を行う。
成人は、通常1回上記1操作の吸入(ベクロメタゾンプロピオン酸エステルとして100μg)を、1日4回鼻腔内に噴霧吸入する。小児は、通常1回上記1操作の吸入(ベクロメタゾンプロピオン酸エステルとして100μg)を、1日2回鼻腔内に噴霧吸入する。なお、年齢・体重・症状により適宜増減するが、1日の最大投与量は、成人では16吸入、小児では8吸入を限度とする。また、症状の緩解がみられた場合は、その後の経過を観察しながら減量する。
重要な基本的注意
本剤の投与期間中に鼻症状の悪化がみられた場合には、抗ヒスタミン剤あるいは、全身性ステロイド剤を短期間併用し、症状の軽減にあわせて併用薬剤を徐々に減量すること。
本剤には持続効果が認められるので、特に通年性の患者において長期に使用する場合は、症状の改善状態が持続するようであれば、本剤の減量又は休薬につとめること。
全身性ステロイド剤の減量は本剤の吸入開始後症状の安定をみて徐々に行う。減量にあたっては一般のステロイド剤の減量法に準ずる。
全身性ステロイド剤の減量並びに離脱に伴って、気管支喘息、ときに湿疹、蕁麻疹、眩暈、動悸、倦怠感、顔のほてり、結膜炎等の症状が発現・増悪することがある。このような症状があらわれた場合には適切な処置を行うこと。
特定の背景を有する患者に関する注意
合併症・既往歴等のある患者
結核性疾患又は感染症(有効な抗菌剤の存在しない感染症、全身の真菌症を除く)の患者
症状を増悪するおそれがある。
反復性鼻出血の患者
出血を増強するおそれがある。
高血圧の患者
血圧上昇を起こすおそれがある。
糖尿病の患者
症状を増悪するおそれがある。
重症な肥厚性鼻炎や鼻茸の患者
本剤の鼻腔内での作用を確実にするため、これらの症状がある程度減少するよう他の療法を併用するとよい。
長期又は大量の全身性ステロイド療法を受けている患者
全身性ステロイド剤の減量中並びに離脱後も副腎皮質機能検査を行い、外傷、手術、重症感染症等の侵襲には十分に注意を払うこと。また、必要があれば一時的に全身性ステロイド剤の増量を行うこと。これらの患者では副腎皮質機能不全となっていることが考えられる。
喘息発作重積状態又は喘息の急激な悪化状態の患者
原則として本剤は使用しないこと。
妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。動物実験で催奇形作用が報告されている。
授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
小児等
本剤はステロイド剤であることを考慮し、非ステロイド系薬剤によって諸症状の緩解が得られない場合に使用すること。
使用に当たっては、使用法を正しく指導し、経過の観察を十分行うこと。長期、大量使用により発育障害をきたすおそれがある。
低出生体重児、新生児、乳児又は5才以下の幼児を対象とした臨床試験は実施していない。
高齢者
患者の状態を観察しながら投与期間に注意するなど慎重に投与すること。一般に生理機能が低下している。
副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
重大な副作用
その他の副作用
| 頻度不明 |
|---|
過敏症 | 蕁麻疹等の発疹、紅斑、そう痒、浮腫 |
|---|
鼻腔 | 鼻症状(刺激感、そう痒感、乾燥感、不快感)注)、くしゃみ発作、鼻出血注)、感染注)、異臭感、嗅覚障害 |
|---|
口腔並びに呼吸器 | 咽喉頭症状(刺激感、異物感)、感染注) |
|---|
消化器 | 食欲不振、悪心、嘔吐、下痢 |
|---|
循環器 | 高血圧 |
|---|
精神神経系 | 頭痛、めまい |
|---|
その他 | 気管支喘息の発現・増悪、鼻中隔穿孔 |
|---|
過量投与
症状
下垂体・副腎皮質系機能抑制があらわれることがある。この抑制が長期にわたった場合、副腎皮質ステロイド剤を全身投与した場合と同様な症状があらわれることがある。
処置
全身性ステロイド療法を中止する手順で本剤を徐々に減量すること。
適用上の注意
薬剤交付時の注意
使用前
患者には添付の携帯袋(
をお使いになる患者さんと保護者の方へ)を渡し、使用方法を指導すること。
使用時
容器は振らずに使用すること。
初回使用時のみ予備噴霧を行うこと。
噴霧口を針やピン等で突かないこと。
その他の注意
臨床使用に基づく情報
レセルピン系製剤、α-メチルドパ製剤等の降圧剤には、副作用として鼻閉がみられることがある。このような降圧剤服用中のアレルギー性鼻炎又は血管運動性鼻炎の患者に、本剤を投与すると、鼻閉症状に対する本剤の効果が隠蔽されるおそれがあるので、臨床的観察を十分に行いながら投与すること。
薬効薬理
作用機序
ベクロメタゾンプロピオン酸エステルは合成糖質副腎皮質ステロイドであり、局所抗炎症作用を有する。
アレルギー性鼻炎モデルにおける作用
本剤の点鼻投与は、受動感作ラットにおける抗原誘発鼻粘膜血管透過性亢進モデル及び能動感作モルモットにおける抗原誘発鼻腔内圧上昇モデルの2種類の実験的アレルギー性鼻炎モデルに対して、用量依存的な抑制作用を示した。
生物学的同等性試験
本剤とアルデシンAQネーザル50μgについて、同一用量の点鼻投与による薬効薬理作用の同等性確認試験を行った。両剤は、抗原誘発鼻粘膜血管透過性亢進モデル(ラット)における漏出色素量増加及び抗原誘発鼻腔内圧上昇モデル(モルモット)における鼻腔内圧上昇を同程度に抑制した。また、両剤の抑制作用に有意な差は認められなかったことより、両剤が生物学的に同等の抑制作用を示すと判断された。
有効成分に関する理化学的知見
一般的名称
ベクロメタゾンプロピオン酸エステル
(Beclometasone Dipropionate)
化学名
9-Chloro-11β,17,21-trihydroxy-16β-methylpregna-1,4-diene-3,20-dione 17,21-dipropanoate
分子式
C28H37ClO7
分子量
521.04
性状
白色~微黄色の粉末で、においはない。クロロホルムに溶けやすく、メタノールにやや溶けやすく、エタノール(95)又は1,4-ジオキサンにやや溶けにくく、ジエチルエーテルに溶けにくく、水にほとんど溶けない。
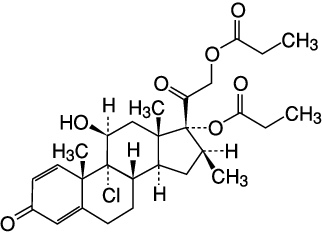
化学構造式
融点
約208℃(分解)
包装
主要文献
文献請求先及び問い合わせ先
製造販売業者等