1
Yonemori K, et al.:Cancer Sci. 2008;99(6):1237-1242
2
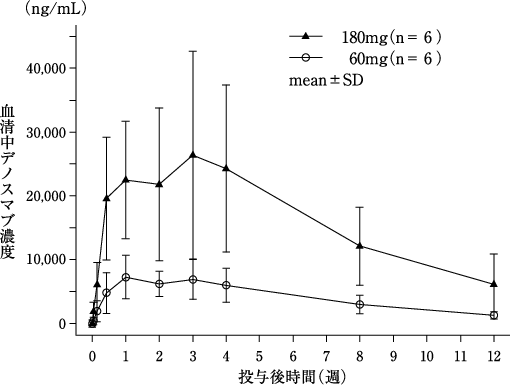
Kumagai Y, et al.:Bone. 2011;49(5):1101-1107
3
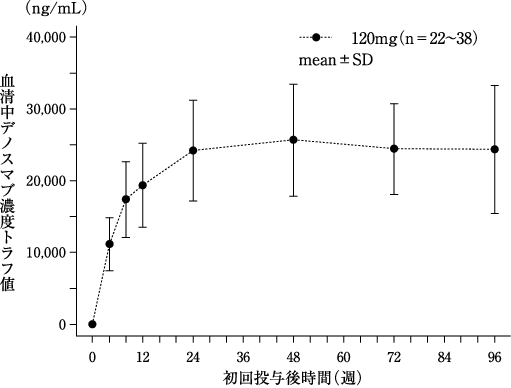
社内資料:骨転移を有する乳癌患者を対象とした第Ⅲ相臨床試験における日本人被験者の薬物動態(2012年1月18日承認、CTD2.7.2.2)
4
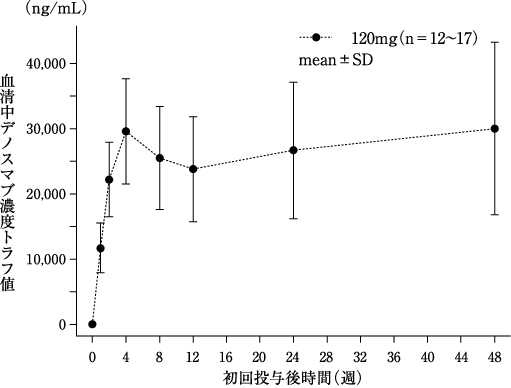
社内資料:骨巨細胞腫患者を対象とした国内第Ⅱ相臨床試験における薬物動態(2014年5月23日承認、CTD2.7.6.4)
5
社内資料:健康被験者、低骨密度又は骨粗鬆症の閉経後女性及びがん患者におけるデノスマブの母集団薬物動態解析(2012年1月18日承認、CTD2.7.2.3)
6
社内資料:125I標識デノスマブを単回皮下投与したカニクイザルにおける分布及び排泄(2012年1月18日承認、CTD2.6.4)
7
社内資料:125I標識デノスマブを単回皮下投与したカニクイザルにおけるQWBA試験(2012年1月18日承認、CTD2.6.4.4)
8
Block GA, et al.:J Bone Miner Res. 2012;27(7):1471-1479
9
社内資料:重度腎疾患患者及び透析の必要な末期腎不全患者を対象とした第Ⅰ相臨床試験結果(2014年5月23日承認、CTD2.7.4.5)
10
Stopeck AT, et al.:J Clin Oncol. 2010;28(35):5132-5139
11
Fizazi K, et al.:Lancet. 2011;377(9768):813-822
12
Henry DH, et al.:J Clin Oncol. 2011;29(9):1125-1132
13
Ueda T, et al.:Ann Oncol. 2015;26(10):2149-2154
14
社内資料:骨巨細胞腫患者を対象とした外国第Ⅱ相臨床試験における客観的奏効率(2014年5月23日承認、CTD2.7.3.3)
15
社内資料:腎機能の程度が異なる被験者を対象とした薬物動態試験における低カルシウム血症の発現状況(2012年1月18日承認、CTD2.7.6.10)
16
Lacey DL, et al.:Cell. 1998;93(2):165-176
17
Roodman GD, et al.:Cancer Treat Rev. 2008;34(1):92-101
18
社内資料:デノスマブのRANKLに対する結合試験(2012年1月18日承認、CTD2.6.2.2)
19
Kostenuik PJ, et al.:J Bone Miner Res. 2009;24(2):182-195
20
社内資料:デノスマブの骨吸収抑制作用(2012年1月18日承認、CTD2.6.2.2)
21
Roux S, et al.:Am J Clin Pathol. 2002;117(2):210-216
22
Branstetter DG, et al.:Clin Cancer Res. 2012;18(16):4415-4424
23
社内資料:カニクイザルにおけるデノスマブ投与試験(2012年1月18日承認、CTD2.6.2.2)
24
社内資料:乳癌のマウス骨転移モデルにおけるOPG-Fcの効果(2012年1月18日承認、CTD2.6.2.2)
25
Morony S, et al.:Cancer Res. 2001;61(11):4432-4436
26
Canon JR, et al.:Clin Exp Metastasis. 2008;25(2):119-129
27
社内資料:前立腺癌のマウス骨転移モデルにおけるOPG-Fcの効果(2012年1月18日承認、CTD2.6.2.2)
28
社内資料:肺癌のマウス骨転移モデルにおけるOPG-Fcの効果(2012年1月18日承認、CTD2.6.2.2)