作成又は改訂年月
**
2019年3月改訂
(第8版)
*
2012年6月改訂
日本標準商品分類番号
薬効分類名
承認等
販売名
*プロチレリン酒石酸塩注射液1mg「サワイ」
販売名コード
承認・許可番号
22300AMX01275000
PROTIRELIN TARTRATE
薬価基準収載年月
販売開始年月
貯法・使用期限等
規制区分
処方箋医薬品
注意−医師等の処方箋により使用すること
組成及び性状の表
| 有効成分・含量 | 添加物 | 剤形・性状 | pH | 浸透圧比 |
1アンプル(1mL)中
日局プロチレリン酒石酸塩水和物 1.464mg
(プロチレリンとして1mg) | D-ソルビトール 50mg
塩化ナトリウム、塩化カリウム、pH調節剤 | 無色澄明の注射液 | 5.5〜6.5 | 約1
(生理食塩液に対する比) |
販売名
*プロチレリン酒石酸塩注射液2mg「サワイ」
販売名コード
承認・許可番号
22300AMX01241000
PROTIRELIN TARTRATE
薬価基準収載年月
販売開始年月
貯法・使用期限等
規制区分
処方箋医薬品
注意−医師等の処方箋により使用すること
組成及び性状の表
| 有効成分・含量 | 添加物 | 剤形・性状 | pH | 浸透圧比 |
1アンプル(1mL)中
日局プロチレリン酒石酸塩水和物 2.928mg
(プロチレリンとして2mg) | D-ソルビトール 50mg
pH調節剤 | 無色澄明の注射液 | 5.5〜6.5 | 約1
(生理食塩液に対する比) |
一般的名称
効能又は効果/用法及び用量
下記疾患に伴う昏睡、半昏睡を除く遷延性意識障害
頭部外傷
くも膜下出血、ただし、意識障害固定期間3週以内
通常、成人には疾患に応じて、下記の用量を1日1回10日間静注又は点滴静注する。静脈内注射の場合は、生理食塩液、ブドウ糖注射液又は注射用水5〜10mLに希釈して、徐々に注射する。
頭部外傷:1回プロチレリン酒石酸塩水和物として0.732〜2.92mg(プロチレリンとして0.5〜2mg)
くも膜下出血(ただし、意識障害固定期間3週以内):1回プロチレリン酒石酸塩水和物として2.92mg(プロチレリンとして2mg)
通常、成人には1日1回プロチレリン酒石酸塩水和物として0.732〜2.92mg(プロチレリンとして0.5〜2mg)を筋肉内又は静脈内に注射するが、重症例にはプロチレリン酒石酸塩水和物として2.92mg(プロチレリンとして2mg)を注射する。
2〜3週間連日注射した後、2〜3週間の休薬期間をおく。以後、これを反復するか、週2〜3回の間歇注射を行う。
静脈内注射の場合は、生理食塩液、ブドウ糖注射液又は注射用水5〜10mLに希釈して、徐々に注射する。
使用上の注意
慎重投与
心障害のある患者〔本剤は血圧および脈拍数を一過性に上昇させることがある。〕
**遺伝性果糖不耐症の患者〔本剤の添加剤D-ソルビトールが体内で代謝されて生成した果糖が正常に代謝されず、低血糖、肝不全、腎不全等が誘発されるおそれがある。〕
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用
(頻度不明)
一過性の血圧低下、意識喪失等のショック様症状があらわれることがある。
痙攣があらわれることがある。
下垂体腺腫患者に投与した場合、頭痛、視力・視野障害等を伴う下垂体卒中があらわれることがあるので、このような症状があらわれた場合には外科的治療等適切な処置を行うこと。
血小板減少があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
その他の副作用
| 頻度不明 |
| 循環器 | 脈拍数の変動、熱感、顔面潮紅感、動悸、胸部圧迫感、血圧の変動 |
| 消化器 | 悪心、心窩部不快感、嘔吐、食欲不振、腹痛、口渇、異味感 |
| 肝臓 | AST(GOT)、ALT(GPT)、Al-Pの上昇 |
| 血液 | 貧血、白血球減少 |
| 精神神経系 | 興奮、多弁、頭痛、めまい、しびれ感、振戦、不安、不眠 |
| 過敏症注) | 発疹、そう痒 |
| その他 | 尿意、発熱、発汗、悪寒、倦怠感、脱力感、咽頭違和感、浮腫、排尿障害、乳房腫大、乳汁分泌 |
妊婦、産婦、授乳婦等への投与
妊婦又は妊娠している可能性のある婦人には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。〔妊娠中の投与に関する安全性は確立していない。〕
小児等への投与
低出生体重児、新生児、乳児、幼児、小児に対する安全性は確立していない。
適用上の注意
静脈内投与にあたってはできるだけゆっくり投与すること。〔急速に静脈内注射すると、一過性の尿意、悪心、熱感等があらわれやすい。〕
筋肉内注射にあたっては、組織・神経等への影響を避けるため、下記の点に注意すること。
同一部位への反復注射は行わないこと。
なお、小児には特に注意すること。
神経走行部位を避けるよう注意すること。
注射針を刺入したとき、激痛を訴えたり、血液の逆流をみた場合は、直ちに針を抜き、部位をかえて注射すること。
アンプルカット時:本品は、ワンポイントアンプルなので、マークを上にして下方へ折ること。なお、アンプルカット部分をエタノール綿等で清拭してからカットすることが望ましい。
その他の注意
本剤の連用により、TRHに対するTSH分泌反応が低下するので、定められた投与期間を標準として投与すること。
本剤の連用によるTSH分泌反応低下は連用中止1週ないし2週後に回復するので、TRHテストを施行する場合はその後に行うこと。
甲状腺ホルモン剤、抗甲状腺剤、副腎皮質ステロイド剤投与中の患者ではTRHに対するTSH分泌反応が変化することがある。
薬効薬理
プロチレリン(TRH,thyrotropin releasing hormone)はグルタミン酸・ヒスチジン・プロリンの3つのアミノ酸からなるペプチドで、視床下部ホルモンとして下垂体からの甲状腺刺激ホルモン、プロラクチンの放出を促進する。
中脳−辺縁ドーパミン系の賦活、アセチルコリン作動性ニューロンの賦活などを介して、自発運動亢進作用、覚醒促進作用、脳波賦活作用が発現するとされている。
有効成分に関する理化学的知見
一般名
プロチレリン酒石酸塩水和物(Protirelin Tartrate Hydrate)
化学名
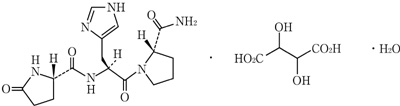
5-Oxo-L-prolyl-L-histidyl-L-prolinamide monotartrate monohydrate
分子式
C16H22N6O4・C4H6O6・H2O
分子量
530.49
融点
約187℃(分解)
構造式
性状
プロチレリン酒石酸塩水和物は白色〜微帯黄白色の結晶又は結晶性の粉末である。水に溶けやすく、酢酸(100)にやや溶けにくく、エタノール(95)又はジエチルエーテルにほとんど溶けない。
取扱い上の注意
・安定性試験
1mg:ガラスアンプルに充てんしたものを用いた加速試験(40℃75%RH、6ヶ月)の結果、通常の市場流通下において3年間安定であることが推測された。1)
2mg:ガラスアンプルに充てんしたものを用いた長期保存試験(室温、3年間)の結果、通常の市場流通下において3年間安定であることが確認された。2)
包装
プロチレリン酒石酸塩注射液1mg「サワイ」:10アンプル
プロチレリン酒石酸塩注射液2mg「サワイ」:10アンプル
主要文献及び文献請求先
主要文献
1
沢井製薬(株)社内資料[安定性試験]
2
沢井製薬(株)社内資料[安定性試験]
文献請求先
〔主要文献(社内資料を含む)は下記にご請求下さい〕
沢井製薬株式会社 医薬品情報センター
〒532-0003 大阪市淀川区宮原5丁目2-30
TEL:0120-381-999
FAX:06-6394-7355
製造販売業者等の氏名又は名称及び住所
製造販売元
沢井製薬株式会社
大阪市淀川区宮原5丁目2-30