1
社内資料:ラット胚・胎児発生に関する試験(2022年12月23日承認、CTD2.6.6.6.2.3)
2
社内資料:ウサギ胚・胎児発生に関する試験(2022年12月23日承認、CTD2.6.6.6.3.3)
3
社内資料:薬物動態試験〈乳汁移行性〉(2022年12月23日承認、CTD2.6.4.6)
4
社内資料:マウス2年間がん原性試験(2022年12月23日承認、CTD2.6.6.5.3)
5
社内資料:ラット2年間がん原性試験(2022年12月23日承認、CTD2.6.6.5.6)
6
社内資料:作用機序(2022年12月23日承認、CTD2.6.2.2.1)
7
社内資料:ラット13週間用量設定試験(2022年12月23日承認、CTD2.6.6.5.5)
8
社内資料:サル13週間反復経口投与毒性試験(2022年12月23日承認、CTD2.6.6.3.3.3)
9
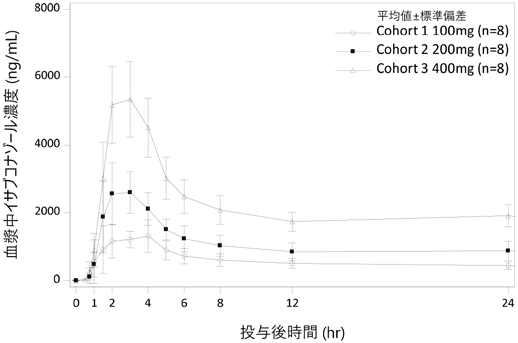
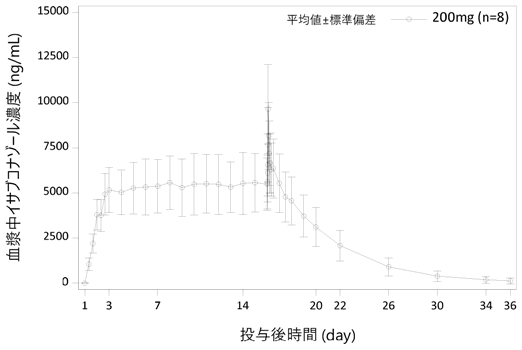
社内資料:臨床薬理試験〈第I相/PK〉(2022年12月23日承認、CTD2.7.6.5)
10
Shirae S, et al.: Clin Pharmacol Drug Dev. 2022;11(6):744-753
11
社内資料:臨床薬理試験(2022年12月23日承認、CTD2.7.2.3)
12
社内資料:臨床薬理試験(2022年12月23日承認、CTD2.5.3.1)
13
米国添付文書
14
社内資料:臨床薬理試験〈薬物相互作用試験(in vitro)〉(2022年12月23日承認、CTD2.7.2.2)
15
社内資料:日本人深在性真菌症を対象とした国内第Ⅲ相試験(2022年12月23日承認、CTD2.7.6.45)
16
Kohno S, et al.: J Infect Chemother. 2023;29(2):163-170
17
社内資料:海外第Ⅲ相試験(9766-CL-0104試験)(2022年12月23日承認、CTD2.7.6.46)
18
Maertens JA, et al.: Lancet. 2016;387:760-769
19
社内資料:海外第Ⅲ相試験(9766-CL-0103試験)(2022年12月23日承認、CTD2.7.6.47)
20
Marty FM, et al.: Lancet Infect Dis. 2016;16:828-837
21
社内資料:In vitro抗真菌作用(2022年12月23日承認、CTD2.6.2.2.3)
22
社内資料:In vivo抗真菌作用(2022年12月23日承認、CTD2.6.2.2.4)