作成又は改訂年月
**
2019年7月改訂
(第11版)
*
2014年3月改訂
日本標準商品分類番号
日本標準商品分類番号等
1996年3月
1990年3月
薬効分類名
承認等
販売名
ニポラジン錠3mg
販売名コード
承認・許可番号
21900AMX01296000
NIPOLAZIN Tablets 3mg
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯 法
遮光・気密容器、室温保存
使用期限
外箱等に表示
規制区分
組成
性状
| 添加物 | D−マンニトール、トウモロコシデンプン、カルメロースナトリウム、ステアリン酸マグネシウム |
|---|
| 性 状 | 白色の割線入り錠剤 |
|---|
| 外 形 | 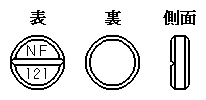 |
|---|
| 大きさ | 直径:8.0mm 厚さ:2.5mm |
|---|
| 質 量 | 170mg |
|---|
| 識別コード | NF121 |
|---|
一般的名称
禁忌
1本剤の成分、フェノチアジン系化合物及びその類似化合物に対し過敏症の既往歴のある患者
2**閉塞隅角緑内障の患者
[抗コリン作用により眼圧が上昇し、症状を悪化させることがある。]
3前立腺肥大等下部尿路に閉塞性疾患のある患者
[抗コリン作用により排尿困難等を起こすことがある。]
効能又は効果
気管支喘息
アレルギ―性鼻炎
じん麻疹
皮膚疾患に伴うそう痒(湿疹・皮膚炎、皮膚そう痒症)
用法及び用量
[気管支喘息の場合]
通常成人1回2錠(メキタジンとして6mg)を1日2回経口投与する。
なお、年齢、症状に応じて適宜増減する。
[アレルギ―性鼻炎、じん麻疹、皮膚疾患に伴うそう痒(湿疹・皮膚炎、皮膚そう痒症)の場合]
通常成人1回1錠(メキタジンとして3mg)を1日2回経口投与する。
なお、年齢、症状に応じて適宜増減する。
使用上の注意
慎重投与
1腎障害のある患者
[長期投与例で臨床検査値異常としてBUN上昇がみられることがある。]
2**開放隅角緑内障の患者
[抗コリン作用により眼圧が上昇し、症状を悪化させることがある。]
3高齢者
[「高齢者への投与」の項参照]
重要な基本的注意
眠気を催すことがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械操作には従事させないよう十分注意すること。
相互作用
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|
中枢神経抑制剤(バルビツール酸誘導体、麻酔剤、麻薬性鎮痛剤、鎮静剤、精神安定剤等)
フェノバルビタ−ル等 | 眠気等があらわれることがあるので、減量するなど注意すること。 | 本剤の中枢神経抑制作用により、作用が増強されることがある。 |
|---|
抗コリン作用を有する薬剤(三環系抗うつ剤、MAO阻害剤等)
イミプラミン塩酸塩、ブチルスコポラミン臭化物等 | 口渇、排尿困難等があらわれることがあるので、減量するなど注意すること。 | 本剤の抗コリン作用により、作用が増強されることがある。 |
|---|
| メトキサレン | 光線過敏症を起こすおそれがある。 | これらの薬剤は光線感受性を高める作用を有する。 |
|---|
| アルコ−ル | 眠気等があらわれることがあるので、アルコ−ル含有清涼飲料水等の摂取に注意すること。 | 本剤の中枢神経抑制作用により、作用が増強されることがある。 |
|---|
副作用
再審査終了時
ニポラジン錠及びゼスラン錠(共同開発品目)、総症例30,168例中、1,005例(3.33%)に副作用が認められた。
その主なものは、眠気654件(2.17%)、けん怠感139件(0.46%)、口渇134件(0.44%)等であった。
重大な副作用
1**ショック、アナフィラキシー(頻度不明)
ショック、アナフィラキシーを起こすことがあるので、観察を十分に行い、血圧低下、呼吸困難、咽頭浮腫、蕁麻疹、嘔気等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。
2肝機能障害、黄疸(頻度不明)
AST(GOT)、ALT(GPT)、Al-P等の上昇を伴う肝機能障害、黄疸があらわれることがある。また、劇症肝炎の報告がある。観察を十分に行い、異常が認められた場合には投与を中止するなど、適切な処置を行うこと。
3血小板減少(頻度不明)
血小板減少があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど、適切な処置を行うこと。
その他の副作用
| 0.1〜5%未満 | 0.1%未満 | 頻度不明 |
| 過敏症注1) | − | 発疹、光線過敏症 | − |
| 肝 臓注2) | − | AST(GOT)の上昇、ALT(GPT)の上昇 | 黄疸 |
| 血 液注1) | − | 血小板減少 | − |
| 精神神経系 | 眠気、けん怠感、ふらふら感 | 頭痛、めまい | 興奮 |
| 消化器 | 口渇、胃部不快感 | 下痢、便秘、食欲不振、嘔吐、胃痛、腹痛 | − |
| 循環器 | − | 胸部苦悶感、心悸亢進 | − |
| 泌尿器 | − | 排尿困難 | − |
| その他 | − | 咽頭痛、浮腫、顔面潮紅、視調節障害、
月経異常、味覚異常、口内しびれ感 | − |
高齢者への投与
高齢者では副作用があらわれやすいので、注意すること。臨床試験において高齢者に口渇等の副作用の発現率が高い傾向が認められている。
妊婦、産婦、授乳婦等への投与
1妊婦又は妊娠している可能性のある婦人には投与しないことが望ましい。
[妊娠中の投与に関する安全性は確立していない。]
2授乳婦に投与する場合には授乳を中止させること。
[動物実験(ラット)で乳汁中へ移行することが報告されている。]
小児等への投与
低出生体重児、新生児、乳児、幼児又は小児に対する安全性は確立していない。
[使用経験が少ない。]
過量投与
徴候、症状
誤って過量服用したときに眠気、悪心、嘔吐、軽度の抗コリン作用性障害がみられる。
処 置
通常、早期には催吐、胃洗浄を行う。必要に応じ補助呼吸又は人工呼吸、抗痙攣剤を投与する。
適用上の注意
薬剤交付時
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。[PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することが報告されている。]
その他の注意
動物実験(ラット)でメラニンに対する親和性が認められている。また、他のフェノチアジン系化合物の長期投与又は大量投与により角膜・水晶体の混濁、網膜・角膜の色素沈着が報告されているので注意すること。
薬物動態
1血中濃度1)
1単回投与
健常人に3mg(n=4)又は6mg(n=4)を食後1回経口投与した場合の薬動力学的パラメ−タ−は[薬物動態の表]の通りであった。
2反復投与
健常人に3mg(n=4)又は6mg(n=4)を1日2回食後反復経口投与した場合、血中濃度は投与7日目までに定常状態に達し、その血中濃度は単回投与の最高血中濃度の3〜4倍であり、生物学的半減期T1/2(β)は単回投与時とほぼ同程度であった。
2代 謝2)
健常人に経口投与した場合、尿から未変化体のほかに代謝物として3種類の遊離体(SO、NO、モノ水酸化体)及びグルクロン酸抱合体が確認されている。
3排 泄2)
健常人に経口投与した場合、48時間以内に投与量の約20%が尿中へ排泄される。
薬物動態の表
投与量
(mg) | Cmax
(ng/mL) | Tmax
(hr) | AUC0→∞
(ng・hr/mL) | T1/2(α)
(hr) | T1/2(β)
(hr) |
| 3 | 2.00±0.10 | 6.70±0.62 | 99.40±29.16 | 5.43±0.71 | 32.7±3.2 |
| 6 | 5.36±0.23 | 6.74±0.91 | 252.38±14.60 | 6.65±1.61 | 38.6±3.7 |
臨床成績
本剤の臨床試験成績の概要は[臨床成績の表]のとおりである3〜16)。
臨床成績の表
| 疾患名 | 有効率 |
| 気管支喘息 | 39.9%(81/203) |
| アレルギ−性鼻炎 | 54.8%(244/445) |
| じん麻疹 | 69.5%(228/328) |
| 湿疹・皮膚炎群 | 62.6%(122/195) |
| 皮膚そう痒症 | 71.1%(59/83) |
薬効薬理
1ケミカルメディエ−タ−拮抗作用17〜20)
1ヒスタミン、ロイコトリエン、アセチルコリンによるモルモット摘出回腸・気管筋・肺実質収縮、ブラジキニン、セロトニンによるモルモット摘出回腸収縮、PAF(血小板活性化因子)によるモルモット摘出気管筋収縮、プロスタグランジンF2αによるモルモット摘出肺実質収縮を抑制する(in vitro)。
2抗ヒスタミン作用
ヒスタミン致死を長時間防御する(マウス)。
2ケミカルメディエ−タ−遊離抑制作用19,20)
ラット腹腔細胞、ヒト肺、ヒト白血球からのヒスタミン及びヒト肺、ヒト白血球からのロイコトリエンの遊離を抑制する(in vitro)。これらの遊離抑制作用の機序の一部としてホスホジエステラ−ゼ活性の阻害、Ca2+流入阻害等の関与が考えられている(in vitro)。
抗アレルギ−作用18,21)
1遊離メディエ−タ−に対する作用
感作モルモット肺切片からの遊離メディエ−タ−による回腸収縮を抑制する(in vitro)。
2局所アナフィラキシ−反応に対する作用
homologous PCA反応を長時間抑制する(ラット)。
3全身アナフィラキシ−反応に対する作用
能動的及び受動的全身アナフィラキシ−反応を抑制する(モルモット)。
4抗喘息作用
抗原の静注又は吸入により誘発される実験的喘息を抑制する(モルモット)。
有効成分に関する理化学的知見
一般名
メキタジン(Mequitazine)
化学名
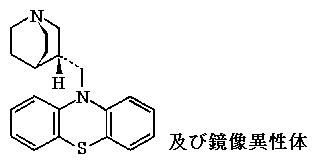
10-[(3RS)-1-Azabicyclo[2,2,2]oct-3-ylmethyl]-10H-phenothiazine
構造式
分子式
C20H22N2S
分子量
322.47
性 状
白色の結晶又は結晶性の粉末である。メタノ−ル又は酢酸(100)に溶けやすく、エタノール(95)にやや溶けやすく、水にほとんど溶けない。メタノ−ル溶液(1→50)は旋光性を示さない。光によって徐々に着色する。
融 点
146〜150℃
分配係数
3.79(pH6.98、水-シクロヘキサン系)
包装
100錠、500錠、1000錠、3000錠(PTP)、1000錠(バラ)
主要文献及び文献請求先
主要文献
1寺門敬夫 他:メキタジンの健常人における体内動態に関する研究(社内資料)
2中島光好 他:メキタジンの健康人における薬物動態と作業能率におよぼす影響(社内資料)
3信太隆夫 他:臨床医薬,4,611(1988)
4長野 準 他:臨床医薬,4,991(1988)
5長野 準 他:臨床医薬,4,735(1988)
6三井健司:臨床医薬,4,745(1988)
7佐野靖之 他:Prog Med,8,2159(1988)
8須貝哲郎:基礎と臨床,15,2897(1981)
9久木田淳 他:皮膚,23,332(1981)
10雲井健雄 他:耳鼻臨床,74,171(1981)
11古内一郎 他:耳鼻咽喉科展望,24(補1),74(1981)
12須貝哲郎:基礎と臨床,15,4466(1981)
13久木田淳 他:西日本皮膚科,43,1346(1981)
14武田一雄 他:耳鼻臨床,74,381(1981)
15外松茂太郎 他:皮膚,23,260(1981)
16斉藤英雄 他:耳鼻咽喉科展望,27(補4),531(1984)
17藤村 一 他:日本薬理学雑誌,78,279(1981)
18藤村 一 他:日本薬理学雑誌,78,291(1981)
19河野茂勝 他:日本薬理学雑誌,92,145(1988)
20Tasaka,K.et al.:Arzneimittelforschung/Drug Res,40,1092(1990)
21河野茂勝 他:日本薬理学雑誌,92,159(1988)
文献請求先
主要文献に記載の社内資料につきましても下記にご請求下さい。
**アルフレッサ ファーマ株式会社 製品情報部
〒540-8575 大阪市中央区石町二丁目2番9号
TEL 06-6941-0306 FAX 06-6943-8212
製造業者又は輸入販売業者の氏名又は名称及び住所
製造販売元
アルフレッサ ファーマ株式会社
大阪市中央区石町二丁目2番9号