1
国内のMDS患者にアザシチジンを皮下または静脈内投与した場合の薬物動態(ビダーザ注射用:2011年1月21日承認、申請資料概要 2.7.1.2.2)
2
海外のMDS患者にアザシチジンを皮下または静脈内投与した場合の薬物動態(ビダーザ注射用:2011年1月21日承認、申請資料概要 2.7.1.2.1)
3
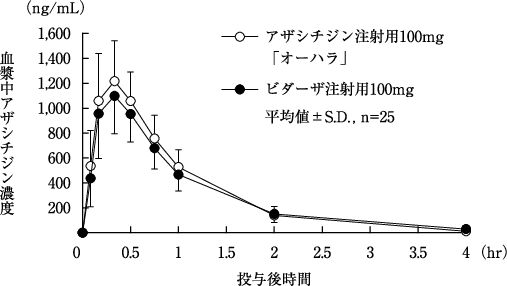
大原薬品工業株式会社 社内資料:生物学的同等性試験(2021年)
4
in vitroヒト血清タンパク結合率(ビダーザ注射用:2011年1月21日承認、申請資料概要 2.6.4.4.2)
5
in vitroヒト血球移行率(ビダーザ注射用:2011年1月21日承認、申請資料概要 2.6.4.4.5)
6
Daher GC, et al.:Pharmacol Ther. 1990;48:189-222
7
in vitro代謝試験(ビダーザ注射用:2011年1月21日承認、申請資料概要 2.6.4.5)
8
in vitro代謝試験(ビダーザ注射用:2011年1月21日承認、審査報告書)
9
Troetel WM, et al.:Cancer Chemother Rep. 1972;56:405-411
10
Israili ZH, et al.:Cancer Res. 1976;36:1453-1461
11
雄性ラットに静脈内投与又は皮下投与した後の尿及び糞中排泄率(ビダーザ注射用:2011年1月21日承認、申請資料概要 2.6.4.6.3)
12
Laille E, et al.:Pharmacotherapy. 2014;34:440-451
13
Uchida T, et al.:Cancer Sci. 2011;102:1680-1686
14
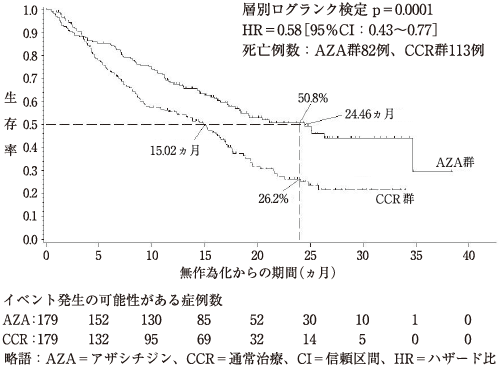
骨髄異形成症候群に対するアザシチジンの外国第Ⅲ相比較試験(AZA-001試験)(ビダーザ注射用:2011年1月21日承認、申請資料概要 2.7.3.3.2.1)
15
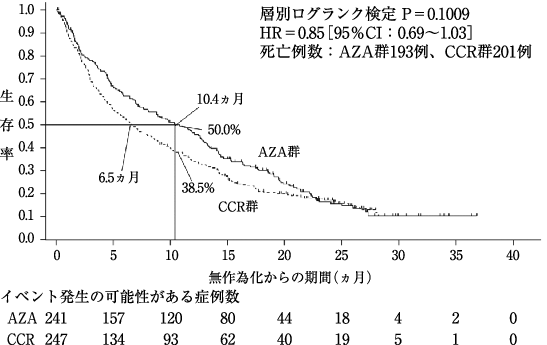
Dombret H, et al.:Blood. 2015;126:291-299
16
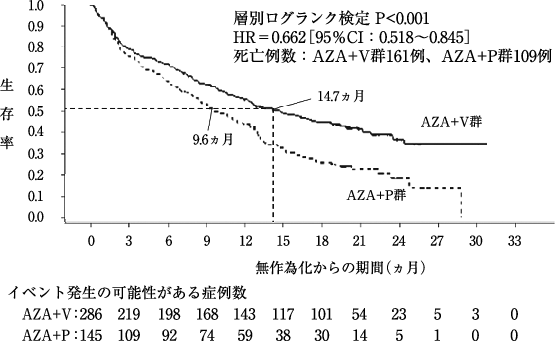
DiNardo CD, et al.:N Engl J Med. 2020;383:617-629
17
Hollenbach PW, et al.:PLoS ONE. 2010;5:e9001
18
Hofmann WK, et al.:Leuk Res. 2006;30:1347-1353
19
Khan R, et al.:Exp Hematol. 2006;34:35-43
20
Kimura S, et al.:Anticancer Res. 2012;32:795-798




 0120-419-363 FAX 03-6740-7703
0120-419-363 FAX 03-6740-7703

