1
Hattori M, et al.: Clin Exp Nephrol. 2014; 18: 634-641[88854]
2
Besarab A, et al.: N Engl J Med. 1998; 339: 584-590[88855]
3
Singh AK, et al.: N Engl J Med. 2006; 355: 2085-2098[88856]
4
Pfeffer MA, et al.: N Engl J Med. 2009; 361: 2019-2032[88857]
5
Leyland-Jones B, et al.: J Clin Oncol. 2005; 23: 5960-5972[88858]
6
Henke M, et al.: Lancet. 2003; 362: 1255-1260[88859]
7
Overgaard J, et al.: J Clin Oncol. 2009; 27: 302s[88860]
8
Luksenburg H, et al.: FDA Briefing Document. ODAC May 4, 2004[88861]
9
Smith RE Jr, et al.: J Clin Oncol. 2008; 26: 1040-1050[88862]
10
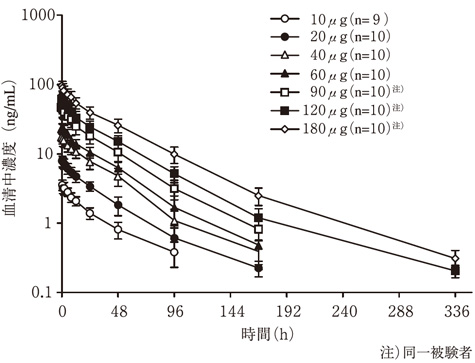
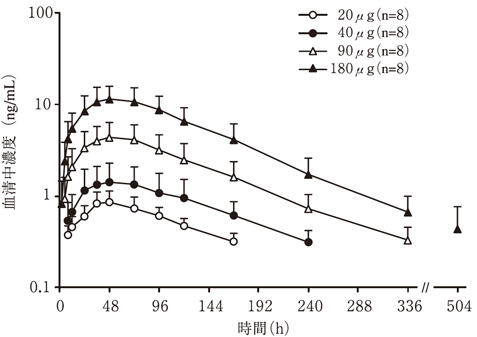
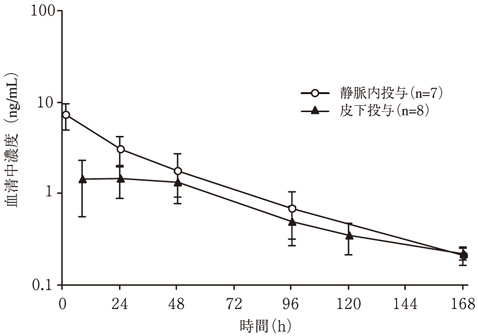
社内資料:健康成人を対象とした第Ⅰ相臨床試験[88825]
11
菅朗ほか:腎と透析. 2007; 63: 625-631[000149]
12
Uematsu T, et al.: Jpn J Clin Pharmacol Ther. 2007; 38: 331-339 [000150]
13
飯野靖彦ほか:腎と透析. 2010; 68: 111-120[000151]
14
Uemura O, et al.: Clin Exp Nephrol. 2014; 18: 932-938[000152]
15
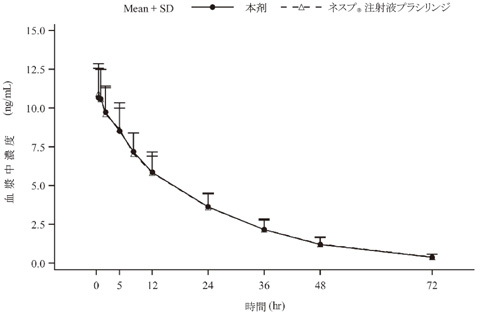
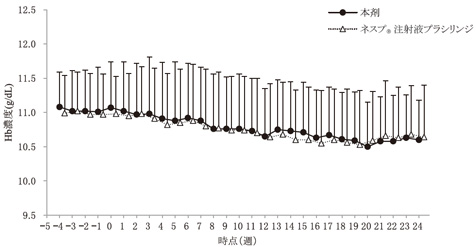
ネスプⓇ注射液プラシリンジ:本剤反復投与による薬物動態の検討(2010年4月16日承認、CTD 2.7.2.2)
16
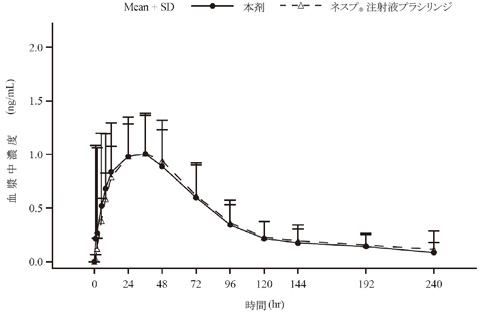
ネスプⓇ注射液プラシリンジ:保存期慢性腎臓病患者における皮下投与時のバイオアベイラビリティ(2010年4月16日承認、CTD 2.7.1.3)
17
ネスプⓇ注射液プラシリンジ:ラットにおける静脈内投与時の組織分布(2007年4月18日承認、CTD 2.6.4.4)
18
ネスプⓇ注射液プラシリンジ:ラットにおける皮下投与時の組織分布(2010年4月16日承認、CTD 2.6.4.4)
19
社内資料:血液透析施行中の腎性貧血患者を対象とした第Ⅲ相検証試験[88826]
20
保利敬ほか:腎と透析. 2007; 62: 679-691[000153]
21
Akizawa T, et al.: Ther Apher Dial. 2007; 11: 220-226[000154]
22
林晃正ほか:腎と透析. 2010; 68: 931-945[000155]
23
Akizawa T, et al.: Ther Apher Dial. 2011; 15: 431-440[000156]
24
ネスプⓇ注射液プラシリンジ:腹膜透析患者を対象とした本剤の効果(第Ⅲ相)(2010年4月16日承認、CTD 2.7.3.3.3.3)
25
社内資料:ヒトエリスロポエチン受容体に対する結合親和性[88827]
26
社内資料:ヒトエリスロポエチン依存性細胞における増殖作用[88828]
27
社内資料:ヒト骨髄赤芽球系前駆細胞の分化・増殖促進作用[88829]
28
社内資料:正常ラットにおける単回静脈内及び単回皮下投与による赤血球造血促進作用[88830]
29
社内資料:病態モデルラットにおける間歇静脈内投与による貧血改善作用[88831]
30
永野伸郎ほか:腎と透析. 2006; 60: 1039-1046[000157]
31
ネスプⓇ注射液プラシリンジ:腎性貧血モデルラットにおける本剤及びエポエチン アルファ単回皮下投与時の貧血改善効果(2010年4月16日承認、CTD 2.6.2.2)