1
臨床薬理試験(個々の試験結果の要約)(ビビアント錠:2010年7月23日承認、申請資料概要2.7.2.2)
2
閉経後骨粗鬆症患者における薬物動態(ビビアント錠:2010年7月23日承認、申請資料概要2.7.3.2.1.2)
3
反復投与試験(ビビアント錠:2010年7月23日承認、審査報告書)
4
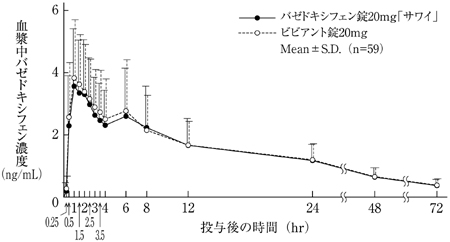
田中孝典他:新薬と臨床, 2020;69(6):735-745
5
生物薬剤学及び関連する分析法(個々の試験結果の要約)(ビビアント錠:2010年7月23日承認、申請資料概要2.7.1.2)
6
分布(ビビアント錠:2010年7月23日承認、申請資料概要2.6.4.4)
7
代謝(ビビアント錠:2010年7月23日承認、申請資料概要2.6.4.5)
8
臨床薬理試験(試験を通した結果の比較及び分析)(ビビアント錠:2010年7月23日承認、申請資料概要2.7.2.3)
9
Itabashi, A. et al.:J. Bone Miner. Res., 2011;26(3):519-529
10
国内第Ⅱ相試験(ビビアント錠:2010年7月23日承認、申請資料概要2.7.3.6, 2.7.6.19)
11
Silverman, S. L. et al.:J. Bone Miner. Res., 2008;23(12):1923-1934
12
海外第Ⅲ相試験(ビビアント錠:2010年7月23日承認、申請資料概要2.7.6.18)
13
作用機序(ビビアント錠:2010年7月23日承認、申請資料概要2.6.2.1)
14
薬理試験(効力を裏付ける試験)(ビビアント錠:2010年7月23日承認、申請資料概要2.6.2.2)