1
Mitchell DY, et al.: Br J Clin Pharmacol. 2000; 49: 215-222
2
Takata S, et al.: J Bone Miner Metab. 2006; 24: 359-367
3
高田信二郎 他: Osteoporosis Japan. 2007; 15: 246-249
4
MID-NET®を用いた調査結果の概要(MID-NET®を用いたビスホスホネート製剤の腎機能障害患者における低カルシウム血症のリスク評価に関するデータベース調査):
https://www.pmda.go.jp/files/000249186.pdf
https://www.pmda.go.jp/files/000249186.pdf
5
国内第Ⅰ相17.5mg単回投与試験(アクトネル錠17.5mg、ベネット錠17.5mg: 2007年4月18日承認、申請資料概要2.7.6.1)
6
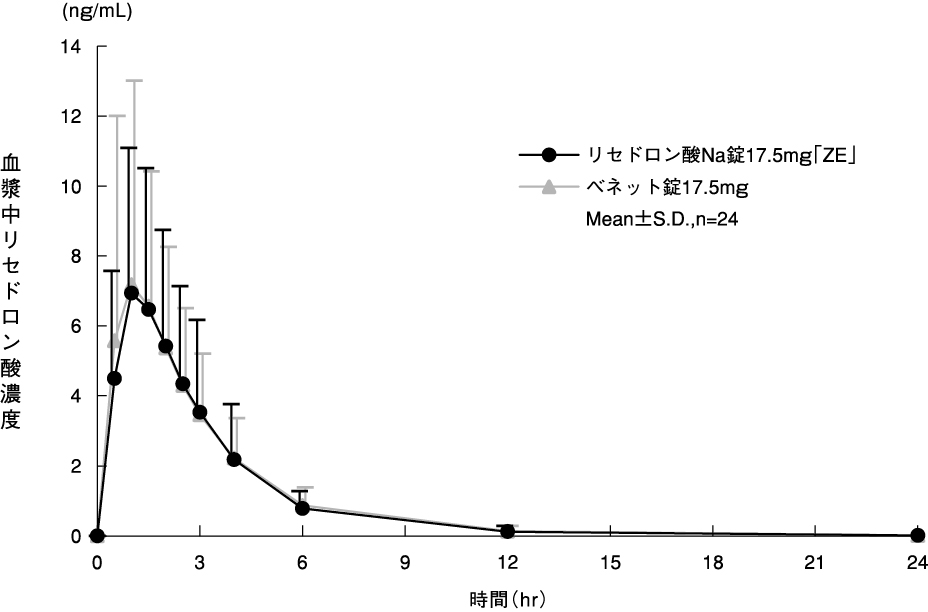
社内資料: 生物学的同等性試験
7
Ogura Y, et al.: J Bone Miner Metab. 2004; 22: 120-126
8
食事の影響(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、申請資料概要ヘ.3.(1).3))
9
飲料の影響について(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、審査報告書)
10
腎機能障害者における体内動態(外国)(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、申請資料概要ヘ.3.(6))
11
Kishimoto H, et al.: J Bone Miner Metab. 2006; 24: 405-413
12
Kushida K, et al.: J Bone Miner Metab. 2004; 22: 469-478
13
リセドロン酸ナトリウムの臨床試験成績(アクトネル錠17.5mg、ベネット錠17.5mg: 2008年7月16日承認、申請資料概要2.7.3.2)
14
国内第Ⅲ相試験(アクトネル錠17.5mg、ベネット錠17.5mg: 2008年7月16日承認、申請資料概要2.7.6.12)
15
Miller PD, et al.: Am J Med. 1999; 106: 513-520
16
外国第Ⅲ相試験(アクトネル錠17.5mg、ベネット錠17.5mg: 2008年7月16日承認、申請資料概要2.7.6.11)
17
作用機序に関する検討(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、申請資料概要ホ.1.(6))
18
ラット卵巣摘除モデルに対する12ヵ月間投与による予防的作用(アクトネル錠17.5mg、ベネット錠17.5mg: 2008年7月16日承認、申請資料概要2.6.2.2)
19
ミニブタ18ヵ月間投与による予防効果(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、申請資料概要ホ.1.(1).1))
20
Mosekilde L, et al.: Bone. 2000; 27: 639-645
21
骨密度と骨強度の相関性に関する検討(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、申請資料概要ホ.1.(4).1))
22
病態モデル系での石灰化に対する作用(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、申請資料概要ホ.1.(4).2))
23
成長期ラットにおける骨吸収及び骨石灰化に対する作用(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、申請資料概要ホ.1.(4).2))
24
ビーグル犬骨折モデルにおける骨折治癒に対する作用(リセドロネート原末、アクトネル錠2.5mg、ベネット錠2.5mg: 2002年1月17日承認、申請資料概要ホ.1.(5))








 0120-189-228
0120-189-228

