作成又は改訂年月
**印:
2020年7月改訂
(第12版)
*印:
2019年10月改訂
日本標準商品分類番号
薬効分類名
承認等
販売名
**タムスロシン塩酸塩カプセル0.1mg「武田テバ」
販売名コード
承認・許可番号
**30200AMX00680000
Tamsulosin Hydrochloride Cap.0.1mg "TAKEDA TEVA"
薬価収載
販売開始
使用期限等
貯 法
室温・気密容器保存
使用期限
外装に表示の使用期限内に使用すること。
規制区分
処方箋医薬品
(注意−医師等の処方箋により使用すること)
組成
1カプセル中:
タムスロシン塩酸塩 …………0.1mg
〈添加物〉
クエン酸トリエチル、結晶セルロース、酸化チタン、ステアリン酸カルシウム、ゼラチン、タルク、ポリソルベート80、メタクリル酸コポリマーLD、ラウリル硫酸ナトリウム、黄色三二酸化鉄
性状
蓋部ごくうすい黄色不透明、胴体部白色不透明、内容物が白色〜微黄白色の粒の4号カプセル剤
識別コード(PTP)
t 526
外形(サイズ)
側面

(全長 14.2mm)(重量 122.8mg)
外形(サイズ)
断面

(蓋部 5.3mm)(胴体部 5.1mm)
販売名
**タムスロシン塩酸塩カプセル0.2mg「武田テバ」
販売名コード
承認・許可番号
**30200AMX00681000
Tamsulosin Hydrochloride Cap.0.2mg "TAKEDA TEVA"
薬価収載
販売開始
使用期限等
貯 法
室温・気密容器保存
使用期限
外装に表示の使用期限内に使用すること。
規制区分
処方箋医薬品
(注意−医師等の処方箋により使用すること)
組成
1カプセル中:
タムスロシン塩酸塩 …………0.2mg
〈添加物〉
クエン酸トリエチル、結晶セルロース、酸化チタン、ステアリン酸カルシウム、ゼラチン、タルク、ポリソルベート80、メタクリル酸コポリマーLD、ラウリル硫酸ナトリウム、三二酸化鉄
性状
蓋部ごくうすい赤色不透明、胴体部白色不透明、内容物が白色〜微黄白色の粒の4号カプセル剤
識別コード(PTP)
t 527
外形(サイズ)
側面

(全長 14.2mm)(重量 205.6mg)
外形(サイズ)
断面

(蓋部 5.3mm)(胴体部 5.1mm)
一般的名称
禁忌
効能・効果
用法・用量
通常、成人にはタムスロシン塩酸塩として0.2mgを1日1回食後に経口投与する。
なお、年齢、症状により適宜増減する。
使用上の注意
慎重投与
起立性低血圧のある患者[症状が悪化するおそれがある]
重篤な肝機能障害のある患者[血漿中濃度が上昇するおそれがある]
重篤な腎機能障害のある患者[血漿中濃度が上昇するおそれがある]
高齢者 (「高齢者への投与」の項参照)
ホスホジエステラーゼ5阻害作用を有する薬剤を服用している患者 (「相互作用」の項参照)
重要な基本的注意
本剤の過剰投与により血圧低下が予想されるので、投与量には注意すること。
立位血圧が低下することがあるので、体位変換による血圧変化に注意すること。
本剤による治療は原因療法ではなく、対症療法であることに留意し、本剤投与により期待する効果が得られない場合は、手術療法等、他の適切な処置を考慮すること。
めまい等があらわれることがあるので、高所作業、自動車の運転等危険を伴う作業に従事する場合には注意させること。
本剤投与開始時に降圧剤投与の有無について問診を行い、降圧剤が投与されている場合には血圧変化に注意し、血圧低下がみられたときには、減量又は中止するなど適切な処置を行うこと。
相互作用
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|
降圧剤 | 起立性低血圧が起こるおそれがあるので、減量するなど注意すること。 | 降圧剤服用中の患者は起立時の血圧調節力が低下している場合がある。 |
|---|
ホスホジエステラーゼ5阻害作用を有する薬剤
シルデナフィルクエン酸塩
バルデナフィル塩酸塩水和物等 | 併用により症候性低血圧があらわれるとの報告がある。 | 本剤はα遮断作用を有するため、併用によりこれらの血管拡張作用による降圧作用を増強するおそれがある。 |
|---|
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用(頻度不明)
失神・意識喪失
血圧低下に伴う一過性の意識喪失等があらわれることがあるので、観察を十分に行い、異常が認められた場合には、本剤の投与を中止し適切な処置を行うこと。
肝機能障害、黄疸
AST(GOT)上昇、ALT(GPT)上昇、黄疸等があらわれることがあるので、観察を十分に行い、異常が認められた場合には、本剤の投与を中止するなど、適切な処置を行うこと。
その他の副作用
精神神経系
頻度不明
めまい、ふらふら感、立ちくらみ、頭痛、眠気、いらいら感、しびれ感
循環器
頻度不明
血圧低下、起立性低血圧、頻脈、動悸、不整脈
*過敏症注)
頻度不明
そう痒感、発疹、蕁麻疹、多形紅斑、血管浮腫
消化器
頻度不明
胃不快感、嘔気、嘔吐、口渇、便秘、胃重感、胃痛、食欲不振、下痢、嚥下障害
その他
頻度不明
鼻閉、浮腫、尿失禁、咽頭灼焼感、全身けん怠感、味覚異常、女性化乳房、持続勃起症、射精障害、術中虹彩緊張低下症候群、霧視、視力障害、ほてり、熱感、灼熱感
高齢者への投与
高齢者では腎機能が低下していることがあるので、腎機能が低下している場合は0.1mgから投与を開始し、経過を十分に観察した後に0.2mgに増量すること。0.2mgで期待する効果が得られない場合にはそれ以上の増量は行わず、他の適切な処置を行うこと。
適用上の注意
薬剤交付時:
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。(PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することが報告されている)
服用時:
カプセル中の粒をかみ砕いたり、カプセルを開けて服用しないよう患者に指導すること。(本剤は、タムスロシン塩酸塩の徐放性粒を充填した硬カプセルであるため、薬物動態が変わる可能性がある)
その他の注意
α1遮断薬を服用中又は過去に服用経験のある患者において、α1遮断作用によると考えられる術中虹彩緊張低下症候群(Intraoperative Floppy Iris Syndrome)があらわれるとの報告がある。
前立腺肥大症の診断・診療については、国内外のガイドライン等の最新の情報を参考にすること。
薬物動態
生物学的同等性試験1)
●タムスロシン塩酸塩カプセル0.1mg「武田テバ」
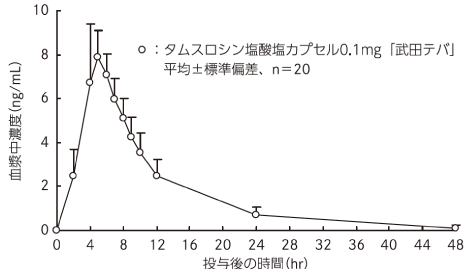
○絶食投与
タムスロシン塩酸塩カプセル0.1mg「武田テバ」と標準製剤を、クロスオーバー法によりそれぞれ2カプセル(タムスロシン塩酸塩として0.2mg)健康成人男子に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。
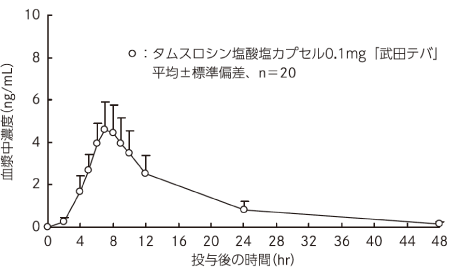
○食後投与
タムスロシン塩酸塩カプセル0.1mg「武田テバ」と標準製剤を、クロスオーバー法によりそれぞれ2カプセル(タムスロシン塩酸塩として0.2mg)健康成人男子に食後単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。
●タムスロシン塩酸塩カプセル0.2mg「武田テバ」
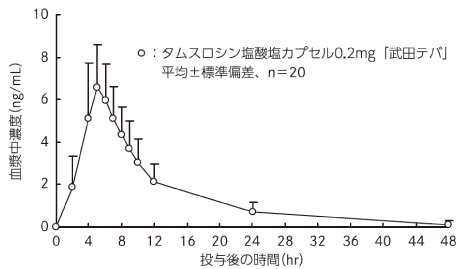
○絶食投与
タムスロシン塩酸塩カプセル0.2mg「武田テバ」と標準製剤を、クロスオーバー法によりそれぞれ1カプセル(タムスロシン塩酸塩として0.2mg)健康成人男子に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。
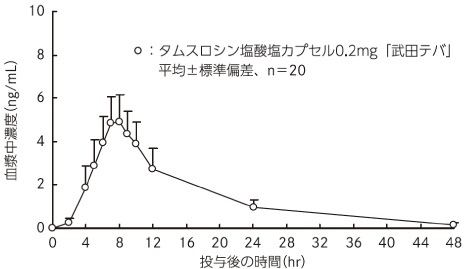
○食後投与
タムスロシン塩酸塩カプセル0.2mg「武田テバ」と標準製剤を、クロスオーバー法によりそれぞれ1カプセル(タムスロシン塩酸塩として0.2mg)健康成人男子に食後単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。
溶出性4)
タムスロシン塩酸塩カプセル0.1mg「武田テバ」及びタムスロシン塩酸塩カプセル0.2mg「武田テバ」の溶出性は、日本薬局方外医薬品規格第3部に定められた規格に適合していることが確認されている。
薬物動態の表
タムスロシン塩酸塩カプセル0.1mg「武田テバ」 絶食単回経口投与
薬物動態パラメータ (平均±標準偏差、n=20)
| | 投与量
(mg) | AUC0-48
(ng・hr/mL) | Cmax
(ng/mL) | Tmax
(hr) | T1/2
(hr) |
| タムスロシン塩酸塩カプセル0.1mg「武田テバ」 | 0.2 | 81.94±17.74 | 8.49±1.35 | 4.9±0.7 | 7.2±2.0 |
タムスロシン塩酸塩カプセル0.1mg「武田テバ」 食後単回経口投与
薬物動態パラメータ (平均±標準偏差、n=20)
| | 投与量
(mg) | AUC0-48
(ng・hr/mL) | Cmax
(ng/mL) | Tmax
(hr) | T1/2
(hr) |
| タムスロシン塩酸塩カプセル0.1mg「武田テバ」 | 0.2 | 61.87±19.28 | 4.77±1.36 | 7.4±0.7 | 8.1±2.0 |
タムスロシン塩酸塩カプセル0.2mg「武田テバ」 絶食単回経口投与
薬物動態パラメータ (平均±標準偏差、n=20)
| | 投与量
(mg) | AUC0-48
(ng・hr/mL) | Cmax
(ng/mL) | Tmax
(hr) | T1/2
(hr) |
| タムスロシン塩酸塩カプセル0.2mg「武田テバ」 | 0.2 | 71.04±26.61 | 6.92±2.29 | 5.1±0.8 | 7.8±2.4 |
タムスロシン塩酸塩カプセル0.2mg「武田テバ」 食後単回経口投与
薬物動態パラメータ (平均±標準偏差、n=20)
| | 投与量
(mg) | AUC0-48
(ng・hr/mL) | Cmax
(ng/mL) | Tmax
(hr) | T1/2
(hr) |
| タムスロシン塩酸塩カプセル0.2mg「武田テバ」 | 0.2 | 68.76±16.41 | 5.24±1.31 | 7.7±1.1 | 8.5±1.6 |
薬効薬理
アドレナリンα1-受容体の選択的遮断薬。α1-受容体刺激作用に拮抗するが、尿道平滑筋のα1-受容体遮断作用による尿道緊張緩和に基づく排尿困難改善作用が臨床的に利用される。2)
有効成分に関する理化学的知見
一般名
タムスロシン塩酸塩(Tamsulosin Hydrochloride)
化学名
5-{(2R)-2-[2-(2-Ethoxyphenoxy)ethylamino]propyl}-2-methoxybenzenesulfonamide monohydrochloride
分子式
C20H28N2O5S・HCl
分子量
444.97
融 点
約230℃(分解)
性 状
白色の結晶である。ギ酸に溶けやすく、水にやや溶けにくく、酢酸(100)に溶けにくく、エタノール(99.5)に極めて溶けにくい。
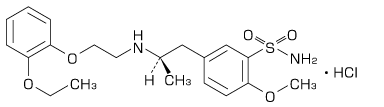
構造式
取扱い上の注意
安定性試験結果の概要3)
加速試験(40℃、相対湿度75%、6ヵ月)の結果、タムスロシン塩酸塩カプセル0.1mg「武田テバ」及びタムスロシン塩酸塩カプセル0.2mg「武田テバ」は通常の市場流通下において3年間安定であることが推測された。
包装
●タムスロシン塩酸塩カプセル0.1mg「武田テバ」
PTP包装:140カプセル(14カプセル×10)
●タムスロシン塩酸塩カプセル0.2mg「武田テバ」
PTP包装:140カプセル(14カプセル×10)
主要文献
1
武田テバファーマ(株)社内資料(生物学的同等性試験)
2
*第十七改正日本薬局方解説書
3
武田テバファーマ(株)社内資料(安定性試験)
4
武田テバファーマ(株)社内資料(溶出試験)
文献請求先・製品情報お問い合わせ先
主要文献欄に記載の文献・社内資料は下記にご請求下さい。
武田テバファーマ株式会社 武田テバDIセンター
〒453-0801 名古屋市中村区太閤一丁目24番11号
TEL 0120-923-093
受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
製造販売業者等の氏名又は名称及び住所
販売
武田薬品工業株式会社
大阪市中央区道修町四丁目1番1号
製造販売元
武田テバファーマ株式会社
名古屋市中村区太閤一丁目24番11号
 (全長 14.2mm)(重量 122.8mg)
(全長 14.2mm)(重量 122.8mg) (蓋部 5.3mm)(胴体部 5.1mm)
(蓋部 5.3mm)(胴体部 5.1mm) (全長 14.2mm)(重量 205.6mg)
(全長 14.2mm)(重量 205.6mg) (蓋部 5.3mm)(胴体部 5.1mm)
(蓋部 5.3mm)(胴体部 5.1mm)