作成又は改訂年月
*
2020年6月改訂
(第3版)
2019年12月改訂
(投薬期間制限医薬品に関する情報削除)
日本標準商品分類番号
日本標準商品分類番号等
薬効分類名
承認等
販売名
*モビコール配合内用剤LD

販売名コード
承認・許可番号
*30200AMX00472
*MOVICOL LD
薬価基準収載年月
*2020年11日
販売開始年月
貯法・使用期限等
貯法
室温保存(高温を避けて保存すること)
使用期限
外箱に表示の使用期限内に使用すること
規制区分
処方箋医薬品注)
注)注意−医師等の処方箋により使用すること
組成
本剤は、1包中に下記の成分を含有する。
本剤は経口液用製剤(散剤)で、白色の粉末である。
成分(1包(6.8523g)中)
マクロゴール4000 6.5625g
塩化ナトリウム 0.1754g
炭酸水素ナトリウム 0.0893g
塩化カリウム 0.0251g
禁忌
本剤の成分に対し過敏症の既往歴のある患者
腸閉塞、腸管穿孔、重症の炎症性腸疾患(潰瘍性大腸炎、クローン病、中毒性巨大結腸症等)が確認されている患者又はその疑いがある患者[病態を悪化させるおそれがある。]
効能又は効果
効能又は効果/用法及び用量
用法及び用量
本剤は、水で溶解して経口投与する。
通常、2歳以上7歳未満の幼児には初回用量として1回1包を1日1回経口投与する。以降、症状に応じて適宜増減し、1日1〜3回経口投与、最大投与量は1日量として4包まで(1回量として2包まで)とする。ただし、増量は2日以上の間隔をあけて行い、増量幅は1日量として1包までとする。
通常、7歳以上12歳未満の小児には初回用量として1回2包を1日1回経口投与する。以降、症状に応じて適宜増減し、1日1〜3回経口投与、最大投与量は1日量として4包まで(1回量として2包まで)とする。ただし、増量は2日以上の間隔をあけて行い、増量幅は1日量として1包までとする。
通常、成人及び12歳以上の小児には初回用量として1回2包を1日1回経口投与する。以降、症状に応じて適宜増減し、1日1〜3回経口投与、最大投与量は1日量として6包まで(1回量として4包まで)とする。ただし、増量は2日以上の間隔をあけて行い、増量幅は1日量として2包までとする。
用法及び用量に関連する使用上の注意
本剤投与中は腹痛や下痢があらわれるおそれがあるので、症状に応じて減量、休薬又は中止を考慮し、本剤を漫然と継続投与しないよう、定期的に本剤の投与継続の必要性を検討すること。
使用上の注意
副作用
副作用等発現状況の概要
承認時までの国内の臨床試験では192例中33例(17.2%)に副作用が認められている。主な副作用は下痢7例(3.6%)、腹痛7例(3.6%)であった。
重大な副作用
ショック、アナフィラキシー
(頻度不明)
ショック、アナフィラキシーがあらわれることがあるので、観察を十分に行い、血圧低下、蕁麻疹、呼吸困難、顔面浮腫等の異常が認められた場合には投与を中止し、適切な処置を行うこと。
その他の副作用
以下のような副作用が認められた場合には症状に応じて、適切な処置を行うこと。
過敏症注)
1〜5%未満
発疹
過敏症注)
1%未満
紅斑
過敏症注)
頻度不明
血管浮腫、蕁麻疹、そう痒症
精神神経系
頻度不明
頭痛
消化器
1〜5%未満
下痢、腹痛、腹部膨満、悪心、腹部不快感、下腹部痛、裂肛、胃腸音異常
消化器
頻度不明
嘔吐、消化不良、鼓腸、肛門直腸不快感
その他
1%未満
末梢性浮腫
その他
頻度不明
高カリウム血症、低カリウム血症
その他の副作用の注意
注):このような症状が発現した場合には、投与を中止すること。
高齢者への投与
一般に高齢者では生理機能が低下しているので、減量するなど注意すること。
妊婦、産婦、授乳婦等への投与
妊婦又は妊娠している可能性のある婦人には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。[妊娠中の投与に関する安全性は確立していない。]
授乳中の投与は、治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
小児等への投与
低出生体重児、新生児、乳児、2歳未満の幼児に対する安全性は確立していない(使用経験がない)。
過量投与
過量投与により、下痢又は嘔吐による過度の体液喪失が生じた際には、水分摂取、電解質補正等の適切な処置を行うこと。
適用上の注意
調製方法
本品1包あたりコップ1/3程度(約60mL)の水に溶解する。溶解後は速やかに服用すること。
保存時
やむを得ず保存する必要がある場合は、冷蔵庫に保存し、できるかぎり速やかに服用すること。
薬物動態
マクロゴール4000は経口投与時にほとんど吸収されず1)2)、ウサギでは代謝や腸内細菌で分解されない3)。
臨床成績
成人国内第III相試験(検証期:プラセボ対照試験)
自発排便回数が平均3回/週未満の状態が6ヵ月以上持続している15歳以上の慢性便秘症の患者156例を対象に、プラセボ又は本剤を排便状況により1日2〜6包を2週間経口投与したとき、主要評価項目である「検証期第2週の自発排便回数の観察期間第2週からの変化量」は表1のとおりであり、本剤のプラセボに対する優越性が検証された4)。
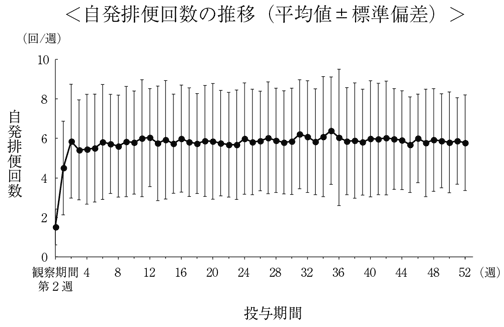
成人国内第III相試験(継続期:長期投与試験)
15歳以上の慢性便秘症の患者153例を対象に、本剤1日2〜6包を52週間経口投与したときの、52週までの7日あたりの自発排便回数の推移は下図のとおりであった
4)。
*小児国内第III相試験
自発排便回数が平均2回/週以下の状態が2ヵ月以上持続している2歳以上14歳以下の慢性便秘症の患者39例を対象に、排便状況により2歳以上11歳以下:1日1〜4包、12歳以上14歳以下:1日2〜6包を12週間経口投与した。
主要評価項目である「投与期間第2週の自発排便回数の観察期間第2週からの変化量」は表2のとおりであった5)。
| 投与群 | 自発排便回数(回)
観察期間
第2週 | 自発排便回数(回)
検証期
第2週 | 変化量 | 変化量の群間差注1)
[95%信頼区間] | P値注1)2) |
| プラセボ群 | 1.39±0.87
(76例) | 3.07±2.16
(73例) | 1.64±2.00
(73例) | 2.66
[1.86, 3.45] | P<0.0001 |
| 本剤群 | 1.60±0.94
(80例) | 5.85±2.87
(80例) | 4.25±2.93
(80例) | 2.66
[1.86, 3.45] | P<0.0001 |
| 投与群 | 自発排便回数(回)
観察期間第2週 | 自発排便回数(回)
投与期間第2週 | 変化量 |
| 本剤群 | 1.00±0.89
(39例) | 6.54±4.38
(39例) | 5.54±4.55 |
薬効薬理
本剤はマクロゴール4000及び電解質を配合した製剤であり、主にマクロゴール4000の物理化学的性質により、高い浸透圧効果を有し6)、消化管内に水分を保持することで、用量依存的に便の排出を促進する7)。
有効成分に関する理化学的知見
一般名
マクロゴール4000(JAN)
Macrogol 4000(JAN)
(ポリエチレングリコール4000)
化学名
Poly(oxy-1,2-ethanediyl)
化学式
HOCH2(CH2OCH2)nCH2OH
(n:59〜84)
分子量
2600〜3800
凝固点
53〜57℃
性状
本品は白色のパラフィン様の塊、薄片又は粉末で、においはないか、又は僅かに特異なにおいがある。本品は水に極めて溶けやすく、メタノール又はピリジンに溶けやすく、エタノール(99.5)又はジエチルエーテルにほとんど溶けない。
承認条件
医薬品リスク管理計画を策定の上、適切に実施すること。
包装
主要文献及び文献請求先
主要文献
1
Brady CE 3rd., et al.:Gastroenterology 1986;90(6):1914-8
2
DiPiro JT., et al.:Clin. Pharm. 1986;5(2):153-5
3
Seidman EG., et al.:Gastroenterology 1986;90(1):120-6
4
社内資料(成人国内第III相試験)
5
社内資料(小児国内第III相試験)
6
Schiller LR., et al.:Gastroenterology 1988;94(4):933-41
7
Hammer HF., et al.:J. Clin. Invest. 1989;84(4):1056-62
文献請求先
主要文献に記載の社内資料につきましても下記にご請求ください。
EAファーマ株式会社
くすり相談室
〒104-0042 東京都中央区入船二丁目1番1号
フリーダイヤル 0120-917-719
製造販売業者等の氏名又は名称及び住所
製造販売元
EAファーマ株式会社
東京都中央区入船二丁目1番1号
プロモーション提携
エーザイ株式会社
東京都文京区小石川4-6-10