作成又は改訂年月
日本標準商品分類番号
薬効分類名
承認等
販売名
スクラルファート顆粒90%「日医工」
販売名コード
承認・許可番号
22500AMX01356000
Sucralfate
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
室温保存
使用期限
外箱等に表示の使用期限内に使用すること
組成
有効成分
スクラルファート水和物
含量
1g中 900mg
添加物
カルメロース,メチルセルロース,ハッカ油
製剤の性状
一般的名称
禁忌
透析療法を受けている患者[長期投与によりアルミニウム脳症,アルミニウム骨症,貧血等があらわれることがある。]
効能又は効果
○胃潰瘍,十二指腸潰瘍
○下記疾患の胃粘膜病変(びらん,出血,発赤,浮腫)の改善
急性胃炎,慢性胃炎の急性増悪期
用法及び用量
通常,成人1回1〜1.2gずつ,1日3回経口投与する。
なお,年令・症状により適宜増減する。
使用上の注意
慎重投与
腎障害のある患者[長期投与によりアルミニウム脳症,アルミニウム骨症,貧血等があらわれるおそれがあるので,定期的に血中アルミニウム,リン,カルシウム,アルカリフォスファターゼ等の測定を行うこと。]
リン酸塩の欠乏している患者[アルミニウムは消化管内でリン酸塩と結合し,その吸収を阻害する。]
相互作用
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
クエン酸製剤
クエン酸カリウム,
クエン酸ナトリウム水和物等 | 血中アルミニウム濃度が上昇することがあるので,同時に服用させないなど注意すること。 | キレートを形成し,アルミニウムの吸収が促進されると考えられる。 |
血清カリウム抑制イオン交換樹脂
ポリスチレンスルホン酸カルシウム,
ポリスチレンスルホン酸ナトリウム | 血清カリウム抑制イオン交換樹脂の効果が減弱するおそれがある。 | アルミニウムイオンと非選択的に交換すると考えられる。 |
ニューキノロン系抗菌剤
ノルフロキサシン,
塩酸シプロフロキサシン等 | 同時に服用することにより,これら併用薬剤の吸収を遅延又は阻害するおそれがある。この相互作用は併用薬を本剤の2時間以上前に服用することにより,弱まるとの報告がある。 | アルミニウムイオンと併用薬剤が不溶性のキレートを形成し,消化管からの吸収を遅延又は阻害する。 |
ジギタリス製剤
ジゴキシン等
フェニトイン
テトラサイクリン系抗生物質
スルピリド等 | 同時に服用することにより,これら併用薬剤の吸収を遅延又は阻害するおそれがある。この作用は薬剤の服用時間をずらすことにより,弱まるとの報告がある。 | 本剤が併用薬剤を吸着し,消化管からの吸収を遅延又は阻害する。 |
甲状腺ホルモン剤
レボチロキシンナトリウム水和物等 | 同時に服用することにより,これら併用薬剤の吸収を遅延又は阻害することがある。これらの作用は薬剤の服用時間をずらすことにより,弱まると考えられる。 | 消化管内で本剤と吸着することにより,これらの薬剤の吸収が阻害される。 |
胆汁酸製剤
ウルソデオキシコール酸,
ケノデオキシコール酸 | 同時に服用することにより,これら併用薬剤の吸収を遅延又は阻害することがある。これらの作用は薬剤の服用時間をずらすことにより,弱まると考えられる。 | 消化管内で本剤と吸着することにより,これらの薬剤の吸収が阻害される。 |
| テオフィリン徐放性製剤 | 同時に服用することにより,テオフィリン徐放性製剤のAUCが低下するおそれがある。 | 本剤がテオフィリン徐放性製剤の吸収を阻害するとの報告がある。 |
| キニジン等 | 制酸剤(乾燥水酸化アルミニウムゲル等)の投与により,併用薬剤の排泄が遅延することが知られている。 | 制酸剤による尿のpH上昇による。 |
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
以下のような副作用が認められた場合には,減量・休薬など適切な処置を行うこと。
消化器(頻度不明)
便秘,口渇,悪心,嘔気等
皮膚(頻度不明)
発疹,蕁麻疹等
過敏症(頻度不明)
アナフィラキシー反応
長期投与
長期投与によりアルミニウム脳症,アルミニウム骨症,貧血等があらわれるおそれがあるので,慎重に投与すること。
高齢者への投与
一般に高齢者では生理機能が低下しているので用量に注意すること。
その他の注意
経管栄養処置を受けている成人患者,低出生体重児及び新生児発育不全において,胃石・食道結石がみられたとの報告があるので,観察を十分に行い,これらが疑われた場合には本剤の投与を中止し,適切な処置を行うこと。
有効成分に関する理化学的知見
一般名
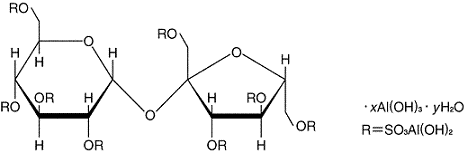
スクラルファート水和物(Sucralfate Hydrate)
分子式
C12H30Al8O51S8・xAl(OH)3・yH2O
性状
白色の粉末で,におい及び味はない。
水,熱湯,エタノール(95)又はジエチルエーテルにほとんど溶けない。
本品は希塩酸又は硫酸・水酸化ナトリウム試液に溶ける。
取扱い上の注意
安定性試験
本品につき加速試験(40℃,相対湿度75%,6ヵ月)を行った結果,スクラルファート顆粒90%「日医工」は通常の市場流通下において3年間安定であることが推測された。1)
包装
スクラルファート顆粒90%「日医工」
1g×1200包
100g(バラ)
1kg(バラ)
主要文献及び文献請求先
主要文献
文献請求先
主要文献欄に記載の文献・社内資料は下記にご請求下さい。
日医工株式会社 お客様サポートセンター
〒930-8583 富山市総曲輪1丁目6番21
フリーダイアル(0120)517-215
Fax(076)442-8948
製造販売業者等の氏名又は名称及び住所
製造販売元
日医工株式会社
富山市総曲輪1丁目6番21