1
阿部真也 他:周産期医学.2017;47:1353-1355
2
齊藤大祐 他:鹿児島産科婦人科学会雑誌.2021;29:49-54
3
Naito T.et al.:J Hum Lact.2015;31:301-306
4
第十八改正日本薬局方解説書.東京:廣川書店;2021.C1455-1461
5
社内資料:生物学的同等性試験(配合錠LD)
6
社内資料:生物学的同等性試験(配合錠HD)
7
第十八改正日本薬局方解説書.東京:廣川書店;2021.C306-311
持続性アンジオテンシンⅡ受容体拮抗薬/持続性Ca拮抗薬配合剤
1錠 29.8円
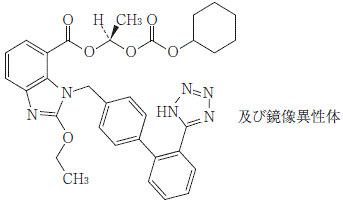
有効成分 | 1錠中 日本薬局方カンデサルタン シレキセチル 8mg |
|---|---|
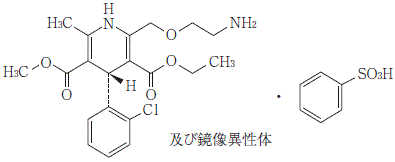
有効成分 | 日本薬局方アムロジピンべシル酸塩 3.47mg アムロジピンとして 2.5mg |
添加剤 | エリスリトール、結晶セルロース、トウモロコシデンプン、クロスカルメロースナトリウム、クエン酸トリエチル、エデト酸ナトリウム水和物、ヒドロキシプロピルセルロース、ステアリン酸マグネシウム、黄色4号(タートラジン)、赤色102号 |
有効成分 | 1錠中 日本薬局方カンデサルタン シレキセチル 8mg |
|---|---|
有効成分 | 日本薬局方アムロジピンべシル酸塩 6.93mg アムロジピンとして 5mg |
添加剤 | エリスリトール、結晶セルロース、トウモロコシデンプン、クロスカルメロースナトリウム、クエン酸トリエチル、エデト酸ナトリウム水和物、ヒドロキシプロピルセルロース、ステアリン酸マグネシウム、黄色4号(タートラジン)、赤色102号、赤色2号 |
| 外形 |  |
|---|---|
| 大きさ | 大きさ(長径) 8.6mm 大きさ(短径) 5.0mm 錠厚 3.0mm 重量 130mg |
| 性状 | 淡黄色の素錠 |
| 本体表示 | カムシアLD 日新 |
| 外形 |  |
|---|---|
| 大きさ | 大きさ(長径) 8.6mm 大きさ(短径) 5.0mm 錠厚 3.0mm 重量 130mg |
| 性状 | 淡赤色の素錠 |
| 本体表示 | カムシアHD 日新 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
アリスキレンフマル酸塩 ラジレス (糖尿病患者に使用する場合。ただし、他の降圧治療を行ってもなお血圧のコントロールが著しく不良の患者を除く。) | 非致死性脳卒中、腎機能障害、高カリウム血症及び低血圧のリスク増加が報告されている。 | レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
降圧作用を有する他の薬剤 β-遮断剤 ニトログリセリン シルデナフィル等 | 降圧作用が増強するおそれがある。用量調節等に注意すること。 | 作用機序の異なる降圧作用により互いに協力的に作用する。 |
カリウム保持性利尿剤 スピロノラクトン トリアムテレン等 エプレレノン カリウム補給剤 | 血清カリウム値が上昇することがある。 | カンデサルタン シレキセチルのアルドステロン分泌抑制作用によりカリウム貯留作用が増強することによる。 危険因子:特に腎機能障害のある患者 |
利尿剤 フロセミド トリクロルメチアジド等 | 利尿剤で治療を受けている患者に本剤を初めて投与する場合、降圧作用が増強するおそれがあるので、慎重に投与すること。 | 利尿剤で治療を受けている患者にはレニン活性が亢進している患者が多く、カンデサルタン シレキセチルが奏効しやすい。 危険因子:特に最近利尿剤投与を開始した患者 |
アリスキレンフマル酸塩 | 腎機能障害、高カリウム血症及び低血圧を起こすおそれがある。eGFRが60mL/min/1.73m2未満の腎機能障害のある患者へのアリスキレンフマル酸塩との併用については、治療上やむを得ないと判断される場合を除き避けること。 | レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
アンジオテンシン変換酵素阻害剤 | 腎機能障害、高カリウム血症及び低血圧を起こすおそれがある。 | レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
炭酸リチウム | カンデサルタン シレキセチルとの併用において、リチウム中毒が報告されている。 | カンデサルタン シレキセチルにより腎尿細管におけるリチウムの再吸収が促進される。 |
非ステロイド性消炎鎮痛剤(NSAIDs) インドメタシン等 | 降圧作用が減弱することがある。 | 非ステロイド性消炎鎮痛剤は血管拡張作用を有するプロスタグランジンの合成を阻害することから、降圧作用を減弱させる可能性があると考えられている。 |
非ステロイド性消炎鎮痛剤(NSAIDs) インドメタシン等 | 腎障害のある患者では、さらに腎機能が悪化するおそれがある。 | 非ステロイド性消炎鎮痛剤のプロスタグランジン合成阻害作用により、腎血流量が低下するためと考えられている。 |
CYP3A4阻害剤 エリスロマイシン ジルチアゼム リトナビル イトラコナゾール等 | アムロジピンの血中濃度が上昇するおそれがある。 エリスロマイシン又はジルチアゼムとの併用により、アムロジピンの血中濃度が上昇したとの報告がある。 | アムロジピンの代謝が競合的に阻害される可能性が考えられる。 |
CYP3A4誘導剤 リファンピシン等 | アムロジピンの血中濃度が低下するおそれがある。 | アムロジピンの代謝が促進される可能性が考えられる。 |
グレープフルーツジュース | 降圧作用が増強されるおそれがある。 | グレープフルーツに含まれる成分がアムロジピンの代謝を阻害し、アムロジピンの血中濃度が上昇する可能性が考えられる。 |
シンバスタチン | アムロジピンベシル酸塩とシンバスタチン80mg(国内未承認の高用量)との併用により、シンバスタチンのAUCが77%上昇したとの報告がある。 | 機序は不明である。 |
タクロリムス | アムロジピンベシル酸塩との併用によりタクロリムスの血中濃度が上昇し、腎障害等のタクロリムスの副作用が発現するおそれがある。併用時にはタクロリムスの血中濃度をモニターし、必要に応じてタクロリムスの用量を調整すること。 | アムロジピンとタクロリムスは、主としてCYP3A4により代謝されるため、併用によりタクロリムスの代謝が阻害される可能性が考えられる。 |
0.1~5%未満 | 頻度不明 | |
|---|---|---|
過敏症 | 湿疹、発疹、蕁麻疹、そう痒、光線過敏症、多形紅斑、血管炎 | |
循環器 | めまい注)、ほてり(熱感、顔面紅潮等)、血圧低下 | 動悸、徐脈、頻脈、ふらつき注)、立ちくらみ注)、胸痛、期外収縮、心房細動、洞房ブロック、洞停止 |
精神神経系 | 頭痛、眠気、舌のしびれ感、頭重感、不眠、四肢のしびれ感、気分動揺、末梢神経障害、振戦、錐体外路症状 | |
消化器 | 胃部不快感、腹部膨満、下痢 | 悪心、食欲不振、口渇、嘔吐、心窩部痛、便秘、軟便、排便回数増加、口内炎、味覚異常、消化不良、胃腸炎、膵炎 |
肝臓 | ALT、γ-GTPの上昇 | AST、Al-P、LDHの上昇、腹水 |
血液 | 白血球増多、好酸球増多 | 貧血、白血球減少、赤血球減少、紫斑 |
腎臓 | BUNの上昇 | クレアチニンの上昇、蛋白尿 |
その他 | 咳、耳鳴、血中CK上昇、血中尿酸上昇、尿管結石 | 血中カリウム上昇、血中カリウム減少、筋肉痛、倦怠感、脱力感、疲労、鼻出血、頻尿、夜間頻尿、尿潜血陽性、浮腫、総コレステロール上昇、CRP上昇、血清総タンパク減少、低ナトリウム血症、腰背部痛、関節痛、筋痙攣、筋緊張亢進、勃起障害、排尿障害、(連用により)歯肉肥厚、女性化乳房、脱毛、多汗、鼻炎、体重増加、体重減少、疼痛、皮膚変色、発熱、視力異常、呼吸困難、異常感覚、高血糖、糖尿病、尿中ブドウ糖陽性 |
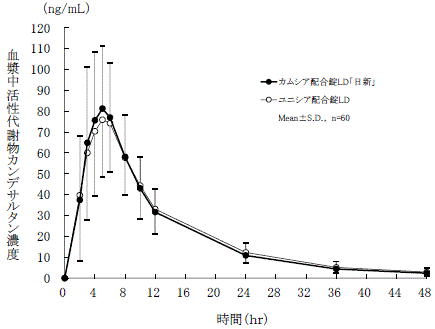
判定パラメータ | 参考パラメータ | |||
AUC0-48 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
カムシア配合錠 LD「日新」 | 1061.1±283.5 | 88.5±31.2 | 4.8±1.2 | 10.9±5.1 |
ユニシア配合錠LD | 1041.3±277.5 | 81.3±28.2 | 5.0±1.1 | 10.8±4.3 |
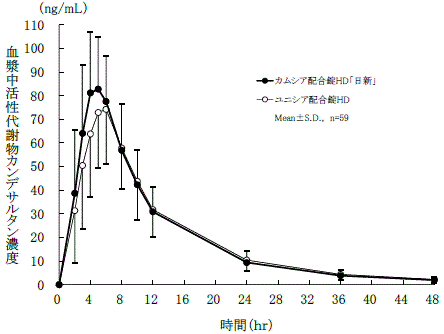
判定パラメータ | 参考パラメータ | |||
AUC0-48 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
カムシア配合錠 HD「日新」 | 987.6±223.4 | 92.0±23.5 | 4.6±1.3 | 10.6±3.6 |
ユニシア配合錠HD | 961.8±233.1 | 81.5±25.2 | 5.3±1.4 | 10.9±4.2 |
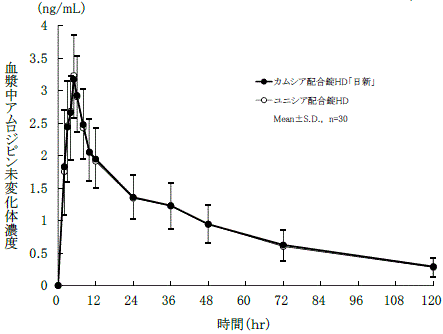
判定パラメータ | 参考パラメータ | |||
AUC0-120 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
カムシア配合錠 HD「日新」 | 115.5±32.8 | 3.25±0.68 | 4.8±0.8 | 41.4±8.0 |
ユニシア配合錠HD | 113.9±31.1 | 3.26±0.61 | 4.9±0.6 | 40.5±7.1 |