作成又は改訂年月
**
2020年12月改訂
(第10版)
*
2015年8月改訂
日本標準商品分類番号
薬効分類名
承認等
販売名
**エペリゾン塩酸塩錠50mg「KO」
販売名コード
承認・許可番号
**30200AMX00545000
**Eperisone Hydrochloride Tablets 50mg「KO」
薬価基準収載年月
販売開始年月
貯法・使用期限等
規制区分
処方箋医薬品
注意-医師等の処方箋により使用すること
組成
成分・含量
1錠中 日局 エペリゾン塩酸塩50mg
添加物
リン酸二水素Ca、クエン酸Ca、ヒドロキシプロピルセルロース、ステアリン酸Mg、ステアリン酸、アミノアルキルメタアクリレートコポリマーE、タルク
性状
| 剤型 | 白色のフィルムコート錠 |
|---|
| 外形 |  |
|---|
| 直径(mm) | 7.1 |
|---|
| 厚さ(mm) | 3.4 |
|---|
| 重量(mg) | 126 |
|---|
| 識別コード | KTB-21 |
|---|
一般的名称
禁忌
効能・効果
下記疾患による筋緊張状態の改善
頸肩腕症候群、肩関節周囲炎、腰痛症
下記疾患による痙性麻痺
脳血管障害、痙性脊髄麻痺、頸部脊椎症、術後後遺症(脳・脊髄腫瘍を含む)、外傷後遺症(脊髄損傷、頭部外傷)、筋萎縮性側索硬化症、脳性小児麻痺、脊髄小脳変性症、脊髄血管障害、スモン(SMON)、その他の脳脊髄疾患
用法・用量
通常、成人には1日量として3錠(エペリゾン塩酸塩として150mg)を3回に分けて食後に経口投与する。
なお、年齢、症状により適宜増減する。
使用上の注意
慎重投与
薬物過敏症の既往歴のある患者
肝障害のある患者〔肝機能を悪化させることがある。〕
重要な基本的注意
本剤投与中に脱力感、ふらつき、眠気等が発現することがあるので、その場合には減量又は休薬すること。なお、本剤投与中の患者には自動車の運転など危険を伴う機械の操作には従事させないように注意すること。
相互作用
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|
| メトカルバモール | 類似薬のトルペリゾン塩酸塩で、眼の調節障害があらわれたとの報告がある。 | 機序不明 |
|---|
副作用
副作用等発現状況の概要
本剤は、使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用(頻度不明)
ショック、アナフィラキシー
ショック、アナフィラキシーを起こすことがあるので、観察を十分に行い、発赤、そう痒感、蕁麻疹、顔面等の浮腫、呼吸困難等の異常が認められた場合には投与を中止し、適切な処置を行うこと。
中毒性表皮壊死融解症(Toxic Epidermal Necrolysis : TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、
中毒性表皮壊死融解症、皮膚粘膜眼症候群等の重篤な皮膚障害を起こすことがあるので、観察を十分に行い、発熱、紅斑、水疱、そう痒感、眼充血、口内炎等の症状が認められた場合には投与を中止し、適切な処置を行うこと。
その他の副作用
肝臓注1)
頻度不明
AST(GOT)、ALT(GPT)、Al-Pの上昇等
腎臓注1)
頻度不明
蛋白尿、BUNの上昇等
血液注1)
頻度不明
貧血
過敏症注2)
頻度不明
発疹、そう痒、多形滲出性紅斑
精神神経系
頻度不明
眠気、不眠、頭痛、四肢のしびれ、体のこわばり、四肢のふるえ
消化器
頻度不明
悪心・嘔吐、食欲不振、胃部不快感、腹痛、下痢、便秘、口渇、口内炎、腹部膨満感
泌尿器
頻度不明
尿閉、尿失禁、残尿感
全身症状
頻度不明
脱力感、ふらつき、全身倦怠感、筋緊張低下、めまい
その他
頻度不明
ほてり、発汗、浮腫、動悸、しゃっくり
注1)このような症状があらわれることがあるので、観察を十分に行い、異常が認められた場合には、投与を中止するなど適切な処置を行うこと。
注2)このような症状があらわれた場合には、投与を中止すること。
高齢者への投与
一般に高齢者では生理機能が低下しているので減量するなど注意すること。
妊婦、産婦、授乳婦等への投与
妊婦
妊婦又は妊娠している可能性のある婦人には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。〔妊娠中の投与に関する安全性は確立していない。〕
授乳婦
授乳中の婦人に投与することは避けることが望ましいが、やむを得ず投与する場合には、授乳を避けさせること。〔動物実験(ラット)で乳汁中へ移行することが報告されている。〕
小児等への投与
低出生体重児、新生児、乳児、幼児又は小児に対する安全性は確立していない(使用経験が少ない)。
適用上の注意
薬剤交付時
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。〔PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告されている。〕
薬物動態
**生物学的同等性試験1)
エペリゾン塩酸塩錠50mg「KO」と標準製剤を、クロスオーバー法によりそれぞれ1錠(エペリゾン塩酸塩50mg)健康成人男子に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUCt、Cmax)について統計解析を行った結果、両剤の生物学的同等性が確認された。
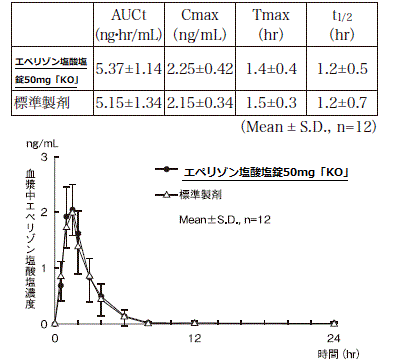
血漿中濃度並びにAUCt、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
**溶出挙動2)
エペリゾン塩酸塩錠50mg「KO」は、日本薬局方外医薬品規格第3部に定められたエペリゾン塩酸塩の溶出規格に適合していることが確認されている。
**薬効薬理
脊髄において単及び多シナプス反射を抑制するとともに、γ-運動ニューロンの自発発射を減少させ、筋紡錘の感度を低下させることで、メフェネシンよりも強力な骨格筋弛緩作用を発揮する。また、中脳毛様体及び後部視床下部を介する脳波覚醒反応を抑制する作用や、血管平滑筋のCa2+チャネル遮断や交感神経活動の抑制を介して、皮膚・筋や脳への血流量を増大させる作用もある。脊髄レベルにおける鎮痛作用も有する。3)
有効成分に関する理化学的知見
一般名
エペリゾン塩酸塩(Eperisone Hydrochloride)
化学名
(2RS)-1-(4-Ethylphenyl)-2-methyl-3-piperidin-1-ylpropan-1-one monohydrochloride
分子式
C17H25NO・HCl
分子量
295.85
構造式
融点
約167℃(分解)
性状
本品は白色の結晶性の粉末である。
本品は水、メタノール又は酢酸(100)に溶けやすく、エタノール(99.5)にやや溶けやすい。
本品のメタノール溶液(1→100)は旋光性を示さない。
**取扱い 上の注意
安定性試験4)
最終包装製品を用いた加速試験(40℃、相対湿度75%、6ヵ月)の結果、エペリゾン塩酸塩錠50mg「KO」は通常の市場流通下において3年間安定であることが推測された。
**包装
エペリゾン塩酸塩錠50mg「KO」:
100錠(10錠(PTP)×10)
1,000錠(10錠(PTP)×100)
主要文献及び文献請求先
**主要文献
1
エペリゾン塩酸塩錠50mg「KO」と標準製剤との生物学的同等性試験(寿製薬株式会社社内資料)
2
エペリゾン塩酸塩錠 50mg「KO」の溶出挙動(寿製薬株式会社社内資料)
3
第十七改正日本薬局方解説書.東京:廣川書店;2016.C-986-989.
4
エペリゾン塩酸塩錠 50mg「KO」の安定性試験(寿製薬株式会社社内資料)
** *文献請求先
主要文献に記載の社内資料につきましても下記 にご請求下さい。
寿製薬株式会社 くすり相談窓口
〒389-0606 長野県埴科郡坂城町大字上五明字東川原198
TEL:0120-996-156
FAX:0268-82-2215
製造販売業者等の氏名又は名称及び住所
製造販売元
寿製薬株式会社
長野県埴科郡坂城町大字上五明字東川原198