1
Freudenthaler S,et al.:Br J Clin Pharmacol.1998;46(6):541-546
2
健康成人男性における単回経口投与時の薬物動態の検討(メマリー錠:2011年1月21日承認、申請資料概要2.7.6.4)
3
大和田 康子ほか:新薬と臨床.2014;63(3):374-378
4
アルツハイマー型認知症患者における反復経口投与時の薬物動態の検討(メマリー錠:2011年1月21日承認、申請資料概要2.7.6.7)
5
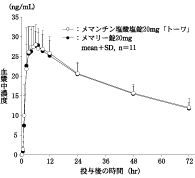
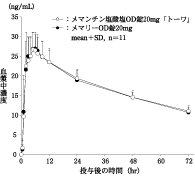
社内資料:生物学的同等性試験(錠20mg)
6
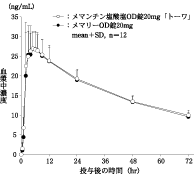
社内資料:生物学的同等性試験(OD錠20mg)
7
ラットにおける14C-標識体を用いた臓器への分布(メマリー錠:2011年1月21日承認、申請資料概要2.6.4.4)
8
ラットにおける14C-標識体を用いた脳内濃度(メマリー錠:2011年1月21日承認、申請資料概要2.6.4.4)
9
ウサギにおける14C-標識体を用いた胎盤胎児移行性(メマリー錠:2011年1月21日承認、申請資料概要2.6.4.4)
10
ラットにおける14C-標識体を用いた乳汁中への移行(メマリー錠:2011年1月21日承認、申請資料概要2.6.4.6)
11
高齢者における尿中排泄物(メマリー錠:2011年1月21日承認、申請資料概要2.7.2.2)
12
酵素による代謝と酵素阻害(メマリー錠:2011年1月21日承認、申請資料概要2.7.2.2)
13
外国人における排泄率(メマリー錠:2011年1月21日承認、申請資料概要2.7.1.2)
14
腎機能障害患者における薬物動態の検討(メマリー錠:2011年1月21日承認、申請資料概要2.7.6.8)
15
メマンチン塩酸塩とヒドロクロロチアジド・トリアムテレン配合剤との薬物動態学的相互作用の検討(メマリー錠:2011年1月21日承認、申請資料概要2.7.6.16)
16
社内資料:生物学的同等性試験(錠5mg)
17
社内資料:生物学的同等性試験(錠10mg)
18
社内資料:生物学的同等性試験(OD錠5mg)
19
社内資料:生物学的同等性試験(OD錠10mg)
20
北村 伸ほか:老年精神医学雑誌.2011;22(4):453-463
21
国内第Ⅱ相試験における副作用(メマリー錠:2011年1月21日承認、申請資料概要2.7.6.19)
22
中村 祐ほか:老年精神医学雑誌.2011;22(4):464-473
23
国内第Ⅲ相試験における副作用(メマリー錠:2011年1月21日承認、申請資料概要2.7.6.20)
24
Tariot PN,et al.:JAMA.2004;291(3):317-324
25
海外第Ⅲ相試験における副作用(メマリー錠:2011年1月21日承認、申請資料概要2.7.6.25)
26
中村 祐ほか:Geriat Med.2016;54(11):1147-1158
27
メマンチン塩酸塩のドネペジル塩酸塩併用時における中等度及び高度アルツハイマー型認知症に対する製造販売後臨床試験(メマリー錠:2020年9月23日、再審査報告書)
28
薬理試験の考察及び結論(メマリー錠:2011年1月21日承認、申請資料概要2.6.2.6)
29
NMDA受容体チャネル親和性の検討(メマリー錠:2011年1月21日承認、申請資料概要2.6.2.2)
30
Parsons CG,et al.:Neuropharmacology.1993;32(12):1337-1350
31
Frankiewicz T,et al.:Br J Pharmacol.1996;117(4):689-697
32
Nakamura S,et al.:Eur J Pharmacol.2006;548(1-3):115-122
33
Zajaczkowski W,et al.:Neuropharmacology.1997;36(7):961-971
34
Misztal M,et al.:Behav Pharmacol.1995;6:550-561




















 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379

