1
生殖発生毒性試験(リリカカプセル:2010年4月16日承認、CTD2.6.6.6)(L20210119)
2
幼若動物を用いた毒性試験(リリカカプセル:2010年4月16日承認、CTD2.6.6.6)(L20210119)
3
がん原性試験(リリカカプセル:2010年4月16日承認、CTD2.6.6.5)(L20210120)
4
健康成人における薬物動態(単回投与)(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.1.1)(L20210121)
5
健康成人における薬物動態(反復投与)(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.1.1)(L20210121)
6
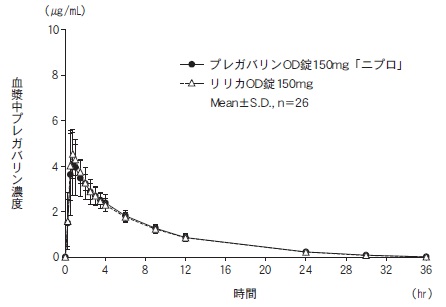
社内資料:生物学的同等性試験(OD錠150mg、水あり投与)
7
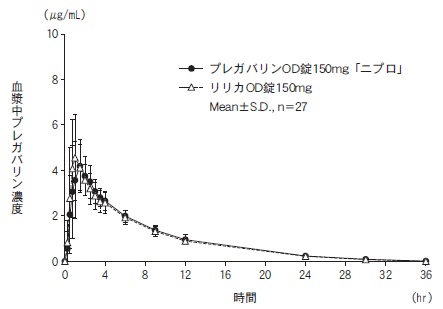
社内資料:生物学的同等性試験(OD錠150mg、水なし投与)
8
食事の影響(リリカカプセル:2010年4月16日承認、CTD2.7.1.2.2)(L20210122)
9
放射性標識体投与時の薬物動態及び代謝(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.1.6)(L20210123)
10
血漿蛋白結合(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.1.5)(L20210124)
11
代謝及び排泄(リリカカプセル:2010年4月16日承認、CTD2.7.6.1)(L20230629)
12
ヒトcytochrome P450に対する阻害作用(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.1.3)(L20210125)
13
高齢者における薬物動態(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.2.1)(L20210126)
14
腎機能障害患者及び血液透析患者における薬物動態(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.2)(L20210127)
15
健康被験者、帯状疱疹後神経痛患者、糖尿病性末梢神経障害に伴う疼痛を有する患者及び線維筋痛症患者における母集団薬物動態(リリカカプセル:2010年10月27日承認、CTD2.7.2.3.5.1、2012年6月22日承認、CTD2.7.2.3.1、2.7.2.3.4)(L20230676)
16
Lockwood PA, et al.:J. Hum. Lact. 2016;32(3):NP1-NP8(L20230630)
17
薬物動態に関する薬物相互作用(リリカカプセル:2010年4月16日承認、CTD2.7.2.3)(L20230631)
18
ガバペンチンとの薬物相互作用(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.3.5)(L20210131)
19
経口避妊薬との薬物相互作用(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.3.6)(L20210132)
20
薬物相互作用(リリカカプセル:2010年4月16日承認、審査報告書)(L20230632)
21
ロラゼパムとの薬物相互作用(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.4.1)(L20210133)
22
オキシコドンとの薬物相互作用(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.4.2)(L20210134)
23
エタノールとの薬物相互作用(リリカカプセル:2010年4月16日承認、CTD2.7.2.2.2.4.3)(L20210135)
24
Brodie MJ, et al.:Epilepsia. 2005;46(9):1407-1413(L20210136)
25
社内資料:生物学的同等性試験(OD錠25mg)
26
社内資料:生物学的同等性試験(OD錠75mg)
27
小川節郎ほか:日本ペインクリニック学会誌. 2010;17(2):141-152(L20210137)
28
国内第Ⅲ相検証試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.6.29)(L20230633)
29
国内第Ⅲ相検証試験(糖尿病性末梢神経障害に伴う疼痛)(リリカカプセル:2010年10月27日承認、CTD2.7.3.3、2.7.6.1)(L20210138)
30
国内第Ⅲ相検証試験(線維筋痛症)(リリカカプセル:2012年6月22日承認、CTD2.7.3.3、2.7.6.(2))(L20210139)
31
国内長期投与試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.3.5.1、2.7.6.37)(L20210140)
32
国内長期投与試験(糖尿病性末梢神経障害に伴う疼痛)(リリカカプセル:2010年10月27日承認、CTD2.7.3.5.2、2.7.6.24)(L20210141)
33
国内長期投与試験(線維筋痛症)(リリカカプセル:2012年6月22日承認、CTD2.7.3.5.1、2.7.6.(2))(L20210142)
34
国内長期投与試験(脊髄損傷後疼痛、脳卒中後疼痛、多発性硬化症に伴う疼痛)(リリカカプセル:2013年2月28日承認、CTD2.7.3.5.1、2.7.6.(2))(L20210143)
35
国際共同第Ⅲ相試験(脊髄損傷後疼痛)(リリカカプセル:2013年2月28日承認、CTD2.7.3.3、2.7.6.(2))(L20210144)
36
外国第Ⅱ相及び第Ⅲ相プラセボ対照試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.3.3)(L20210145)
37
外国第Ⅲ相用量反応試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.6.34)(L20230634)
38
外国第Ⅱ/Ⅲ相プラセボ対照試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.6.30)(L20230635)
39
外国第Ⅲ相プラセボ対照試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.6.31)(L20230636)
40
外国第Ⅱ/Ⅲ相プラセボ対照試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.6.32)(L20230637)
41
外国長期投与試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.3.5.2)(L20210146)
42
臨床的有効性の概要(リリカカプセル:2010年4月16日承認、CTD2.7.3.1)(L20230638)
43
外国長期投与試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.6.35)(L20230639)
44
外国長期投与試験(帯状疱疹後神経痛)(リリカカプセル:2010年4月16日承認、CTD2.7.6.36)(L20230640)
45
処方における食事の影響(リリカカプセル 2010年4月16日承認、CTD2.7.6.3)(L20230641)
46
Bauer CS, et al.:J Neurosci. 2009;29(13):4076-4088(L20210147)
47
Fink K, et al.:Neuropharmacology. 2002;42(2):229-236(L20210148)
48
Maneuf YP, et al.:Pain. 2001;93(2):191-196(L20210149)
49
Tanabe M, et al.:J Neurosci Res. 2008;86(15):3258-3264(L20210150)
50
Bee LA, et al.:Pain. 2008;140(1):209-223(L20210151)
51
Field MJ, et al.:Pain. 1999;83(2):303-311(L20210152)
52
Field MJ, et al.:Pain. 1999;80(1-2):391-398(L20210153)
53
Tanabe M, et al.:Eur J Pharmacol. 2009;609(1-3):65-68(L20210154)
54
慢性筋骨格系疼痛モデルにおける薬効薬理試験(リリカカプセル:2012年6月22日承認、CTD2.6.2.2)(L20210155)
55
Field MJ, et al.:Br J Pharmacol. 1997;121(8):1513-1522(L20210156)
56
Field MJ, et al.:J Pharmacol Exp Ther. 1997;282(3):1242-1246(L20210157)