酸安定性・持続型マクロライド系抗生物質製剤
1錠 15円
| 剤形 | 直径(mm) | 重量(mg) | 厚さ(mm) | 性状 | 本体表示 | 外形 |
| フィルムコーティング錠 | 9.1 | 約227 | 4.6 | 白色 | ロキシスロ SW 150 |  |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| エルゴタミン(エルゴタミン酒石酸塩、ジヒドロエルゴタミンメシル酸塩)を含有する製剤 (クリアミン、ジヒデルゴット等) | エルゴタミンの作用を増強させ、四肢の虚血を起こすおそれがある。 | 肝薬物代謝酵素が阻害され、エルゴタミンの血中濃度が上昇し、エルゴタミンの末梢血管収縮作用が増強すると考えられる。 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| テオフィリン | テオフィリンの血中濃度が上昇し、中毒症状(悪心、嘔吐等)を起こすことがある。 | 肝薬物代謝酵素が阻害され、テオフィリン血中濃度が上昇すると考えられる。 |
| ワルファリンカリウム | ワルファリンの作用を増強させ出血症状を起こすおそれがある。 | 肝薬物代謝酵素が阻害され、ワルファリン血中濃度が上昇すると考えられる。 |
| 頻度不明 | |
| 過敏症注) | 発熱、多形紅斑、発疹等 |
| 精神神経系 | 眠気、錯乱、頭痛、浮動性めまい、舌のしびれ感、しびれ |
| 血液 | 好酸球増多、白血球減少 |
| 肝臓 | 胆汁うっ滞等の肝機能障害、AST(GOT)、ALT(GPT)、Al-P等の上昇 |
| 消化器 | 胸やけ、胃部不快感、腹痛、下痢、嘔吐、口渇、食欲不振、腹部膨満感等 |
| *感覚器 | 味覚異常、嗅覚異常、難聴、耳鳴、回転性めまい、視力障害、霧視 |
| その他 | 全身倦怠感、脱力感、動悸、関節痛、鼻出血、月経異常、浮腫、菌交代症 |
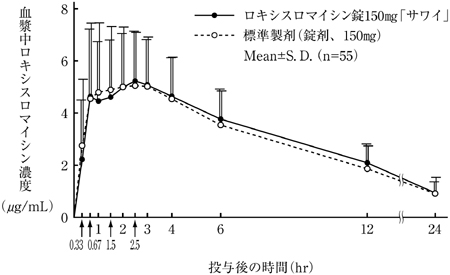
| Cmax(μg/mL) | Tmax(hr) | T1/2(hr) | AUC0-24hr(μg・hr/mL) | |
| ロキシスロマイシン錠150mg「サワイ」 | 6.07±1.97 | 2.0±1.3 | 8.9±1.9 | 61.79±19.85 |
| 標準製剤(錠剤、150mg) | 5.86±2.08 | 1.9±1.2 | 9.0±2.3 | 58.90±24.72 |