作成又は改訂年月
日本標準商品分類番号
薬効分類名
承認等
販売名
クレマスチン錠1mg「日医工」
販売名コード
承認・許可番号
22900AMX00054000
Clemastine
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法:
室温保存
使用期限:
外装に表示の使用期限内に使用すること。
組成
有効成分
クレマスチンフマル酸塩
含量
1錠中 1.34mg(クレマスチンとして1mg)
添加物
乳糖水和物、トウモロコシデンプン、低置換度ヒドロキシプロピルセルロース、ヒドロキシプロピルセルロース、タルク、ステアリン酸マグネシウム、メタケイ酸アルミン酸マグネシウム
剤形・色調
白色の割線入素錠
外形
直径7.1mm、厚さ2.4mm、質量120mg
識別コード

14A
販売名
クレマスチンシロップ0.01%「日医工」
販売名コード
承認・許可番号
22900AMX00052000
Clemastine
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法:
室温保存
使用期限:
外装に表示の使用期限内に使用すること。
規制区分
組成
有効成分
クレマスチンフマル酸塩
含量
1mL中 0.134mg(クレマスチンとして0.1mg)
添加物
白糖、パラオキシ安息香酸エチル、パラオキシ安息香酸ブチル、pH調整剤、エタノール、香料
販売名
クレマスチンドライシロップ0.1%「日医工」
販売名コード
承認・許可番号
22900AMX00053000
Clemastine
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法:
室温保存
使用期限:
外装に表示の使用期限内に使用すること。
規制区分
組成
有効成分
クレマスチンフマル酸塩
含量
1g中 1.34mg(クレマスチンとして1mg)
添加物
精製白糖、香料
一般的名称
クレマスチンフマル酸塩錠
クレマスチンフマル酸塩シロップ
クレマスチンフマル酸塩ドライシロップ
禁忌
本剤の成分に対し過敏症の既往歴のある患者
*閉塞隅角緑内障の患者[抗コリン作用により眼圧が上昇し、症状を悪化させることがある。]
前立腺肥大等下部尿路に閉塞性疾患のある患者[抗コリン作用により排尿障害が悪化するおそれがある。]
狭窄性消化性潰瘍又は幽門十二指腸閉塞のある患者[抗コリン作用により消化管運動が抑制され、症状が悪化するおそれがある。]
効能又は効果
錠1mg:
アレルギー性皮膚疾患(蕁麻疹、湿疹、皮膚炎、そう痒症)
アレルギー性鼻炎
シロップ0.01%、ドライシロップ(0.1%):
アレルギー性皮膚疾患(蕁麻疹、湿疹、皮膚炎、そう痒症)
アレルギー性鼻炎、感冒等上気道炎に伴うくしゃみ・鼻汁・咳嗽
用法及び用量
クレマスチン錠1mg「日医工」
1日量2錠(クレマスチンとして2mg)を朝晩2回に分けて経口投与する。
なお、年齢、症状により適宜増減する。
クレマスチンシロップ0.01%「日医工」
通常1日20mL(クレマスチンとして2mg)を2回に分けて経口投与する。
用量は患者の症状、年齢・体重などにより適宜増減することができる。
幼小児に対する標準的な用量として、下記の1日用量がすすめられる。
年齢:1歳以上3歳未満
1日用量:4mL(クレマスチンとして0.4mg)
年齢:3歳以上5歳未満
1日用量:5mL(クレマスチンとして0.5mg)
年齢:5歳以上8歳未満
1日用量:7mL(クレマスチンとして0.7mg)
年齢:8歳以上11歳未満
1日用量:10mL(クレマスチンとして1mg)
年齢:11歳以上15歳未満
1日用量:13mL(クレマスチンとして1.3mg)
1歳未満の乳児に使用する場合には、体重、症状などを考慮して適宜投与量を決める。
クレマスチンドライシロップ0.1%「日医工」
通常、成人は1日クレマスチンとして2mg(本剤2g)を朝晩2回に分けて経口投与する。
用量は患者の症状、年齢、体重などにより適宜増減する。
なお、用時水に溶かして用いる。
幼小児に対する標準的な用量として、下記の1日量を2回に分け、用時溶解して経口投与する。
年齢:1歳以上3歳未満
1日用量:0.4g(クレマスチンとして0.4mg)
年齢:3歳以上5歳未満
1日用量:0.5g(クレマスチンとして0.5mg)
年齢:5歳以上8歳未満
1日用量:0.7g(クレマスチンとして0.7mg)
年齢:8歳以上11歳未満
1日用量:1g(クレマスチンとして1mg)
年齢:11歳以上15歳未満
1日用量:1.3g(クレマスチンとして1.3mg)
なお、1歳未満の乳児に使用する場合には、体重、症状などを考慮して適宜投与量を決める。
使用上の注意
慎重投与
1てんかん等の痙攣性疾患、又はこれらの既往歴のある患者[痙攣閾値を低下させることがある。]
2*開放隅角緑内障の患者[抗コリン作用により眼圧が上昇し、症状を悪化させることがある。]
重要な基本的注意
眠気を催すことがあるので、本剤投与中の患者には、自動車の運転等危険を伴う機械の操作には従事させないよう十分注意すること。
相互作用
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
中枢神経抑制剤
鎮静剤
催眠剤等
アルコール | 中枢神経抑制作用が増強されることがあるので、減量するなど慎重に投与すること。 | いずれも中枢神経抑制作用を有するため。 |
抗コリン剤
アトロピン等
MAO阻害剤 | 抗コリン作用が増強されることがあるので、減量するなど慎重に投与すること。 | 作用を増強させるため。 |
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用
痙攣、興奮(頻度不明)
痙攣、興奮があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと(乳児、幼児では特に注意すること)。
肝機能障害、黄疸(頻度不明)
AST(GOT)、ALT(GPT)、Al-P、LDH、γ-GTPの上昇等を伴う肝機能障害、黄疸があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。
その他の副作用
| | 頻度不明 |
| 過敏症注) | 発疹 |
| 精神神経系 | 眠気、浮動性めまい,頭重、倦怠感 |
| 消化器 | 悪心・嘔吐、口渇、食欲不振、下痢 |
| 肝臓 | AST(GOT)、ALT(GPT)、Al-P、LDH、γ-GTPの上昇 |
その他の副作用の注意
高齢者への投与
一般に高齢者では生理機能が低下しているので減量するなど注意すること。
妊婦、産婦、授乳婦等への投与
妊婦又は妊娠している可能性のある婦人には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。[妊娠中の投与に関する安全性は確立していない。]
授乳中の婦人には投与することを避け、やむを得ず投与する場合には授乳を中止させること。[母乳中へ移行することが報告されている。]
小児等への投与
乳児、幼児に投与する場合には、観察を十分に行い慎重に投与すること。[痙攣、興奮等の中枢神経症状があらわれることがある。]
過量投与
徴候、症状:
中枢神経抑制、興奮、口渇、瞳孔散大、潮紅、胃腸症状等
処置:
一般的な薬物除去法(催吐、胃洗浄、活性炭投与等)により、除去する。また必要に応じて対症療法を行う。
適用上の注意
薬剤交付時:
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。(PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告されている。)
薬物動態
溶出挙動
クレマスチン錠1mg「日医工」:
日本薬局方外医薬品規格第3部に定められたクレマスチンフマル酸塩錠の溶出規格に適合していることが確認されている。1)
クレマスチンドライシロップ0.1%「日医工」:
日本薬局方外医薬品規格第3部に定められたクレマスチンフマル酸塩ドライシロップの溶出規格に適合していることが確認されている。1)
薬効薬理
クレマスチンフマル酸塩は、ヒスタミンH1受容体遮断薬である。H1受容体を介するヒスタミンによるアレルギー性反応(毛細血管の拡張と透過性亢進、気管支平滑筋の収縮、知覚神経終末刺激によるそう痒など)を抑制する。2)
有効成分に関する理化学的知見
一般名:
クレマスチンフマル酸塩(Clemastine Fumarate)
化学名:
(2R)-2-{2-[(1R)-1-(4-Chlorophenyl)-1-phenylethoxy]ethyl}-1-methylpyrrolidine monofumarate
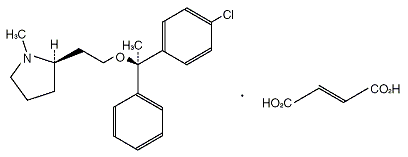
構造式:
分子式:
C21H26ClNO・C4H4O4
分子量:
459.96
性状:
白色の結晶性の粉末で、においはない。
メタノール又は酢酸(100)にやや溶けにくく、エタノール(95)に溶けにくく、ジエチルエーテルに極めて溶けにくく、水にほとんど溶けない。
融点:
176〜180℃(分解)
取扱い上の注意
安定性試験
クレマスチン錠1mg「日医工」:
最終包装製品を用いた長期保存試験(25℃、相対湿度60%)の結果、通常の市場流通下において3年間安定であることが確認された。3)
クレマスチンシロップ0.01%「日医工」:
最終包装製品を用いた長期保存試験(25℃、相対湿度60%)の結果、通常の市場流通下において3年間安定であることが確認された。3)
クレマスチンドライシロップ0.1%「日医工」:
最終包装製品を用いた長期保存試験(25℃、相対湿度60%)の結果、通常の市場流通下において3年間安定であることが確認された。3)
包装
クレマスチン錠1mg「日医工」
100錠(10錠×10;PTP)
1000錠(10錠×100;PTP)
クレマスチンシロップ0.01%「日医工」
0.1mg/mL×500mL
クレマスチンドライシロップ0.1%「日医工」
1mg/g×100g(バラ)
主要文献及び文献請求先
主要文献
1
日医工株式会社 社内資料:溶出試験
2
第十七改正日本薬局方解説書 C-1607,廣川書店,東京(2016)
3
日医工株式会社 社内資料:安定性試験
文献請求先
主要文献欄に記載の文献・社内資料は下記にご請求下さい。
日医工株式会社 お客様サポートセンター
〒930-8583 富山市総曲輪1丁目6番21
フリーダイアル(0120)517-215
Fax(076)442-8948
製造販売業者等の氏名又は名称及び住所
製造販売元
日医工株式会社
富山市総曲輪1丁目6番21


 14A
14A