1
日本人における反復経口投与試験(スプリセル錠:2009年1月21日承認、申請資料概要 2.7.2.2)
2
Takahashi S, et al.:Cancer Sci. 2011;102(11):2058-2064.
3
母集団薬物動態解析(スプリセル錠:2011年6月16日承認、審査報告書)
4
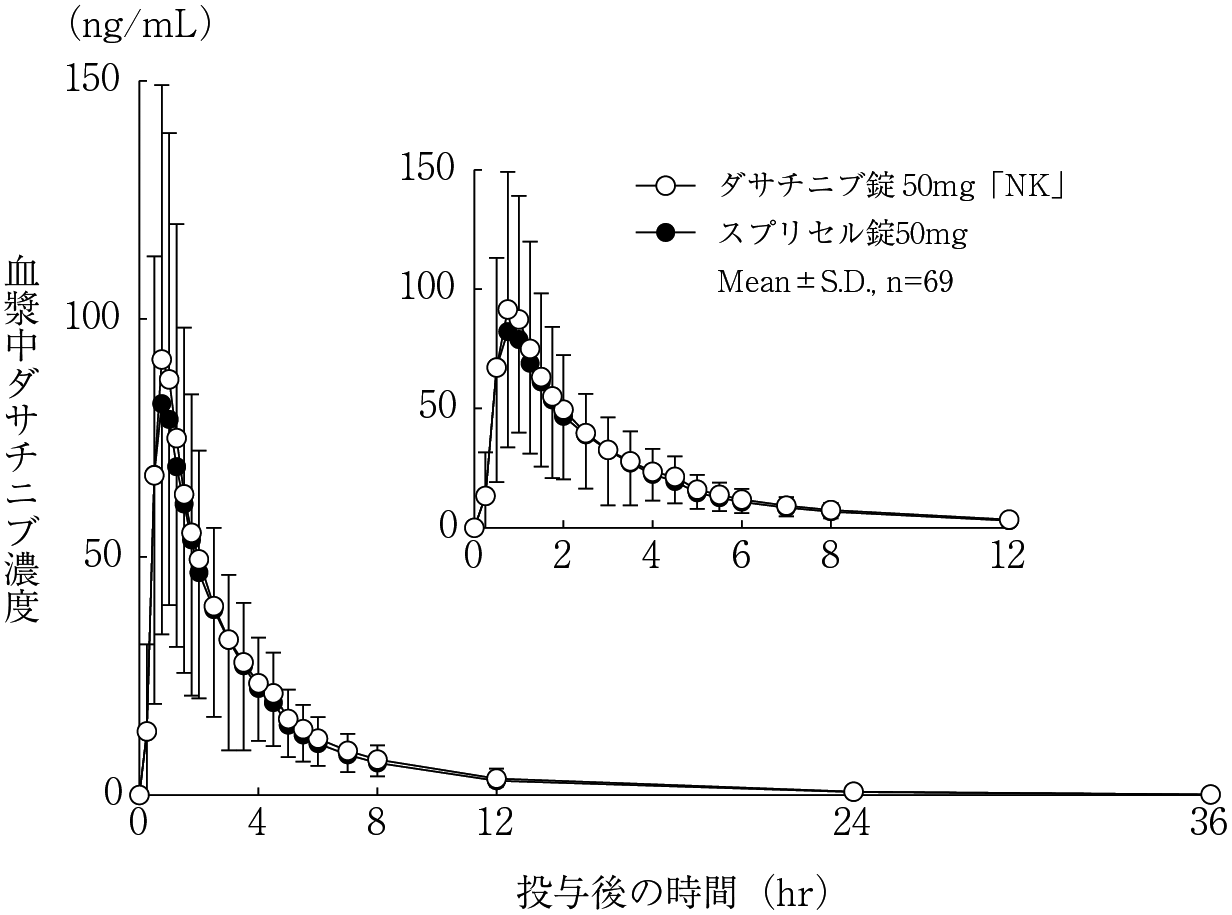
社内資料:生物学的同等性試験(錠50mg)
5
外国人における薬物動態に及ぼす低脂肪食及び高脂肪食の影響(スプリセル錠:2009年1月21日承認、申請資料概要2.7.6.2.13)
6
分布(スプリセル錠:2009年1月21日承認、申請資料概要2.7.2.3)
7
外国人における単回経口投与試験(スプリセル錠:2009年1月21日承認、申請資料概要 2.7.2.3)
8
代謝(動物間の比較)(スプリセル錠:2009年1月21日承認、申請資料概要 2.6.4.5)
9
排泄(スプリセル錠:2009年1月21日承認、申請資料概要2.7.2.2、2.7.2.3)
10
ダサチニブの薬物動態に対する特殊集団の影響(スプリセル錠:2009年1月21日承認、申請資料概要 2.7.2.3)
11
社内資料:生物学的同等性試験(錠20mg)
12
イマチニブに抵抗性又は不耐容の慢性期慢性骨髄性白血病患者におけるダサチニブ100mg1日1回投与法設定のための海外臨床第III相無作為化試験(スプリセル錠:2009年1月21日承認、申請資料概要 2.7.6.2)
13
イマチニブに抵抗性又は不耐容の移行期慢性骨髄性白血病患者における海外臨床第II相試験(スプリセル錠:2009年1月21日承認、申請資料概要 2.7.6.2)
14
イマチニブに抵抗性又は不耐容の骨髄芽球性急性期慢性骨髄性白血病患者における海外臨床第II相試験(スプリセル錠:2009年1月21日承認、申請資料概要 2.7.6.2)
15
イマチニブに抵抗性又は不耐容のリンパ芽球性急性期慢性骨髄性白血病又はPhiladelphia染色体陽性急性リンパ性白血病患者における海外臨床第II相試験(スプリセル錠:2009年1月21日承認、申請資料概要 2.7.6.2)
16
2年間投与による有効性のまとめ-EU clinical summary of efficacy(スプリセル錠:2009年1月21日承認、申請資料概要 2.7.3 Appendix 1)
17
In vitroでの生化学的及び構造学的実験(スプリセル錠:2009年1月21日承認、申請資料概要 2.6.2.2.1)
18
細胞アッセイ(スプリセル錠:2009年1月21日承認、申請資料概要 2.4.2.1.1、2.6.2.2.2)
19
CMLモデルにおける抗腫瘍活性(In vivo)(スプリセル錠:2009年1月21日承認、申請資料概要 2.6.2.2.3)