1
Ishizawa K, et al.:Cancer Sci. 2009;100(2):357-62
2
Kikuchi A, et al.:Int J Hematol. 2009;90(4):492-500
3
社内資料:日本人健康成人における単回投与試験(2009年10月16日承認、CTD2.7.2.2)
4
Goldman S C, et al.:Blood. 2001;97(10):2998-3003
がん化学療法用尿酸分解酵素製剤
1瓶 51084円
有効成分 | ラスブリカーゼ(遺伝子組換え) 1バイアル(2mL容器)中1.5mg |
|---|---|
添加剤 | D‐マンニトール 10.6mg L‐アラニン 15.9mg リン酸水素ナトリウム水和物 12.6-14.3mg |
添加剤 | ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 1アンプル(2mL容器)1.0mL中に1.0mg含有 |
|---|
有効成分 | ラスブリカーゼ(遺伝子組換え) 1バイアル(10mL容器)中7.5mg |
|---|---|
添加剤 | D‐マンニトール 53mg L‐アラニン 79.5mg リン酸水素ナトリウム水和物 63.0-71.5mg |
添加剤 | ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール 1アンプル(5mL容器)5.0mL中に5.0mg含有 |
|---|
| ラスリテック点滴静注用 | |
| pH | 7.7~8.3 |
|---|---|
| 浸透圧比 | 約1(0.9%生理食塩液に対する比) |
| 性状 | 本剤は白色の凍結乾燥品であり、添付溶解液で溶解するとき、無色澄明又はわずかに混濁した液剤となる。 |
| ラスリテック点滴静注用 | |
| pH | 7.7~8.3 |
|---|---|
| 浸透圧比 | 約1(0.9%生理食塩液に対する比) |
| 性状 | 本剤は白色の凍結乾燥品であり、添付溶解液で溶解するとき、無色澄明又はわずかに混濁した液剤となる。 |
5%以上~10%未満 | 5%未満 | 頻度不明 | |
|---|---|---|---|
血液 | 白血球減少、貧血、溶血、血小板減少、ヘモグロビン減少、APTT延長 | ||
消化器 | 便秘、悪心・嘔吐、食欲不振、心窩部不快感、咽喉頭不快感 | 下痢、腹痛、口内炎 | |
肝臓 | 肝機能障害(AST、ALT、Al‐P、総ビリルビンの上昇等) | LDH上昇、γ‐GTP上昇 | |
腎臓 | 尿蛋白、排尿困難、血尿 | ||
泌尿器 | BUN上昇、尿潜血陽性 | ||
精神神経系 | 頭痛、めまい | ||
皮膚 | 発疹、そう痒、脱毛、蕁麻疹 | ||
呼吸器 | 低酸素症、胸膜炎 | 呼吸困難、気管支痙攣、鼻炎 | |
筋・骨格 | 四肢痛 | 背部痛、顎痛 | |
代謝及び栄養 | 電解質異常(Na、K、Pの異常) | 血糖上昇、総蛋白減少、アミラーゼ上昇、アルブミン低下 | 電解質異常(Ca、Mgの異常) |
その他 | アレルギー反応、発熱 | 注射部位反応(硬結、紅斑等)、倦怠感、ほてり | 高血圧、徐脈、低血圧、感染(肺炎、敗血症等を含む)、粘膜の炎症、浮腫、疲労感、疼痛、カテーテル留置部位反応(紅斑、出血、疼痛等) |
投与量 (mg/kg) | 被験者数 | Cmax (μg/mL) | AUC (μg・h/mL) | CL (mL/h/kg) | Vz (mL/kg) | t1/2z (h) |
0.05 | 6 | 1.07±0.18 | 23.5±3.79 | 2.17±0.39 | 78.8±17.6 | 25.1±2.84 |
0.10 | 6 | 2.27±0.20 | 46.1±4.12 | 2.20±0.20 | 70.3±6.48 | 22.2±1.59 |
0.15 | 6 | 3.07±0.43 | 53.9±9.63 | 2.88±0.62 | 89.5±17.2 | 21.7±1.42 |
0.20 | 6 | 4.60±1.07 | 79.1±20.1 | 2.68±0.72 | 86.8±22.9 | 22.8±4.43 |

投与量 (mg/kg) | 被験者数 | Day1 | Day5 | |||
Cmax (μg/mL) | AUC0-24 (μg・h/mL) | Cmax (μg/mL) | AUC0-24 (μg・h/mL) | t1/2z (h) | ||
0.15 | 11 | 3.73±1.08 | 45.7±7.54 | 3.95±0.71 | 48.2±9.66 | 22.5±5.8 |
0.20 | 10 | 4.24±1.56 | 59.3±15.8 | 5.13±1.47 | 65.2±22.7 | 16.1±5.6 |
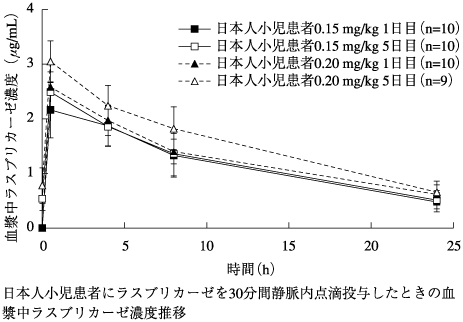
投与量 (mg/kg) | 被験者数 | Day1 | Day5 | |||
Cmax (μg/mL) | AUC0-24 (μg・h/mL) | Cmax (μg/mL) | AUC0-24 (μg・h/mL) | t1/2 (h) | ||
0.15 | 10 | 2.16±0.51 | 28.2±7.27 | 2.49±0.37 | 29.7±6.46 | 11.6±4.96 |
0.20 | 9注4) | 2.58±0.43 | 31.5±4.54 | 3.05±0.38 | 38.1±5.64 | 11.2±3.06 |
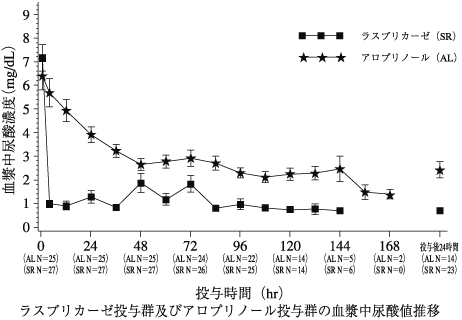
試験番号 | 投与量 | 投与方法 | 投与期間 | |
国内 | ACT5080 ARD5290 | 0.15mg/kg又は0.20mg/kg | 1日1回30分間の静脈内点滴投与 | 5日間 |
海外 | EFC2975 | 0.20mg/kg | 1日1回30分間の静脈内点滴投与 (高尿酸血症が継続している場合又はTLSの危険性が継続している場合は、化学療法開始後72時間までは12時間ごとに投与可能) | 5〜7日間 |