1
生殖発生毒性(ラット)(フェブリク錠:2011年1月21日承認、申請資料概要2.6.6.6)
2
Lehtisalo M, et al.: Clin Transl Sci. 2020; 13(6): 1236-1243.
3
がん原性(マウス、ラット)(フェブリク錠:2011年1月21日承認、申請資料概要2.6.6.5)
4
血漿中濃度及び排泄(健康成人、単回)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.1)
5
血漿中濃度(健康成人、単回)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.5)
6
血漿中濃度(健康成人、反復)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.8)
7
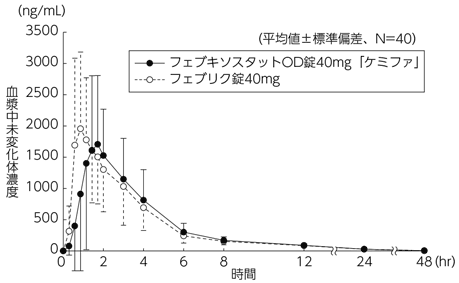
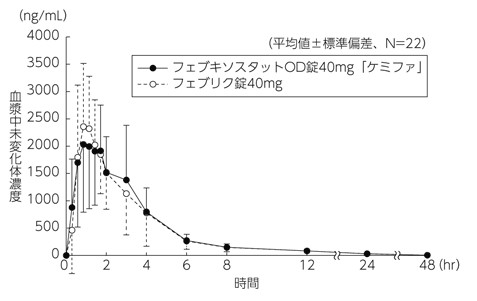
血漿中濃度(高尿酸血症患者、反復)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.31)
8
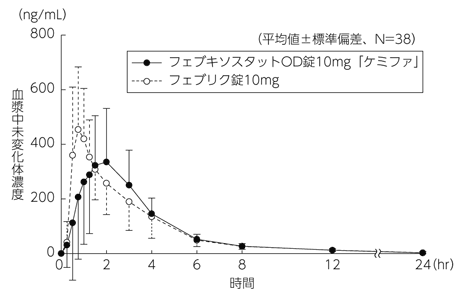
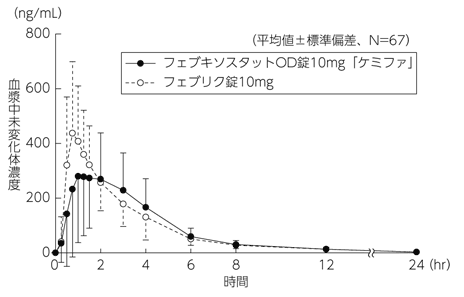
日本ケミファ株式会社:生物学的同等性に関する資料(社内資料)
9
Mukoyoshi M, et al.: Xenobiotica. 2008; 38(5): 496-510.
10
Grabowski BA, et al.: J Clin Pharmacol. 2011; 51(2): 189-201.
11
代謝(ヒト)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.2.2.1)
12
血漿中濃度(腎機能低下患者、反復)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.2.3、2.7.6.13)
13
Mayer MD, et al.: Am J Ther. 2005; 12(1): 22-34.
14
Khosravan R, et al.: J Clin Pharmacol. 2006; 46(1): 88-102.
15
Khosravan R, et al.: J Clin Pharmacol. 2008; 48(9): 1014-1024.
16
Khosravan R, et al.: Br J Clin Pharmacol. 2008; 65(3): 355-363.
17
薬物相互作用(制酸剤)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.20)
18
薬物相互作用(コルヒチン)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.18、2.7.6.19)
19
Khosravan R, et al.: J Clin Pharmacol. 2006; 46(8): 855-866.
20
薬物相互作用(デシプラミン)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.16)
21
薬物相互作用(ワルファリン)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.23、2.7.6.24)
22
Grabowski BA, et al.: Br J Clin Pharmacol. 2010; 70(1): 57-64.
23
薬物相互作用(テオフィリン)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.25)
24
薬物相互作用(ロシグリタゾン)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.26)
25
プラセボ対照無作為化二重盲検用量反応比較試験(痛風を含む高尿酸血症患者)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.33)
26
アロプリノール対照無作為化二重盲検比較試験(痛風を含む高尿酸血症患者)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.35a)
27
アロプリノール対照二重盲検比較試験(フェブリク錠:2011年1月21日承認、審査報告書)
28
長期投与試験(痛風を含む高尿酸血症患者)(フェブリク錠:2011年1月21日承認、申請資料概要2.7.6.40)
29
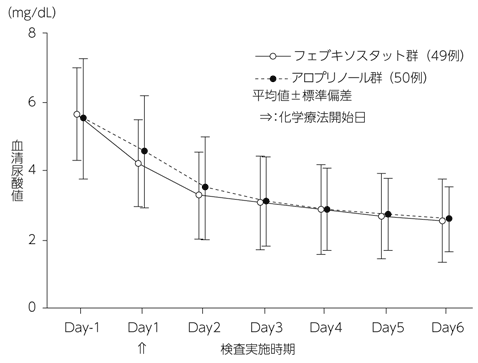
Tamura K, et al.: Int J Clin Oncol. 2016; 21(5): 996-1003.
30
アロプリノール対照非盲検無作為化比較試験(フェブリク錠:2016年5月23日承認、申請資料概要2.7.6.2)
31
Takano Y, et al.: Life Sci. 2005; 76(16):1835-1847.
32
血中及び尿中尿酸低下作用(ラット)(フェブリク錠:2011年1月21日承認、申請資料概要2.6.2.2.2)