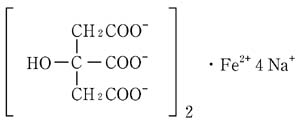1
今井一彰他:中毒研究, 1998;11:271-274
2
Balmadrid, C. et al.:Emerg. Med., 2009;41:36-41
3
社内資料:生物学的同等性試験
4
刈米重夫:代謝, 1981;18:373-384
5
内田立身:鉄欠乏性貧血, 新興医学出版, 1984;4
可溶性の非イオン型鉄剤
1錠 5.7円
有効成分 | クエン酸第一鉄ナトリウム 470.9mg 鉄として 50mg |
|---|---|
添加剤 | カルナウバロウ、結晶セルロース、酸化チタン、ステアリン酸Mg、デンプングリコール酸Na、ヒドロキシプロピルセルロース、ヒプロメロース |
| 剤形 | フィルムコーティング錠 |
|---|---|
| 外形 |   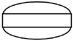 |
| 大きさ | 大きさ(直径) 10.1mm 大きさ(厚さ) 5.5mm |
| 質量 | 約546mg |
| 識別コード | SW 344 |
| 性状 | 白色 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
セフジニル | セフジニルの吸収を約10分の1に阻害することがあるので、3時間以上間隔を空けて本剤を投与すること。 | 相手薬剤と高分子鉄キレートを形成し、相手薬剤の吸収を阻害する。 |
キノロン系抗菌剤 塩酸シプロフロキサシン ノルフロキサシン トスフロキサシントシル酸塩水和物 スパルフロキサシン等 | 抗菌剤の吸収を阻害することがある。 | 相手薬剤と高分子鉄キレートを形成し、相手薬剤の吸収を阻害する。 |
テトラサイクリン系抗生物質 | 相互に吸収を阻害する。 | 相手薬剤と高分子鉄キレートを形成し、相互に吸収を阻害する。 |
甲状腺ホルモン製剤 レボチロキシンナトリウム水和物 リオチロニンナトリウム等 | チロキシンの吸収を阻害するおそれがある。 | 相手薬剤と高分子鉄キレートを形成し、相手薬剤の吸収を阻害するおそれがある。 |
制酸剤 | 鉄の吸収を阻害することがある。 | in vitro試験において、pHの上昇により、難溶性の鉄重合体を形成することが報告されている。 |
タンニン酸を含有する食品 | 鉄の吸収を阻害するおそれがある。 | in vitro試験において、タンニン酸と高分子鉄キレートを形成することが報告されている。 |
5%以上 | 0.1~5%未満 | 0.1%未満 | 頻度不明 | |
|---|---|---|---|---|
消化器 | 悪心・嘔吐 | 上腹部不快感、胃・腹痛、下痢、食欲不振、便秘、胸やけ | 腹部膨満感 | |
過敏症 | 発疹 | 瘙痒感 | 光線過敏症 | |
肝臓 | AST、ALTの上昇等 | Al-Pの上昇等 | ||
精神神経系 | 頭痛、めまい | |||
その他 | 倦怠感、浮腫 |
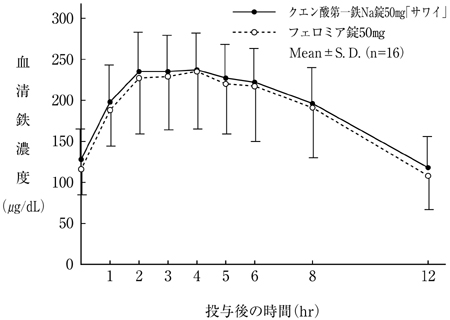
Cmax (μg/dL) | Tmax (hr) | T1/2 (hr) | AUC0-12hr (μg・hr/dL) | |
クエン酸第一鉄Na錠50mg「サワイ」 | 244±44 | 3.4±1.5 | 6.6±2.0 | 2351±474 |
フェロミア錠50mg | 240±68 | 3.6±1.1 | 6.5±3.3 | 2271±635 |