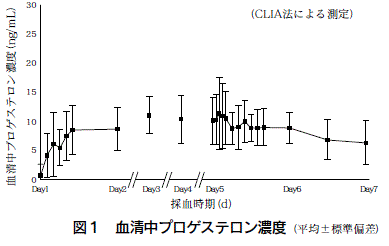
1
Janerich DT,et al:N.Engl.J.Med.,291(14),697,1974
2
梅原千治 他:ステロイドホルモン:製剤・生理・臨床.第4(黄体ホルモン),576,(南江堂)1967
3
Sandberg AA and Slaunwhite WR: J.Clin.Endocr.,18(3),253,1958
4
Hammond GL,et al: J.Biol.Chem.,255(11),5023,1980
5
Kleinstein J; Luteal Phase Study Group. Efficacy and tolerability of vaginal progesterone capsules (Utrogest200) compared with progesterone gel (Crinone 8%) for luteal phase support during assisted reproduction.Fertil.Steril.,83(6),1641,2005
6
富士製薬工業株式会社 社内資料
7
梅原千治 他:ステロイドホルモン:製剤・生理・臨床.第4(黄体ホルモン),603,(南江堂)1967