1
社内資料:生物学的同等性試験[錠5mg、OD錠5mg]
2
第十八改正日本薬局方解説書. 廣川書店. 2021;C-3110
経口脊髄小脳変性症治療剤
1錠 257.6円
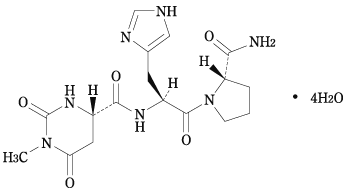
有効成分 | 1錠中、日局タルチレリン水和物 5mgを含有する。 |
|---|---|
添加剤 | D-マンニトール、トウモロコシデンプン、ポリビニルアルコール(部分けん化物)、ステアリン酸マグネシウム |
有効成分 | 1錠中、日局タルチレリン水和物 5mgを含有する。 |
|---|---|
添加剤 | 無水リン酸水素カルシウム、結晶セルロース、カルメロースカルシウム、軽質無水ケイ酸、スクラロース、ステアリン酸マグネシウム |
| 剤形 | 割線入り素錠 |
|---|---|
| 色調 | 白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 約7.0mm 大きさ(厚さ) 約3.0mm |
| 質量 | 約120.0mg |
| 識別コード | Kw324/TAL5 |
| 剤形 | 割線入り素錠 |
|---|---|
| 色調 | 白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 約7.0mm 大きさ(厚さ) 約2.6mm |
| 質量 | 約110.0mg |
| 識別コード | KW TAL/OD5 |
0.1~5%未満 | 0.1%未満 | |
|---|---|---|
血液 | 赤血球減少、ヘモグロビン減少 | |
循環器 | 血圧及び脈拍数の変動、動悸 | |
消化器 | 悪心、嘔吐、下痢、食欲不振、胃部不快感、胃炎、腹痛、口渇、便秘 | 舌炎 |
肝臓 | AST、ALT、γ-GTP、ALP、LDH、トリグリセリド、総コレステロールの上昇 | |
腎臓 | BUNの上昇 | |
精神神経系 | 頭痛、めまい、ふらつき、振戦 | しびれ、眠気、頭がボーっとする、不眠 |
過敏症 | 発疹、そう痒 | |
内分泌 | TSHの変動、甲状腺ホルモン(T3、T4)、プロラクチンの上昇 | 女性化乳房 |
その他 | CKの上昇、血糖上昇、熱感、倦怠感、頻尿 | 脱毛 |
判定パラメータ | 参考パラメータ | |||
AUC(0→12) (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
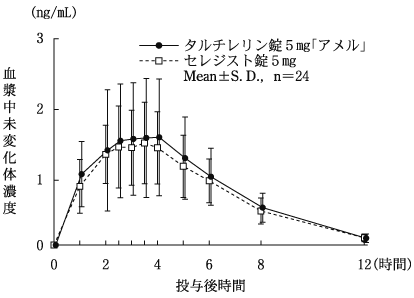
タルチレリン錠5mg「アメル」 | 10.13±4.14 | 1.88±0.96 | 3.00±1.08 | 1.99±0.71 |
セレジスト錠5mg | 9.31±2.95 | 1.73±0.65 | 3.19±0.82 | 1.92±0.26 |
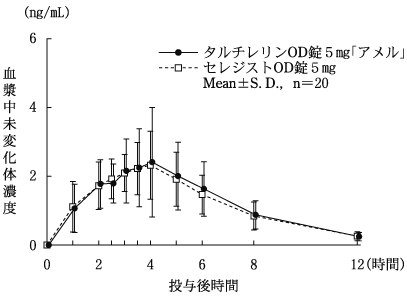
判定パラメータ | 参考パラメータ | |||
AUC(0→12) (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
タルチレリンOD錠 5mg「アメル」 | 14.88±6.00 | 2.75±1.51 | 3.30±1.26 | 2.27±0.38 |
セレジストOD錠5mg | 14.43±4.27 | 2.66±0.97 | 3.38±1.23 | 2.37±0.49 |
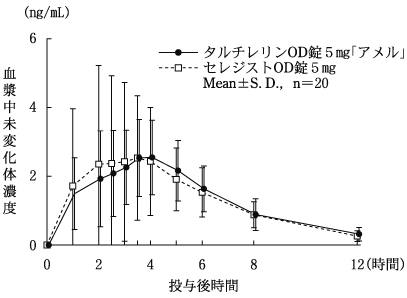
判定パラメータ | 参考パラメータ | |||
AUC(0→12) (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
タルチレリンOD錠 5mg「アメル」 | 16.21±6.04 | 2.97±1.41 | 3.65±0.97 | 2.45±0.43 |
セレジストOD錠5mg | 16.34±11.37 | 3.01±2.76 | 3.60±1.10 | 2.37±0.60 |
 0120-041-189
0120-041-189