1
CYP2D6の遺伝子型の解析(ストラテラカプセル:2012年8月24日承認、申請資料概要2.7.2.1)
2
単回投与及び反復投与(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
3
成人と患児の薬物動態比較(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.3)
4
田中孝典他:新薬と臨床, 2018;67(10):1220-1230
5
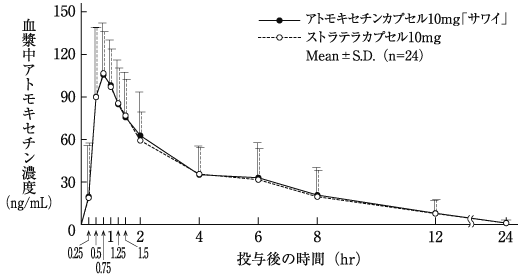
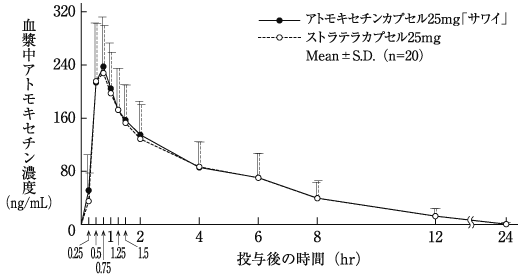
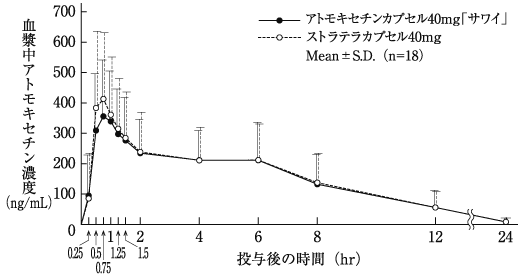
社内資料:生物学的同等性試験(カプセル40mg)
6
絶対的生物学的利用率(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
7
食事の影響(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.1.3)
8
分布(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.3)
9
代謝酵素及び代謝物(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.3)
10
CYP2D6遺伝子多型の薬物動態に及ぼす影響①(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.3, 2.7.2.5)
11
CYP2D6遺伝子多型の薬物動態に及ぼす影響②(ストラテラカプセル:2012年8月24日承認、申請資料概要2.7.2.2)
12
排泄(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.2)
13
腎機能障害時の血漿中濃度(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.2, 2.7.2.5)
14
肝機能障害時の血漿中濃度(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
15
蛋白結合率の高い薬剤との併用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.3)
16
メチルフェニデートとの併用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
17
吸入サルブタモールとの併用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
18
サルブタモール静脈内投与との併用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
19
CYP2D6阻害剤との併用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
20
胃のpHに影響する薬剤との併用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
21
ミダゾラムとの併用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
22
エタノールとの併用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
23
社内資料:生物学的同等性試験(カプセル5mg)
24
Takahashi, M. et al.:J. Child Adolesc. Psychopharmacol., 2009;19(4):341-351
25
小児AD/HD患者に対する国内第Ⅱ/Ⅲ相試験(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.3)
26
小児AD/HD患者に対する第Ⅲ相長期継続投与臨床試験(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.3)
27
Michelson, D. et al.:Pediatrics, 2001;108(5):e83
28
小児AD/HD患者に対する外国第Ⅲ相試験(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.4.2, 2.7.6.3)
29
成人AD/HD患者に対する第Ⅲ相短期投与プラセボ対照二重盲検比較試験(ストラテラカプセル:2012年8月24日承認、申請資料概要2.5.4.2.3, 2.7.6.3)
30
成人AD/HD患者に対する第Ⅲ相長期継続投与臨床試験(ストラテラカプセル:2012年8月24日承認、申請資料概要2.5.4.2.4, 2.7.6.4)
31
Loghin, C. et al.:Br. J. Clin. Pharmacol., 2013;75:538-549
32
作用機序(ストラテラカプセル:2009年4月22日承認、申請資料概要2.6.1)
33
モノアミン取り込み阻害作用の検討(ストラテラカプセル:2009年4月22日承認、申請資料概要2.6.2.2, 2.6.2.3)
34
Bymaster, F. P. et al.:Neuropsychopharmacology, 2002;27(5):699-711