1
厚生労働省:重篤副作用疾患別対応マニュアル 薬剤性過敏症症候群
2
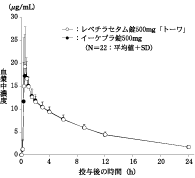
日本人健康成人におけるレベチラセタム単回投与時の薬物動態(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.3)
3
日本人健康成人におけるレベチラセタム反復投与時の薬物動態(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.3)
4
日本人健康成人におけるレベチラセタム錠及び注射剤の単回投与時の比較(イーケプラ点滴静注:2014年7月4日承認、申請資料概要2.7.6.1)
5
外国小児てんかん患者におけるレベチラセタム単回投与時の薬物動態(イーケプラ錠・ドライシロップ:2013年5月31日承認、申請資料概要2.7.6.2、審査報告書)
6
レベチラセタムに関する母集団薬物動態解析-1(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.2.2)
7
Toublanc N,et al.:Drug Metab Pharmacokinet.2014;29:61-68
8
中村卓 他:医学と薬学.2021;78(10):1191-1205
9
日本人健康成人におけるレベチラセタムの薬物動態に及ぼす食事の影響(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.1)
10
Ramael S,et al.:Clin Ther.2006;28:734-744
11
Strolin Benedetti M,et al.:Eur J Clin Pharmacol.2003;59:621-630
12
バイオアベイラビリティ(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.1)
13
分布(イーケプラ錠:2010年7月23日承認、申請資料概要2.6.4.1)
14
代謝(イーケプラ錠:2010年7月23日承認、申請資料概要2.4.3.3)
15
代謝物の薬理試験(イーケプラ錠:2010年7月23日承認、申請資料概要2.6.2.2)
16
薬物動態学的薬物相互作用(イーケプラ錠:2010年7月23日承認、申請資料概要2.6.4.7)
17
排泄(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.2.3)
18
Yamamoto J,et al.:Clin.Drug Investig.2014;34:819-828
19
Brockmöller J,et al.:Clin Pharmacol Ther.2005;77:529-541
20
肝機能低下者(外国人)におけるレベチラセタム単回投与時の薬物動態(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.4)
21
高齢者(外国人)におけるレベチラセタム単回及び反復経口投与時の薬物動態(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.4)
22
Browne T R,et al.:J Clin Pharmacol.2000;40:590-595
23
レベチラセタム及びフェニトインが相互の薬物動態に及ぼす影響(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.5)
24
Coupez R,et al.:Epilepsia.2003;44:171-178
25
Ragueneau-Majlessi I,et al.:Epilepsia.2002;43:697-702
26
レベチラセタム及び経口避妊薬が相互の薬物動態に及ぼす影響(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.5)
27
Levy R H,et al.:Epilepsy Res.2001;46:93-99
28
Ragueneau-Majlessi I,et al.:Epilepsy Res.2001;47:55-63
29
レベチラセタム及び代謝物の薬物動態に及ぼすプロベネシドの影響(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.5)
30
ドライシロップと錠剤の生物学的同等性試験(イーケプラ錠・ドライシロップ:2013年5月31日承認、申請資料概要2.7.6.1)
31
社内資料:生物学的同等性試験(錠250mg)
32
日本における部分発作単剤療法の第Ⅲ相試験(イーケプラ錠・ドライシロップ・点滴静注:2015年2月20日承認、審査報告書)
33
日本における部分発作併用療法のプラセボ対照比較試験(国内第Ⅱ/Ⅲ相試験(成人、併用療法))(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.7)
34
日本における部分発作併用療法のプラセボ対照比較試験(国内第Ⅲ相試験(成人、併用療法))(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.7)
35
八木和一 他:てんかん研究.2012;29:441-454
36
日本における部分発作併用療法の長期継続投与試験(イーケプラ錠:2010年7月23日承認、申請資料概要2.7.6.8、審査報告書)
37
日本における部分発作併用療法の小児第Ⅲ相試験(イーケプラ錠・ドライシロップ:2013年5月31日承認、申請資料概要2.7.4.7、2.7.6.4)
38
日本及び中国における強直間代発作併用療法のプラセボ対照比較試験(イーケプラ錠・ドライシロップ・点滴静注:2016年2月29日承認、申請資料概要2.7.6.1)
39
日本における強直間代発作併用療法の小児第Ⅲ相試験(イーケプラ錠・ドライシロップ・点滴静注:2016年2月29日承認、申請資料概要2.7.6.2)
40
日本における強直間代発作併用療法の長期継続投与試験(イーケプラ錠・ドライシロップ・点滴静注:2016年2月29日承認、申請資料概要2.7.6.2、審査報告書)
41
Noyer M,et al.:Eur J Pharmacol.1995;286:137-146
42
Lynch B A,et al.:Proc Nat Acad Sci U.S.A.2004;101:9861-9866
43
Lukyanetz E A,et al.:Epilepsia.2002;43:9-18
44
Pisani A,et al.:Epilepsia.2004;45:719-728
45
Rigo J M,et al.:Br J Pharmacol.2002;136:659-672
46
Margineanu D G,et al.:Pharmacol Res.2000;42:281-285
47
Kaminski R M,et al.:Neuropharmacology.2008;54:715-720
48
Klitgaard H,et al.:Eur J Pharmacol.1998;353:191-206
49
Gower A J,et al.:Epilepsy Res.1995;22:207-213
50
Gower A J,et al.:Eur J Pharmacol.1992;222:193-203
51
Löscher W,et al.:J Pharmacol Exp Ther.1998;284:474-479
52
Lamberty Y,et al.:Epilepsy Behav.2000;1:333-342
53
Hanon E,et al.:Seizure.2001;10:287-293










 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379

