1
Newport DJ, et al.:Pediatrics. 2008;122:e223-231
2
厚生労働省:重篤副作用疾患別対応マニュアル 薬剤性過敏症症候群
3
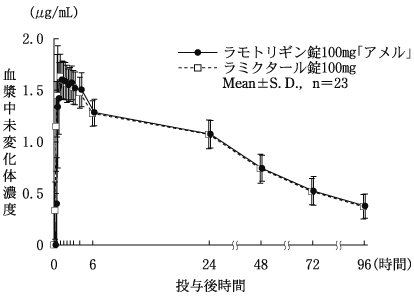
血中濃度(健康成人)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.2.2.2.1)
4
血中濃度(てんかん患者)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.2.2.2)
5
Jawad S, et al.:Epilepsy Res. 1987;1:194-201
6
Anderson GD, et al.:Clin Pharmacol Ther. 1996;60:145-156
7
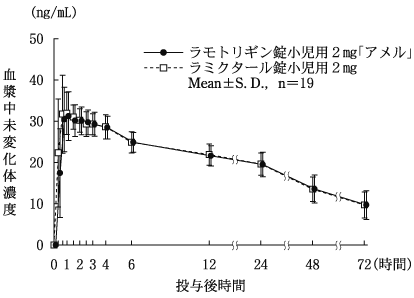
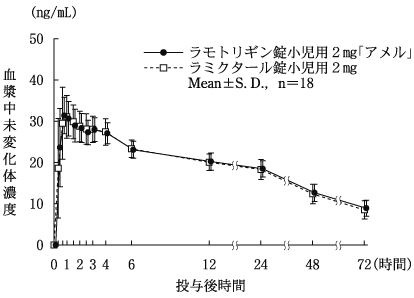
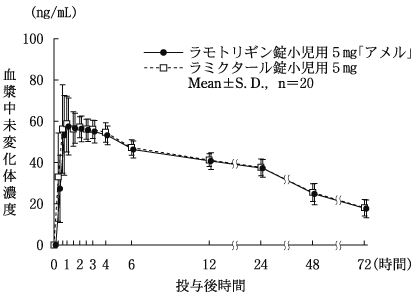
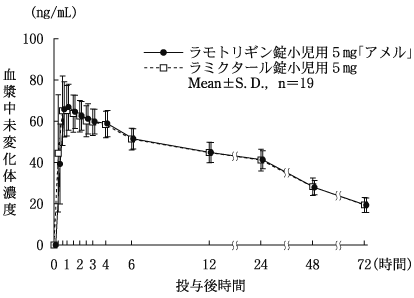
社内資料:生物学的同等性試験[錠小児用2mg、錠小児用5mg、錠100mg]
8
吸収(食事の影響)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.1.1.2)
9
Yuen WC, et al.:Br J Clin Pharmacol. 1988;26:242P
10
血漿蛋白結合(ラミクタール錠:2005年12月26日承認、申請資料概要 2.6.4.4.3)
11
Magdalou J, et al.:J Pharmacol Exp Ther. 1992;260:1166-1173
12
Green MD, et al.:Drug Metab Dispos. 1995;23:299-302
13
代謝(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.2.2.1.7)
14
排泄(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.2.2.2.1.4)
15
Fillastre JP, et al.:Drugs Exp Clin Res. 1993;19:25-32
16
腎機能障害患者(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.2.2.2.3.3)
17
Marcellin P, et al.:Br J Clin Pharmacol, 2001;51:410-414
18
肝機能障害患者(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.2.2.2.3.1)
19
Posner J, et al.:J Pharm Med. 1991;1:121-128
20
血中濃度(高齢者)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.2.3.5)
21
他剤との併用試験(バルプロ酸ナトリウム)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.2.1.7)
22
Ebert U, et al.:Eur J Clin Pharmacol. 2000;56:299-304
23
van der Lee MJ, et al.:Clin Pharmacol Ther. 2006;80:159-168
24
Burger DM, et al.:Clin Pharmacol Ther. 2008;84:698-703
25
他剤との併用試験(リスペリドン)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.2.4.4)
26
他剤との併用試験(経口避妊薬)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.2.4.1)
27
他剤との併用試験(オランザピン)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.2.2.2.4.2, 2.7.6.2.4.2)
28
Levy RH, et al.:Ther Drug Monit. 2005;27:193-198
29
Weintraub D, et al.:Arch Neurol. 2005;62:1432-1436
30
Doose DR, et al.:Epilepsia. 2003;44:917-922
31
Gidal BE, et al.:Epilepsy Res. 2005;64:1-11
32
Perucca E, et al.:Epilepsy Res. 2003;53:47-56
33
Majid O, et al.:Br J Clin Pharmacol. 2016;82:422-430
34
Halász P, et al.:Epilepsia. 2009;50:443-453
35
Brodie MJ, et al.:Epilepsia. 2005;46:1407-1413
36
他剤との併用試験(リチウム)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.2.4.3)
37
Schieber FC, et al.:Hum Psychopharmacol. 2009;24:145-152
38
In vitro試験(ラミクタール錠:2011年7月1日承認、申請資料概要 2.7.4.6)
39
社内資料:生物学的同等性試験(溶出挙動比較)
40
Yamamoto T, et al.:Epilepsy & Seizure Journal of Japan Epilepsy Society. 2014;7:55-65
41
国際共同第Ⅲ相試験(成人、単剤療法)(ラミクタール錠:2014年8月29日承認、審査報告書)
42
Yasumoto S, et al.:Brain Dev. 2016;38:407-413
43
国際共同第Ⅲ相試験(小児、単剤療法)(ラミクタール錠:2015年9月24日承認、申請資料概要 2.7.6.LAM115377試験)
44
Reunanen M, et al.:Epilepsy Res. 1996;23:149-155
45
海外第Ⅲ相試験(小児及び成人、単剤療法)(成人、併用療法)(ラミクタール錠:2014年8月29日承認、審査報告書)
46
村崎光邦, 他:臨床精神薬理. 2008;11:117-134
47
国内第Ⅲ相試験(成人、併用療法)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.3.1.2)
48
国内第Ⅲ相試験(成人、併用療法)(ラミクタール錠:2008年10月16日承認、審査報告書)
49
大田原俊輔, 他:てんかん研究. 2008;25:425-440
50
国内第Ⅲ相試験(小児、併用療法)(ラミクタール錠:2008年10月16日承認、審査報告書)
51
Messenheimer J, et al.:Epilepsia. 1994;35:113-121
52
Schapel GJ, et al.:J Neurol Neurosurg Psychiatry. 1993;56:448-453
53
海外臨床試験(成人、併用療法)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.3.3.2.2.1, 2.7.6.3.1.5, 2.7.6.3.1.6)
54
Duchowny M, et al.:Neurology. 1999;53:1724-1731
55
海外臨床試験(小児、併用療法)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.3.1.8)
56
Motte J, et al.:N Engl J Med. 1997;337:1807-1812
57
海外臨床試験(小児及び成人、併用療法)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.3.1.9)
58
Biton V, et al.:Neurology. 2005;65:1737-1743
59
小山司, 他:臨床精神医学. 2011;40:369-383
60
国内長期投与試験(成人)(ラミクタール錠:2011年7月1日承認、申請資料概要 2.7.4.7, 2.7.6 SCA106052試験)
61
国内長期投与試験(成人)(ラミクタール錠:2011年7月1日承認、審査報告書)
62
厚生労働省医薬食品局:医薬品・医療機器等安全性情報, No.287(2012)
63
国内臨床試験における皮膚障害の発現率(ラミクタール錠:2008年10月16日承認、申請資料概要 2.7.6.3.2.9)
64
国内臨床試験における皮膚粘膜眼症候群(Stevens-Johnson症候群)の発現率(ラミクタール錠:2008年10月16日承認、申請資料概要 2.5.5.4)
65
Xie X, et al.:Pflügers Arch. 1995;430:437-446
66
Leach MJ, et al.:Epilepsia. 1986;27:490-497
67
Miller AA, et al.:Epilepsia. 1986;27:483-489
68
Cramer CL, et al.:Life Sci. 1994;54:PL271-275
69
Dalby NO, et al.:Epilepsy Res. 1997;28:63-72
70
Wheatley PL, et al.:Epilepsia. 1989;30:34-40
71
Otsuki K, et al.:Epilepsy Res. 1998;31:101-112
72
Stratton SC, et al.:Epilepsy Res. 2003;53:95-106
73
De Sarro G, et al.:Neuropharmacology. 1996;35:153-158
74
Smith SE, et al.:Epilepsy Res. 1993;15:101-111
75
Hosford DA, et al.:Epilepsia. 1997;38:408-414
76
遺伝的てんかんモデル動物での評価(ELマウス)(ラミクタール錠:2008年10月16日承認、申請資料概要 2.6.2.2.1.4)














 0120-041-189
0120-041-189

