1
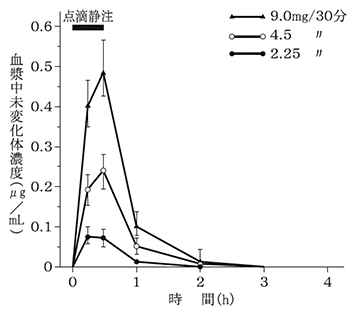
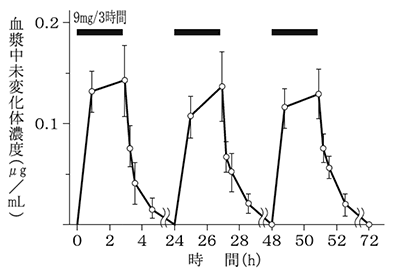
長沢 洋, 他: 臨床薬理. 1981; 12(3): 359-375
2
龍野 淳, 他: 薬理と治療. 1986; 14(S5): 1105-1111
3
社内資料: アルガトロバンの代謝に関与するヒトチトクロームP450(CYP)分子種の推定(2008年7月16日承認、CTD2.7.2.2)
4
井澤 修, 他: 薬理と治療. 1986; 14(S5): 1113-1125
5
田崎義昭, 他: 臨床と研究. 1986; 63(9): 3047-3057
6
田崎義昭, 他: 医学のあゆみ. 1987; 141(8): 499-515
7
田辺達三, 他: 循環器科. 1987; 22(2): 185-202
8
社内資料: アルガトロバンのヘパリン起因性血小板減少症に対する臨床試験(自らが実施する治験)(2008年7月16日承認、CTD2.7.6(1))
9
社内資料: An open-label study of argatroban in patients with heparin-induced thrombocytopenia(HIT). 2008年7月16日承認、CTD2.7.6(2))
10
Ota K, et al.: Nephrol Dial Transplant. 2003; 18(8): 1623-1630
11
Kikumoto R, et al.: Biochemistry. 1984; 23(1): 85-90
12
Okamoto S, et al.:Biochem Biophys Res Commun 1981; 101(2): 440-446
13
田中友二, 他: 臨床医薬. 1987; 3(1): 133-142
14
田辺達三, 他: 臨床医薬. 1986; 2(12): 1635-1644
15
松井則明, 他: 人工臓器. 1982; 11(2): 525-528
16
伊藤勝朗, 他: 外科診療. 1987; 29(1): 122-126
17
玉尾嘉邦, 他: 薬理と治療. 1986; 14(S5): 869-874
18
原 啓人, 他: 薬理と治療. 1986; 14(S5): 875-881
19
Nakamura K, et al.: Thromb Res. 1985; 40(5): 715-720
20
Kawai H, et al.: J Pharmacol Exp Ther. 1996; 278(2): 780-785
21
Kawai H, et al.: Jpn J Pharmacol. 1995; 69(2): 143-148
22
岩本政博, 他: 薬理と治療. 1986; 14(S5): 903-911
23
Kumada T, et al.: Thromb Res. 1981; 24(4): 285-298
24
Kawada T, et al.: Artif Organs Today. 1992; 2(3): 177-184