1
堀本政夫, 他:応用薬理. 1990;39(1):29-38
2
Berit PJ, et al.:J Hum Lact. 2013;29(2):150-153
3
Kloner RA, et al.:J Urol. 2004;172(5Pt1):1935-1940
4
厚生省医薬安全局:医薬品研究. 1998;29(8):627, 636-638
5
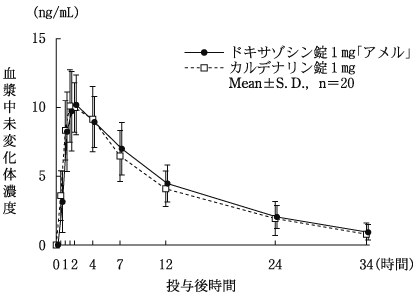
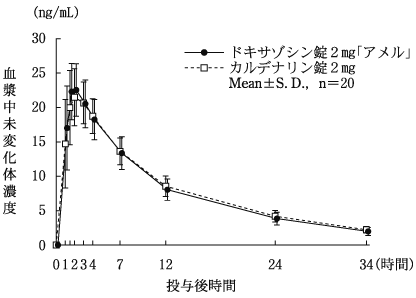
社内資料:生物学的同等性試験[錠1mg、錠2mg]
6
Penenberg D, et al.:J Clin Pharmacol. 2000;40(1):67-73
7
社内資料:生物学的同等性試験(溶出挙動比較)
8
第十八改正日本薬局方解説書. 廣川書店. 2021;C-3474








 0120-041-189
0120-041-189

