1
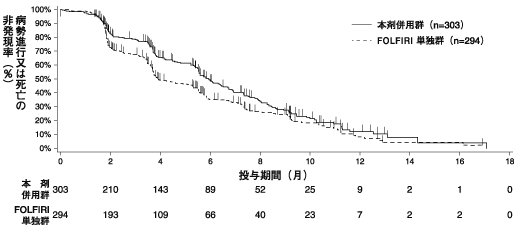
Hecht JR, et al.: J.Clin.Oncol. 2009 ; 27 : 672-680.
2
パニツムマブの臨床試験成績①(2010年4月16日承認、CTD 2.7.6.7)
3
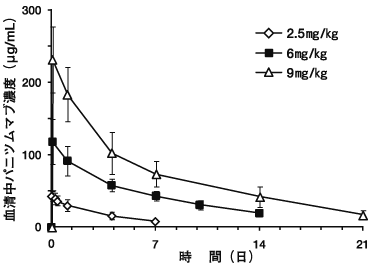
パニツムマブの臨床薬理試験全試験を通しての結果の比較と解析(2010年4月16日承認、CTD 2.7.2.3)
4
パニツムマブの薬物動態試験の概要:分布(2010年4月16日承認、CTD 2.6.4.4)
5
パニツムマブの薬物動態試験の概要:排泄(2010年4月16日承認、CTD 2.6.4.6)
6
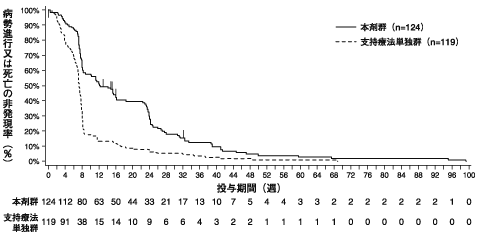
パニツムマブの臨床試験成績②(2010年4月16日承認、CTD 2.7.6.3)
7
パニツムマブの臨床試験成績③(2010年4月16日承認、CTD 2.7.6.1)
8
社内資料:パニツムマブの海外第Ⅲ相試験成績(20020408試験)
9
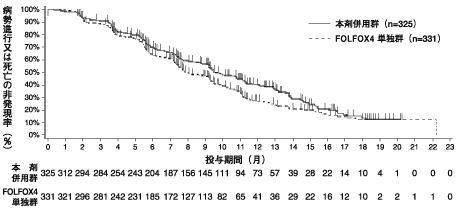
パニツムマブの臨床試験成績④(2010年4月16日承認、CTD 2.7.6.21)
10
Douillard JY, et al.: N Engl J Med. 2013 ; 369 : 1023-1034.
11
パニツムマブの臨床試験成績⑤(2010年4月16日承認、CTD 2.7.6.20)
12
Peeters M, et al.: Clin Cancer Res. 2015 ; 21 : 5469-5479.
13
Davis CG, et al.: Cancer Metastasis Rev. 1999 ; 18 : 421-425.
14
Yang XD, et al.: Cancer Res. 1999 ; 59 : 1236-1243.
15
Yang XD, et al.: Crit.Rev.Oncol.Hematol. 2001 ; 38 : 17-23.
16
パニツムマブの非臨床薬理試験成績(2010年4月16日承認、CTD 2.6.2.2)