作成又は改訂年月
**
2020年9月改訂
(第6版)
*
2019年3月改訂
日本標準商品分類番号
薬効分類名
承認等
販売名
セフジニルカプセル50mg「日医工」
販売名コード
承認・許可番号
22100AMX00031000
Cefdinir
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
室温保存
使用期限
外箱等に表示の使用期限内に使用すること
基準名
規制区分
処方箋医薬品
(注意−医師等の処方箋により使用すること)
組成
有効成分
1カプセル中
セフジニル
50mg(力価)
添加物
トウモロコシデンプン,カルメロースカルシウム,沈降炭酸カルシウム,ラウリル硫酸ナトリウム,ステアリン酸マグネシウム,二酸化ケイ素
カプセル本体:ゼラチン,酸化チタン,三二酸化鉄,黄色三二酸化鉄,ラウリル硫酸ナトリウム
製剤の性状
| 剤形 | 硬カプセル剤 |
|---|
| 色調 | 淡赤色不透明 |
|---|
| 外形 |  |
|---|
| 大きさ | 5号カプセル |
|---|
| 本体コード | 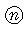 305 305 |
|---|
| 包装コード | 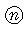 305 305 |
|---|
販売名
セフジニルカプセル100mg「日医工」
販売名コード
承認・許可番号
21900AMX00973000
Cefdinir
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
室温保存
使用期限
外箱等に表示の使用期限内に使用すること
基準名
規制区分
処方箋医薬品
(注意−医師等の処方箋により使用すること)
組成
有効成分
1カプセル中
セフジニル
100mg(力価)
添加物
トウモロコシデンプン,カルメロースカルシウム,沈降炭酸カルシウム,ラウリル硫酸ナトリウム,ステアリン酸マグネシウム,二酸化ケイ素
カプセル本体:ゼラチン,酸化チタン,三二酸化鉄,黄色三二酸化鉄,ラウリル硫酸ナトリウム
製剤の性状
| 剤形 | 硬カプセル剤 |
|---|
| 色調 | 淡赤色不透明 |
|---|
| 外形 |  |
|---|
| 大きさ | 4号カプセル |
|---|
| 本体コード | 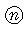 306 306 |
|---|
| 包装コード |  306 306 |
|---|
禁忌
原則禁忌
*セフェム系抗生物質に対し過敏症の既往歴のある患者
効能又は効果
効能又は効果に関連する使用上の注意
**咽頭・喉頭炎,扁桃炎,急性気管支炎,中耳炎,副鼻腔炎への使用にあたっては,「抗微生物薬適正使用の手引き」1)を参照し,抗菌薬投与の必要性を判断した上で,本剤の投与が適切と判断される場合に投与すること。
<適応菌種>
本剤に感性のブドウ球菌属,レンサ球菌属,肺炎球菌,淋菌,モラクセラ(ブランハメラ)・カタラーリス,大腸菌,クレブシエラ属,プロテウス・ミラビリス,プロビデンシア属,インフルエンザ菌,ペプトストレプトコッカス属,アクネ菌
<適応症>
表在性皮膚感染症,深在性皮膚感染症,リンパ管・リンパ節炎,慢性膿皮症,外傷・熱傷及び手術創等の二次感染,乳腺炎,肛門周囲膿瘍,咽頭・喉頭炎,扁桃炎,急性気管支炎,肺炎,膀胱炎,腎盂腎炎,尿道炎,バルトリン腺炎,子宮内感染,子宮付属器炎,麦粒腫,瞼板腺炎,外耳炎,中耳炎,副鼻腔炎,歯周組織炎,歯冠周囲炎,顎炎
用法及び用量
通常,セフジニルとして成人1回100mg(力価)を1日3回経口投与する。
なお,年齢及び症状に応じて適宜増減する。
用法及び用量に関連する使用上の注意
本剤の使用にあたっては,耐性菌の発現等を防ぐため,原則として感受性を確認し,疾病の治療上必要な最小限の期間の投与にとどめること。
高度の腎障害のある患者では血中濃度が持続するので,腎障害の程度に応じて投与量を減量し,投与の間隔をあけて使用すること。血液透析患者では1日100mg1回投与が望ましい。
鉄剤との併用は避けることが望ましい。
やむを得ず併用する場合には,本剤の投与後3時間以上間隔をあけて投与する。(「相互作用」の項参照)
使用上の注意
慎重投与
ペニシリン系抗生物質に対し,過敏症の既往歴のある患者
本人又は両親,兄弟に気管支喘息,発疹,蕁麻疹等のアレルギー症状を起こしやすい体質を有する患者
高度の腎障害のある患者(「用法・用量に関連する使用上の注意」の項参照)
経口摂取の不良な患者又は非経口栄養の患者,全身状態の悪い患者[ビタミンK欠乏症状があらわれることがあるので,観察を十分に行うこと。]
高齢者(「高齢者への投与」の項参照)
重要な基本的注意
ショックがあらわれるおそれがあるので,十分な問診を行うこと。
相互作用
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| 鉄剤 | 本剤の吸収を約10分の1まで阻害するので,併用は避けることが望ましい。やむを得ず併用する場合には,本剤の投与後3時間以上間隔をあけて投与する。 | 腸管内において鉄イオンとほとんど吸収されない錯体を形成する。 |
| ワルファリンカリウム | ワルファリンカリウムの作用が増強されるおそれがある。ただし,本剤に関する症例報告はない。 | 腸内細菌によるビタミンKの産生を抑制することがある。 |
| 制酸剤(アルミニウム又はマグネシウム含有) | 本剤の吸収が低下し,効果が減弱されるおそれがあるので,本剤の投与後2時間以上間隔をあけて投与する。 | 機序不明 |
副作用
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用
ショック(頻度不明)
ショックを起こすことがあるので,観察を十分に行い,不快感,口内異常感,喘鳴,眩暈,便意,耳鳴,発汗等があらわれた場合には投与を中止し,適切な処置を行うこと。
アナフィラキシー(頻度不明)
アナフィラキシー(呼吸困難,全身潮紅,血管浮腫,蕁麻疹等)があらわれることがあるので,観察を十分に行い,異常が認められた場合には投与を中止し,適切な処置を行うこと。
皮膚障害(頻度不明)
中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN),皮膚粘膜眼症候群(Stevens−Johnson症候群)があらわれることがあるので,観察を十分に行い,発熱,頭痛,関節痛,皮膚や粘膜の紅斑・水疱,皮膚の緊張感・灼熱感・疼痛等が認められた場合には投与を中止し,適切な処置を行うこと。
血液障害(頻度不明)
汎血球減少,無顆粒球症(初期症状:発熱,咽頭痛,頭痛,倦怠感等),血小板減少(初期症状:点状出血,紫斑等),溶血性貧血(初期症状:発熱,ヘモグロビン尿,貧血症状等)があらわれることがあるので,定期的に検査を行うなど観察を十分に行い,異常が認められた場合には投与を中止し,適切な処置を行うこと。
大腸炎(頻度不明)
偽膜性大腸炎等の血便を伴う重篤な大腸炎があらわれることがある。腹痛,頻回の下痢があらわれた場合には直ちに投与を中止し,適切な処置を行うこと。
間質性肺炎,PIE症候群(頻度不明)
発熱,咳嗽,呼吸困難,胸部X線異常,好酸球増多等を伴う間質性肺炎,PIE症候群等があらわれることがあるので,このような症状があらわれた場合には投与を中止し,副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
腎障害(頻度不明)
急性腎障害等の重篤な腎障害があらわれることがあるので,定期的に検査を行うなど観察を十分に行い,異常が認められた場合には投与を中止し,適切な処置を行うこと。
劇症肝炎,肝機能障害,黄疸(頻度不明)
劇症肝炎等の重篤な肝炎,著しいAST(GOT),ALT(GPT),Al-Pの上昇等を伴う肝機能障害,黄疸があらわれることがあるので,定期的に検査を行うなど観察を十分に行い,異常が認められた場合には投与を中止し,適切な処置を行うこと。
その他の副作用
| | 頻度不明 |
| 過敏症注) | 発疹,蕁麻疹,そう痒,発熱,浮腫,紅斑 |
| 血液 | 好酸球増多,顆粒球減少 |
| 腎臓 | BUN上昇 |
| 消化器 | 下痢,腹痛,胃部不快感,悪心,嘔吐,胸やけ,食欲不振,便秘 |
| 菌交代症 | 口内炎,カンジダ症,黒毛舌 |
| ビタミン欠乏症 | ビタミンK欠乏症状(低プロトロンビン血症,出血傾向等),ビタミンB群欠乏症状(舌炎,口内炎,食欲不振,神経炎等) |
| その他 | めまい,頭痛,胸部圧迫感,しびれ |
高齢者への投与
高齢者には次の点に注意し,用量並びに投与間隔に留意するなど患者の状態を観察しながら,慎重に投与すること。
1高齢者では生理機能が低下していることが多く,副作用が発現しやすい。
2高齢者ではビタミンK欠乏による出血傾向があらわれることがある。
妊婦、産婦、授乳婦等への投与
妊婦又は妊娠している可能性のある婦人には,治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。[妊娠中の投与に関する安全性は確立していない。]
小児等への投与
小児等に対する安全性は確立していない。(使用経験が少ない。)
臨床検査結果に及ぼす影響
テステープ反応を除くベネディクト試薬,フェーリング試薬による尿糖検査では偽陽性を呈することがあるので注意すること。
直接クームス試験陽性を呈することがあるので注意すること。
適用上の注意
薬剤交付時
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。(PTPシートの誤飲により,硬い鋭角部が食道粘膜へ刺入し,更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することが報告されている。)
その他の注意
粉ミルク,経腸栄養剤など鉄添加製品との併用により,便が赤色調を呈することがある。
尿が赤色調を呈することがある。
薬物動態
生物学的同等性試験
セフジニルカプセル100mg「日医工」及び標準製剤を,クロスオーバー法によりそれぞれ1カプセル(セフジニルとして100mg(力価))健康成人男子に絶食単回経口投与して血漿中セフジニル濃度を測定し,得られた薬物動態パラメータ(AUC,Cmax)について90%信頼区間法にて統計解析を行った結果,log(0.8)〜log(1.25)の範囲内であり,両剤の生物学的同等性が確認された。
2)また,セフジニルカプセル50mg「日医工」は,「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン(平成18年11月24日 薬食審査発第1124004号)」に基づき,セフジニルカプセル100mg「日医工」を標準製剤としたとき,溶出挙動が等しく,生物学的に同等とみなされた。
2)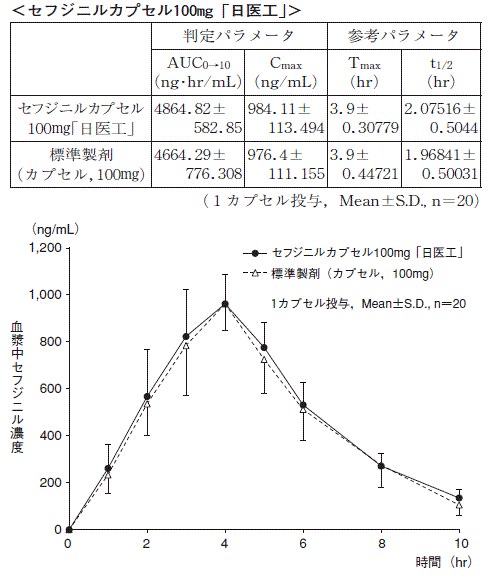
血漿中濃度並びにAUC,Cmax等のパラメータは,被験者の選択,体液の採取回数・時間等の試験条件によって異なる可能性がある。
溶出挙動
セフジニルカプセル50mg「日医工」及びセフジニルカプセル100mg「日医工」は,日本薬局方医薬品各条に定められたセフジニルカプセル(50mg,100mg)の溶出規格に適合していることが確認されている。3)
薬効薬理
セフジニルの作用点は菌種により異なるが,ペニシリン結合たん白(PBP)の1(1a,1bs),2及び3に親和性が高く,細菌細胞壁の合成を阻害することで抗菌作用を発揮する。
グラム陽性菌及び陰性菌に広範囲な抗菌スペクトルを持ち,特にグラム陽性菌のブドウ球菌属,レンサ球菌属などに対して従来の経口用セフェム剤よりも強く,殺菌的に作用する。
β-ラクタマーゼに安定で,β-ラクタマーゼ産生菌にもすぐれた抗菌力を示す。4)
有効成分に関する理化学的知見
一般名
セフジニル(Cefdinir)
略号
CFDN
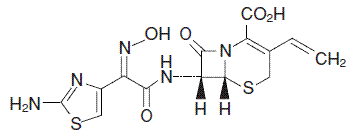
化学名
(6R,7R)-7-[(Z)-2-(2-Aminothiazol-4-yl)-2-(hydroxyimino)acetylamino]-8-oxo-3-vinyl-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid
構造式
分子式
C14H13N5O5S2
分子量
395.41
性状
白色〜淡黄色の結晶性の粉末である。
水,エタノール(95)又はジエチルエーテルにほとんど溶けない。
pH7.0の0.1mol/Lリン酸塩緩衝液に溶ける。
取扱い上の注意
安定性試験
長期保存試験(25℃)の結果より,セフジニルカプセル50mg「日医工」及びセフジニルカプセル100mg「日医工」は通常の市場流通下において2年間安定であることが確認された。5)
包装
セフジニルカプセル50mg「日医工」
100カプセル(10カプセル×10;PTP)
セフジニルカプセル100mg「日医工」
100カプセル(10カプセル×10;PTP)
500カプセル(10カプセル×50;PTP)
主要文献及び文献請求先
主要文献
1
厚生労働省健康局結核感染症課編:抗微生物薬適正使用の手引き
2
日医工株式会社 社内資料:生物学的同等性試験
3
日医工株式会社 社内資料:溶出試験
4
第十七改正日本薬局方解説書 C-2724,廣川書店,東京(2016)
5
日医工株式会社 社内資料:安定性試験
文献請求先
主要文献欄に記載の文献・社内資料は下記にご請求下さい。
日医工株式会社 お客様サポートセンター
〒930-8583 富山市総曲輪1丁目6番21
フリーダイアル(0120)517-215
Fax(076)442-8948
製造販売業者等の氏名又は名称及び住所
製造販売元
日医工株式会社
富山市総曲輪1丁目6番21

 305
305 305
305
 306
306 306
306