1
厚生労働省健康局結核感染症課編:抗微生物薬適正使用の手引き
2
日本薬局方 医薬品情報:じほう. 2001;220-224
3
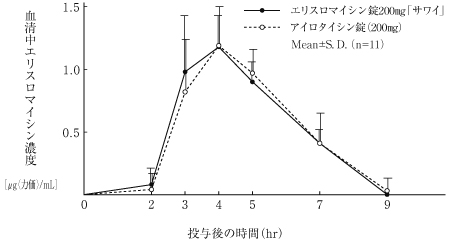
社内資料:生物学的同等性試験
4
黒田善雄:Chemotherapy, 1958;6(6):343-360
5
深谷一太他:Chemotherapy, 1970;18(3):252-258
6
Bergogne-Bérézin, E. et al.:Int. J. Clin. Pharmacol. Res., 1985;5(5):341-344
7
Watkins, P. B. et al.:Proc. Natl. Acad. Sci., 1985;82(18):6310-6314
8
Brian, W. R. et al.:Biochemistry, 1990;29:11280-11292
9
Wells, J. S. et al.:Antibiot. Annu., 1955;1954/1955:291-294
10
小野一男:モダンテラピー, 1953;6:8-13
11
Kroboth, P. D. et al.:Antimicrob. Agents Chemother, 1982;21(1):135-140
12
第十八改正日本薬局方解説書;廣川書店. 2021;C-1078-1085