1
社内資料:生物学的同等性試験[錠100mg]
2
Aono, T. et al.:J. Clin. Endocrinol. Metab. 1979;48(3):478-482
3
社内資料:生物学的同等性試験(動物)
4
第十八改正日本薬局方解説書. 廣川書店. 2021;C-2605
精神情動安定剤
1錠 6.4円
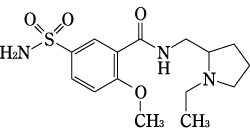
有効成分 | 1錠中、日局スルピリド 100mgを含有する。 |
|---|---|
添加剤 | 乳糖水和物、低置換度ヒドロキシプロピルセルロース、ヒドロキシプロピルセルロース、タルク、ステアリン酸マグネシウム、ヒプロメロース、酸化チタン、マクロゴール6000、カルナウバロウ |
有効成分 | 1錠中、日局スルピリド 200mgを含有する。 |
|---|---|
添加剤 | クロスカルメロースナトリウム、結晶セルロース、ヒドロキシプロピルセルロース、タルク、ステアリン酸マグネシウム、ヒプロメロース、酸化チタン、マクロゴール6000、カルナウバロウ |
| 剤形 | フィルムコーティング錠 |
|---|---|
| 色調 | 白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 約7.1mm 大きさ(厚さ) 約3.2mm |
| 質量 | 約123mg |
| 識別コード | Kw212 |
| 剤形 | フィルムコーティング錠 |
|---|---|
| 色調 | 白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 約9.1mm 大きさ(厚さ) 約3.8mm |
| 質量 | 約245mg |
| 識別コード | Kw222 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
QT延長を起こすことが知られている薬剤 イミプラミン ピモジド 等 | QT延長、心室性不整脈等の重篤な副作用を起こすおそれがある。 | 本剤及びこれらの薬剤はいずれもQT間隔を延長させるおそれがあるため、併用により作用が増強するおそれがある。 |
ジギタリス剤 ジゴキシン ジギトキシン 等 | ジギタリス剤飽和時の指標となる悪心・嘔吐、食欲不振症状を不顕性化するおそれがある。 | 本剤の制吐作用による。 |
ベンザミド系薬剤 メトクロプラミド チアプリド 等 フェノチアジン系薬剤 クロルプロマジン 等 ブチロフェノン系薬剤 ハロペリドール 等 | 内分泌機能異常、錐体外路症状が発現しやすくなる。 | 本剤及びこれらの薬剤は抗ドパミン作用を有するため、併用により抗ドパミン作用が強くあらわれる。 |
中枢神経抑制剤 バルビツール酸誘導体 麻酔剤 等 | 相互に中枢神経抑制作用を増強させることがある。 | 本剤及びこれらの薬剤は中枢神経抑制作用を有する。 |
ドパミン作動薬 レボドパ 等 | 相互に作用を減弱させることがある。 | 本剤は抗ドパミン作用を有するため、作用が拮抗する。 |
アルコール 飲酒 | 相互に中枢神経抑制作用を増強させることがある。 | ともに中枢神経抑制作用を有する。 |
0.1~5%未満 | 0.1%未満 | |
|---|---|---|
心・血管系注1) | 血圧下降 | 心電図異常、血圧上昇、胸内苦悶、頻脈 |
錐体外路症状注2) | パーキンソン症候群(振戦、筋強剛、流涎等)、ジスキネジア(舌のもつれ、言語障害、頸筋捻転、眼球回転、注視痙攣、嚥下困難等)、アカシジア(静坐不能) | |
内分泌 | 乳汁分泌、女性化乳房、月経異常、射精不能 | 乳房腫脹、勃起不全 |
精神神経系 | 睡眠障害、不穏、焦燥感、眠気、頭痛、頭重、めまい、浮遊感、興奮、躁転、躁状態、しびれ、運動失調 | 物忘れ、ぼんやり、徘徊、多動、抑制欠如、無欲状態 |
消化器 | 悪心、嘔吐、口渇、便秘、食欲不振、腹部不快感 | 下痢、胸やけ、腹痛、食欲亢進 |
肝臓 | AST、ALT、Al-P等の上昇 | |
皮膚 | 発疹 | そう痒感 |
眼 | 視力障害、眼球冷感・重感、眼のちらつき | |
その他 | 体重増加、浮腫、脱力感、倦怠感、排尿困難、性欲減退 | 頻尿、腰痛、肩こり、熱感、発熱、発汗、鼻閉 |
AUC(0→48) (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
スルピリド錠100mg「アメル」 | 2601.75±472.50 | 212.95±65.03 | 3.90±1.20 | 12.02±1.40 |
ドグマチール錠100mg | 2581.98±492.97 | 207.13±58.14 | 3.80±1.10 | 11.92±3.19 |
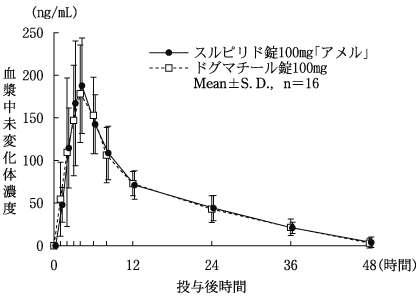
AUC(0→36) (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
スルピリド錠200mg「アメル」 | 26320.94±4876.34 | 3720.73±826.96 | 1.42±0.51 | 6.18±0.40 |
 0120-041-189
0120-041-189