1*厚生労働省健康局結核感染症課編:抗微生物薬適正使用の手引き
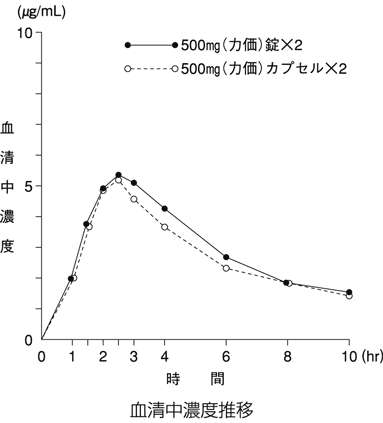
2ホスホマイシンの生物学的同等性試験(社内資料)
3川畑徳幸ほか:Chemotherapy,23(5):1880,1975
4藤田公生ほか:Jpn. J. Antibiot.,41(5):567,1988
5中澤 昭ほか:眼科臨床医報,82(8):1523,1988
6高山幹子ほか:耳鼻と臨床,34(3):801,1988
7川久保淳ほか:耳鼻と臨床,34(4):1043,1988
8松原義雄ほか:感染症学雑誌,49(12):843,1975
9真下啓明ほか:Chemotherapy,23(5):1713,1975
10安田利顕ほか:臨床皮膚科,29(12):1081,1975
11石神襄次ほか:泌尿紀要,21(10):971,1975
12石神襄次ほか:泌尿紀要,24(9):757,1978
13宍戸仙太郎ほか:泌尿紀要,24(9):779,1978
14平石 浩ほか:感染症学雑誌,54(7):343,1980
15馬場駿吉ほか:耳鼻と臨床,29(5):584,1983
16富岡 昌ほか:耳鼻臨床,76(4):1291,1983
17大石正夫ほか:眼科臨床医報,77(7):1095,1983
18宮内慶之輔ほか:Jpn. J. Antibiot.,28(3):320,1975
19Fosfomycinの作用機作(社内資料)
20Kahan, F.M., et al.:Ann. N. Y. Acad. Sci.,235:364,1974
21鶴岡 勉:日本化学療法学会雑誌,47(3):115,1999