1
Yamaguchi T., et al.: Arzneim.-Forsch./Drug Res. 1994; 44: 59-64
2
社内資料: 錠5mgとOD錠5mgの同等性試験
3
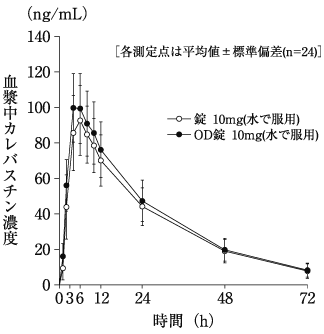
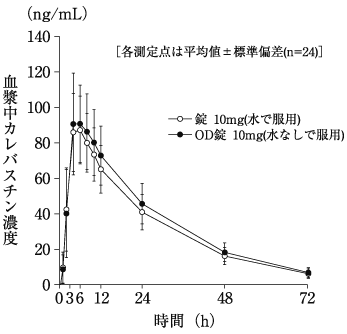
社内資料: 錠10mgとOD錠10mgの同等性試験
4
Fujii T., et al.: Arzneim.-Forsch./Drug Res. 1994; 44: 527-538
5
橋爪孝典: Progress in Medicine. 2003; 23: 282-287
6
Hashizume T., et al.: J. Pharmacol. Exp. Ther. 2002; 300: 298-304
7
長澤絋一ほか: 臨床医薬. 1995; 11: 1213-1226
8
久木田 淳ほか: 臨床医薬. 1994; 10(Suppl. 1): 55-72
9
馬場駿吉ほか: 臨床医薬. 1994; 10(Suppl. 1): 125-145
10
久木田 淳ほか: 臨床医薬. 1994; 10: 895-912
11
馬場駿吉ほか: 臨床医薬. 1994; 10: 1143-1162
12
久木田 淳ほか: 臨床医薬. 1994; 10(Suppl. 1): 43-53
13
久木田 淳ほか: 臨床医薬. 1994; 10(Suppl. 1): 89-102
14
久木田 淳ほか: 臨床医薬. 1994; 10(Suppl. 1): 73-88
15
馬場駿吉ほか: 臨床医薬. 1994; 10(Suppl. 1): 113-124
16
馬場駿吉ほか: 臨床医薬. 1994; 10(Suppl. 1): 177-188
17
馬場駿吉ほか: 臨床医薬. 1994; 10(Suppl. 1): 163-176
18
馬場駿吉ほか: 臨床医薬. 1994; 10(Suppl. 1): 147-161
19
薬王郁久ほか: 日本薬理学雑誌. 1994; 103: 121-135
20
久木田 淳ほか: 臨床医薬. 1994; 10(Suppl. 1): 103-111