アレルギー性疾患治療剤
1g 6.5円
| 剤形 | 性状 |
| ドライシロップ | 白色の粉末を含む微粒子で、ストロベリー様の芳香があり、味は甘い |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| 中枢神経抑制剤 鎮静剤 催眠剤 等 抗ヒスタミン剤 アルコール | 眠気、精神運動機能低下等を起こすことがある。 アルコール性飲料の摂取を制限すること。 | いずれも中枢神経抑制作用を有するため。 |
| 頻度不明 | |
| 泌尿器注) | 頻尿、排尿痛、血尿、残尿感等の膀胱炎様症状 |
| 過敏症注) | 浮腫、多形紅斑、発疹、蕁麻疹 |
| *精神神経系 | 一過性の意識消失注)、頭痛、味覚異常、しびれ感、易刺激性、不眠、神経過敏、鎮静、眠気、めまい、ふらつき、倦怠感、口渇 |
| 消化器 | 腹痛、胃部不快感、食欲不振、口内炎、悪心、下痢、嘔吐、便秘 |
| 肝臓 | LDH、γ-GTP、AST(GOT)、ALT(GPT)、Al-Pの上昇 |
| その他 | ほてり、鼻出血、動悸、月経異常、体重増加 |
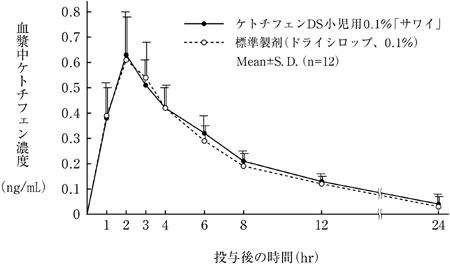
| Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | AUC0-24hr(ng・hr/mL) | |
| ケトチフェンDS小児用0.1%「サワイ」 | 0.65±0.15 | 2.2±0.6 | 7.2±3.1 | 4.66±0.88 |
| 標準製剤(ドライシロップ、0.1%) | 0.63±0.16 | 2.3±0.5 | 7.8±3.9 | 4.45±1.07 |