〈レナリドミド及びデキサメタゾン併用〉
国内第Ⅰ相試験(ONO-7057-05試験)
前治療歴が1回以上の再発又は難治性の多発性骨髄腫患者26例に、本剤注1)、レナリドミド注2)及びデキサメタゾン注3)を併用投与した。奏効率は、88.5%[90%信頼区間:72.8~96.8%](完全奏効1例、最良部分奏効5例、部分奏効17例(国際骨髄腫ワーキンググループ基準に基づく治験責任医師判定))であった。なお、事前に設定した閾値は66.7%であった。また、安全性評価対象となった26例中26例(100%)に副作用(臨床検査値の異常を含む)が認められた。主な副作用(10%以上)は、血小板減少12例(46.2%)、リンパ球減少11例(42.3%)、高血糖10例(38.5%)、ALT増加7例(26.9%)、発疹7例(26.9%)、便秘6例(23.1%)、筋痙縮6例(23.1%)、低リン酸血症5例(19.2%)、白血球増加5例(19.2%)、AST増加4例(15.4%)、好中球減少4例(15.4%)、好中球増加4例(15.4%)、発熱4例(15.4%)、末梢性ニューロパチー4例(15.4%)、血中ビリルビン増加4例(15.4%)、白血球減少4例(15.4%)、高カリウム血症3例(11.5 %)、低カリウム血症3例(11.5%)、悪心3例(11.5%)、高血圧3例(11.5%)、下痢3例(11.5%)、肺炎3例(11.5%)、上気道の炎症3例(11.5%)、味覚異常3例(11.5%)、紅斑3例(11.5%)、血中コレステロール増加3例(11.5%)、ヘモグロビン減少3例(11.5%)及び低ナトリウム血症3例(11.5%)であった。
海外第Ⅲ相試験(PX-171-009試験)
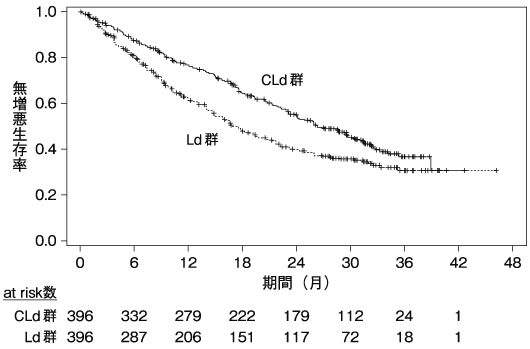
前治療歴が1~3回の再発又は難治性の多発性骨髄腫患者注4)792例(各群396例)に対して、レナリドミド注2)及びデキサメタゾン注3)の併用(Ldレジメン)とLdレジメンに本剤注1)を上乗せしたCLdレジメンを比較した。主要評価項目である無増悪生存期間の結果(中央値[95%信頼区間])は、CLd群で26.3[23.3~30.5]ヵ月、Ld群で17.6[15.0~20.6]ヵ月であり、Ld群に対してCLd群で統計学的に有意な延長を示した(ハザード比0.69[95%信頼区間:0.57~0.83]、p<0.0001[層別log-rank検定]、2014年6月16日データカットオフ)。
また、副次評価項目である全生存期間の中間解析結果(中央値)は、CLd群、Ld群いずれも未到達であり、統計学的に有意な延長は認められていない(ハザード比0.787[95%信頼区間:0.628~0.985]、p=0.0182[層別log-rank検定]、2014年6月16日データカットオフ)。また、安全性評価対象となった392例中332例(84.7%)に副作用(臨床検査値の異常を含む)が認められた。主な副作用(10%以上)は、好中球減少142例(36.2%)、貧血104例(26.5%)、血小板減少99例(25.3%)、疲労88例(22.4%)、下痢74例(18.9%)、筋痙縮72例(18.4%)、不眠症56例(14.3%)、気道感染50例(12.8%)、低カリウム血症43例(11.0%)、高血糖41例(10.5%)及び無力症41例(10.5%)であった。
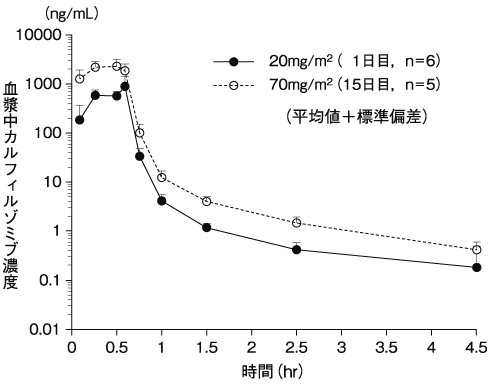
注1)本剤の用法及び用量:28日間を1サイクルとし、1日1回、1、2、8、9、15、16日目に点滴静注した。投与量は、1サイクル目の1、2日目のみ20mg/m2(体表面積)、それ以降は27mg/m2(体表面積)で点滴静注し12サイクルまで繰り返した。13サイクル目以降は、27mg/m2を1日1回、1、2、15、16日目に点滴静注した。なお、18サイクルを超える投与は許容されなかった。
注2)レナリドミドの用法及び用量:28日間を1サイクルとし、25mgを1日1回、21日間経口投与した。
注3)デキサメタゾンの用法及び用量:28日間を1サイクルとし、40mgを1日1回、1、8、15、22日目に経口投与した。デキサメタゾンの投与日が本剤と同日の場合、本剤投与の4時間~30分前に投与した。
なお、国内第Ⅰ相試験(ONO-7057-05試験)では、第1サイクルのカルフィルゾミブの投与日のうち、デキサメタゾン40mgを投与しない投与日については、カルフィルゾミブの投与前にデキサメタゾン4mgを経口又は静脈内投与した。また、第1サイクルにカルフィルゾミブに関連する発熱、悪寒、寒気又は息切れなどが認められた場合は、原則としてデキサメタゾン4mgの投与を第2サイクル以降も継続することとし、第2サイクル以降で、デキサメタゾンを使用していない間にこれらの症状が発現した場合は、原則としてデキサメタゾン4mgの投与を再開することとした。
注4)①ボルテゾミブによる治療中に疾患進行が認められた患者、②レナリドミド及びデキサメタゾンの併用投与による治療開始後3ヵ月以内に疾患進行が認められた患者並びに③レナリドミド及びデキサメタゾンの併用投与による直近の治療中に疾患進行が認められた患者は除外された。
〈デキサメタゾン併用〉
国際共同第Ⅲ相試験(2011-003試験)
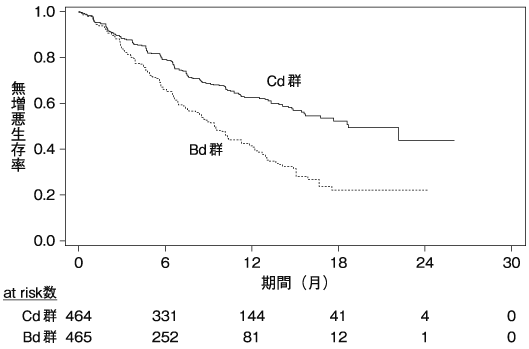
前治療歴が1~3回の再発又は難治性の多発性骨髄腫患者注5)929例(日本人患者44例を含む。Cd群464例、Bd群465例)に対して、ボルテゾミブ注6)及びデキサメタゾン注7)の併用(Bdレジメン)と本剤注8)及びデキサメタゾン注9)の併用(Cdレジメン)を比較した。主要評価項目である無増悪生存期間の結果(中央値[95%信頼区間])は、Cd群で18.7[15.6~NE注10)]ヵ月、Bd群で9.4[8.4~10.4]ヵ月であり、Bd群に対してCd群で統計学的に有意な延長を示した(ハザード比0.53[95%信頼区間:0.437~0.651]、p<0.0001[層別log-rank検定]、2014年11月10日データカットオフ)。
また、副次評価項目である全生存期間の中間解析結果(中央値)は、Cd群で未到達、Bd群で24.3[24.34~NE注10)]ヵ月であり、統計学的に有意な延長は認められていない(ハザード比0.786[95%信頼区間:0.575~1.075]、p=0.065[層別log-rank検定]、2014年11月10日データカットオフ)。また、安全性評価対象となった463例(日本人22例含む)中404例(87.3%)に副作用(臨床検査値の異常を含む)が認められた。主な副作用(10%以上)は、血小板減少126例(27.2%)、貧血107例(23.1%)、疲労97例(21.0%)、不眠症93例(20.1%)、呼吸困難74例(16.0%)、下痢69例(14.9%)、高血圧62例(13.4%)、悪心57例(12.3%)、無力症55例(11.9%)、末梢性ニューロパチー49例(10.6%)、リンパ球減少48例(10.4%)、発熱48例(10.4%)及び高血糖47例(10.2%)であった。
注5)①ボルテゾミブによる治療中に奏効が認められなかった患者、②ボルテゾミブによる治療に不耐容であった患者並びに③ボルテゾミブの最終投与から治験薬の初回投与までの期間が6ヵ月未満の患者は除外された。
注6)ボルテゾミブの用法及び用量:21日間を1サイクルとし、1.3mg/m2(体表面積)を1日1回、1、4、8、11日目に静脈内又は皮下投与した。
注7)デキサメタゾンの用法及び用量:21日間を1サイクルとし、20mgを1日1回、1、2、4、5、8、9、11、12日目に経口投与した。デキサメタゾンの投与日がボルテゾミブと同日の場合、ボルテゾミブ投与の4時間~30分前に投与した。
注8)本剤の用法及び用量:28日間を1サイクルとし、1日1回、1、2、8、9、15、16日目に点滴静注した。投与量は、1サイクル目の1、2日目のみ20mg/m2(体表面積)、それ以降は56mg/m2(体表面積)で点滴静注した。
注9)デキサメタゾンの用法及び用量:28日間を1サイクルとし、20mgを1日1回、1、2、8、9、15、16、22、23日目に経口投与した。デキサメタゾンの投与日が本剤と同日の場合、本剤投与の4時間~30分前に投与した。
注10)NEは推定不能
国際共同第Ⅲ相試験(20140355試験)
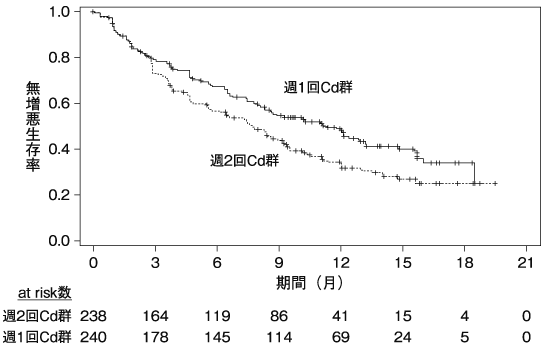
前治療歴が2~3回の再発又は難治性の多発性骨髄腫患者 478例(日本人患者40例を含む。週1回投与群240例、週2回投与群238例)に対して、本剤及びデキサメタゾン注11)の併用(Cdレジメン)における週1回投与注12)と週2回投与注13,14)を比較した。主要評価項目である無増悪生存期間の結果(中央値[95%信頼区間])は、週1回投与群で11.2[8.6~13.0]ヵ月、週2回投与群で7.6[5.8~9.2]ヵ月であり、週2回投与群に対して週1回投与群で統計学的に有意な延長を示した(ハザード比0.693[95%信頼区間:0.544~0.883]、p=0.0014[層別log-rank検定]、2017年6月15日データカットオフ)。
また、副次評価項目である全生存期間の結果(中央値)は、週1回投与群、週2回投与群いずれも未到達であり、統計学的に有意な延長は認められていない(ハザード比0.800[95%信頼区間:0.563~1.138]、p=0.1070[層別log-rank検定]、2017年6月15日データカットオフ)。また、安全性評価対象となった238例(日本人26例含む)中173例(72.7%)に副作用(臨床検査値の異常を含む)が認められた。主な副作用(10%以上)は、血小板減少37例(15.5%)、高血圧35例(14.7%)、不眠症29例(12.2%)、好中球減少26例(10.9%)、貧血25例(10.5%)、疲労25例(10.5%)及び悪心24例(10.1%)であった。
注11)デキサメタゾンの用法及び用量:28日間を1サイクルとし、40mgを1日1回、1、8、15、22日目に経口又は静脈内投与し、9サイクルまで繰り返した。10サイクル目以降は40mgを1日1回、1、8、15日目に経口又は静脈内投与した。デキサメタゾンの投与日が本剤と同日の場合、本剤投与の4時間~30分前に投与した。
注12)本剤の用法及び用量:28日間を1サイクルとし、1日1回、1、8、15日目に点滴静注した。投与量は、1サイクル目の1日目のみ20mg/m2(体表面積)、それ以降は70mg/m2(体表面積)で点滴静注した。
注13)本剤の用法及び用量:28日間を1サイクルとし、1日1回、1、2、8、9、15、16日目に点滴静注した。投与量は、1サイクル目の1、2日目のみ20mg/m2(体表面積)、それ以降は27mg/m2(体表面積)で点滴静注した。
注14)デキサメタゾン併用時における本剤の承認された用法及び用量とは異なる。
〈デキサメタゾン及びダラツムマブ(遺伝子組換え)併用〉
国際共同第Ⅲ相試験(20160275(CANDOR)試験)
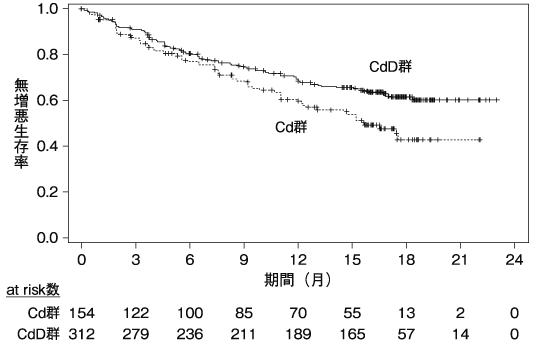
前治療歴が1~3回の再発又は難治性の多発性骨髄腫患者466 例(日本人患者31例を含む。CdD群312例、Cd群154例)に対して、本剤(週2回投与)注15)及びデキサメタゾン注16)の併用(Cdレジメン)とCdレジメンにダラツムマブ(遺伝子組換え)注17)を上乗せしたCdDレジメンを比較した。主要評価項目である無増悪生存期間の結果(中央値[95%信頼区間])は、CdD群でNE注18)[NE~NE]、Cd群で15.8[12.1~NE注18)]ヵ月であり、Cd群に対してCdD群で統計学的に有意な延長を示した(ハザード比0.630 [95%信頼区間:0.464~0.854]、p=0.0014[層別log-rank検定]、2019年7月14日データカットオフ)。
また、副次評価項目である全生存期間の結果(中央値)は、CdD群、Cd群いずれも未到達であり、統計学的に有意な延長は認められていない(ハザード比0.745 [95%信頼区間:0.491~1.131]、p=0.0836[層別log-rank検定]、2019年7月14日データカットオフ)。また、安全性評価対象となった308例(日本人20例含む)中260例(84.4%)に副作用(臨床検査値の異常を含む)が認められた。主な副作用(10%以上)は、血小板減少103例(33.4%)、高血圧79例(25.6%)、貧血56例(18.2%)、呼吸困難52例(16.9%)、不眠症51例(16.6%)、疲労46例(14.9%)、下痢46例(14.9%)、悪心33例(10.7%)及び好中球減少31例(10.1%)であった。
注15)本剤の用法及び用量:28日間を1サイクルとし、1日1回、1、2、8、9、15、16日目に点滴静注した。投与量は、1サイクル目の1、2日目のみ20mg/m2(体表面積)、それ以降は56mg/m2(体表面積)で点滴静注した。
注16)デキサメタゾンの用法及び用量:28日間を1サイクルとし、20mgを1、2、8、9、15、16日目に40mgを22日目(75歳超の場合は1週ごとに20mg)に経口又は静脈内投与した。デキサメタゾンの投与日が本剤と同日の場合、本剤投与の4時間~30分前、ダラツムマブ投与の1~3時間前に投与した。
注17)ダラツムマブ(遺伝子組換え)の用法及び用量:28日間を1サイクルとし、1回16mg/kgを、1週間間隔(1~8週目、初回のみ2日間に分割して8mg/kgずつ投与)、2週間間隔(9~24週目)、及び4週間間隔(25週目以降)で点滴静注した。
注18)NEは推定不能