1
陶易王他:新薬と臨床, 2006;55(6):856-862
2
第十八改正日本薬局方解説書, 廣川書店, 2021;C-1144
3
松本昌世他:日薬理誌, 1964;60:162-163
Caアスパルテート製剤
1錠 5.7円
有効成分 | L-アスパラギン酸カルシウム水和物 無水物として200mg(Ca2+:1.3mEq) |
|---|---|
添加剤 | ステアリン酸Mg、タルク、デキストリン、トウモロコシデンプン |
| 剤形 | 素錠 |
|---|---|
| 外形 | 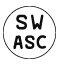   |
| 大きさ | 大きさ(直径) 9.0mm 大きさ(厚さ) 4.0mm |
| 質量 | 約275mg |
| 識別コード | SW ASC |
| 性状 | 白色 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
ジギタリス製剤 ジゴキシン、ジギトキシン | ジギタリス中毒(不整脈、ショック)があらわれることがある。 定期的にジギタリス中毒の有無、心電図検査を行い、必要に応じてジギタリス製剤の血中濃度を測定し、異常が認められた場合には、ジギタリス製剤の減量若しくは投与を中止する。 | ジギタリス製剤の作用を増強する。 |
テトラサイクリン系抗生物質 テトラサイクリン | テトラサイクリン系抗生物質の作用が減弱するおそれがある。 同時服用を避け、併用する場合には1~3時間以上あける等注意する。 | カルシウムイオンはキレート化によりテトラサイクリン系抗生物質の吸収を阻害する。 |
ニューキノロン系抗菌剤 シプロフロキサシン塩酸塩、ノルフロキサシン、トスフロキサシントシル酸塩水和物 | ニューキノロン系抗菌剤の作用が減弱するおそれがある。 同時服用を避け、併用する場合には、2時間以上あける等注意する。 | カルシウムイオンはキレート化によりニューキノロン系抗菌剤の吸収を阻害し、血中濃度を低下させる。 |
活性型ビタミンD製剤 アルファカルシドール カルシトリオール等 | 高カルシウム血症があらわれやすい。 | 腸管でのカルシウムの吸収が促進される。 |
0.1~5%未満 | 頻度不明 | |
|---|---|---|
長期投与 | 高カルシウム血症、結石症 | |
消化器 | 腹部膨満感、胸やけ、軟便 | |
その他 | 頭痛、心窩部不快感、発疹 |
最大尿中カルシウム排泄速度 (mg/hr) | 累積尿中カルシウム排泄量 (mg) | |
L-アスパラギン酸Ca錠200mg「サワイ」 | 9.16±2.73 | 54.97±15.75 |
アスパラ-CA錠200 | 8.80±2.77 | 52.06±15.71 |